解答题-原理综合题 适中0.65 引用2 组卷120
苯是重要的化工产品,也是化工原料,在生产中有广泛应用。回答下列问题:
已知: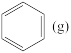 +H2(g)
+H2(g) 
反应I: ++H2(g)
++H2(g) 
 (1,
(1, 环己二烯;g)
环己二烯;g) 
反应II: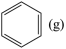 +2H2(g)
+2H2(g) 
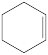 (g)
(g) 
反应III: +3H2(g)
+3H2(g) 
 (g)
(g) 
(1)反应: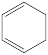 (1,3-环己二烯;g)+H2(g)
(1,3-环己二烯;g)+H2(g) 
 (g)
(g)
_______  ;苯的稳定性比1,
;苯的稳定性比1, 环已二烯
环已二烯_______ (填“强”或“弱”)。
(2)一定温度下,向恒容密闭容器中充入 苯蒸气和
苯蒸气和 氢气,在催化剂镍的条件下同时发生反应I、II、III,下列叙述正确的是_______(填标号)。
氢气,在催化剂镍的条件下同时发生反应I、II、III,下列叙述正确的是_______(填标号)。
(3)在体积相等、温度相同的甲、乙两个容器中起始都投入 苯蒸气和
苯蒸气和 氢气,只发生反应III
氢气,只发生反应III
用“>”、“<”或“=”填空:
①
_______  ;②
;②
_______  ;③
;③
_______  。
。
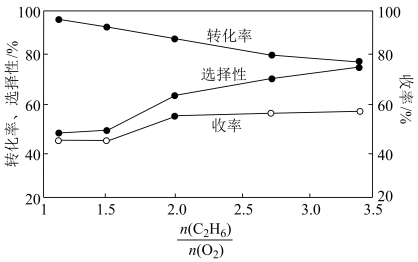
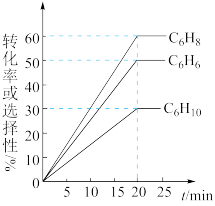
(4)一定温度下,向密闭容器中充入 苯(g)和
苯(g)和 同时发生反应I、II、III,测得苯的转化率和产物选择性如图所示(某一产物的选择性
同时发生反应I、II、III,测得苯的转化率和产物选择性如图所示(某一产物的选择性 ),已知:平衡时气体总压强为
),已知:平衡时气体总压强为 。
。 时1,
时1, 环己二烯的分压为
环己二烯的分压为_______  。上述反应I的平衡常数
。上述反应I的平衡常数
_______ (以分压表示,分压=总压×物质的量分数) 。
。
(5)对苯醌( )是制备口腔消毒剂的原料。以硫酸和硫酸钠的混合溶液为电解质溶液,用惰性电极电解苯可以制备对苯醌。则阳极的电极反应式为
)是制备口腔消毒剂的原料。以硫酸和硫酸钠的混合溶液为电解质溶液,用惰性电极电解苯可以制备对苯醌。则阳极的电极反应式为_______ 。
已知:
 +H2(g)
+H2(g) 反应I:
 ++H2(g)
++H2(g)  (1,
(1,反应II:
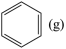 +2H2(g)
+2H2(g)  (g)
(g) 反应III:
 +3H2(g)
+3H2(g)  (g)
(g) (1)反应:
 (1,3-环己二烯;g)+H2(g)
(1,3-环己二烯;g)+H2(g)  (g)
(g)(2)一定温度下,向恒容密闭容器中充入
| A.气体密度不变时反应达到平衡状态 |
| B.混合气体中环己烷的体积分数可能等于50% |
| C.平衡后再充入少量氢气,平衡向正反应方向移动 |
| D.增大催化剂镍的质量,反应速率和苯的转化率都会增大 |
| 容器 | 甲 | 乙 |
| 反应条件 | 恒温恒容 | 绝热恒容 |
| 苯蒸气的平衡转化率 | ||
| 平衡时正反应速率 | ||
| 平衡常数 |
①
(4)一定温度下,向密闭容器中充入

(5)对苯醌(
 )是制备口腔消毒剂的原料。以硫酸和硫酸钠的混合溶液为电解质溶液,用惰性电极电解苯可以制备对苯醌。则阳极的电极反应式为
)是制备口腔消毒剂的原料。以硫酸和硫酸钠的混合溶液为电解质溶液,用惰性电极电解苯可以制备对苯醌。则阳极的电极反应式为22-23高三上·河北沧州·阶段练习
类题推荐
CO、CO2加氢有利于缓解化石能源消耗,实现“碳中和”.该体系主要涉及以下反应:
反应I:CO(g)+2H2(g) CH3OH(g) ΔH1<0
CH3OH(g) ΔH1<0
反应II:2CO(g)+4H2(g) C2H5OH(g)+H2O(g) ΔH2<0
C2H5OH(g)+H2O(g) ΔH2<0
反应III:2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) ΔH3<0
C2H5OH(g)+3H2O(g) ΔH3<0
反应IV:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH4<0
CH3OH(g)+H2O(g) ΔH4<0
反应V:2CH3OH(g) C2H5OH(g)+H2O(g) ΔH5
C2H5OH(g)+H2O(g) ΔH5
回答下列问题:
(1)上述反应中,ΔH5=____ (写出一个代数式即可)。
(2)密闭容器中,上述反应体系在一定条件下建立平衡后,下列描述正确的有____ (填标号)。
(3)恒容下,n(CO)=n(CO2)=1mol,并按照不同氢碳比[ ]投料,发生上述反应。图甲表示不同氢碳比时,[CO+CO2]的总平衡转化率随温度变化的关系;图乙表示氢碳比=3时,平衡后体系中C2H5OH、CH3OH的选择性随温度变化的关系。
]投料,发生上述反应。图甲表示不同氢碳比时,[CO+CO2]的总平衡转化率随温度变化的关系;图乙表示氢碳比=3时,平衡后体系中C2H5OH、CH3OH的选择性随温度变化的关系。
已知:CH3OH的选择性= ×100%;C2H5OH的选择性=
×100%;C2H5OH的选择性= ×100%
×100%
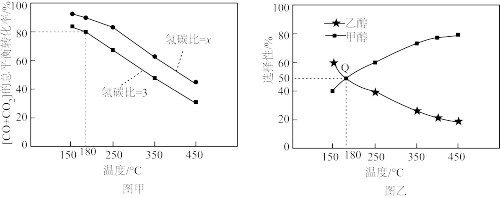
①图甲中x____ 3(填“大于”“小于”或“等于”),其原因是____ 。
②Q点对应的体系中n(CH3OH)=___ mol;此时,H2转化了4mol,则反应2CH3OH(g) C2H5OH(g)+H2O(g)的平衡常数Kp=
C2H5OH(g)+H2O(g)的平衡常数Kp=____ (Kp为以分压表示的平衡常数,分压=总压×物质的量分数,结果保留两位有效数字)。
(4)常温常压下,以Ag为催化剂,在酸性水溶液中将CO2电催化还原为CO的反应历程如图所示:
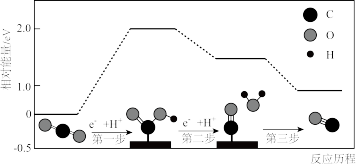
①据图,CO和CO2相比,____ (填化学式)更稳定。
②吸附在催化剂表面上的物种用*标注,图中第一步反应为CO2+e-+H+=*COOH,则第二步反应为____ 。
反应I:CO(g)+2H2(g)
反应II:2CO(g)+4H2(g)
反应III:2CO2(g)+6H2(g)
反应IV:CO2(g)+3H2(g)
反应V:2CH3OH(g)
回答下列问题:
(1)上述反应中,ΔH5=
(2)密闭容器中,上述反应体系在一定条件下建立平衡后,下列描述正确的有
| A.加入催化剂,可提高CO2的平衡转化率 |
| B.降低温度,反应Ⅱ的正反应速率增大,逆反应速率减小 |
| C.增大CO的浓度,反应Ⅲ、IV的平衡均向左移动 |
| D.恒温恒容充入氩气,反应Ⅰ、Ⅱ的平衡不移动 |
已知:CH3OH的选择性=

①图甲中x
②Q点对应的体系中n(CH3OH)=
(4)常温常压下,以Ag为催化剂,在酸性水溶液中将CO2电催化还原为CO的反应历程如图所示:

①据图,CO和CO2相比,
②吸附在催化剂表面上的物种用*标注,图中第一步反应为CO2+e-+H+=*COOH,则第二步反应为
烃(碳氢化合物)在工业生产、生活中有重要用途。
(1)工业由丁烯(C4H8)高温裂解制备丙烯(C3H6)和乙烯(C2H4),其主要反应原理为:
反应I:C4H8(g)
 C3H6(g) ∆H1
C3H6(g) ∆H1
反应II:C4H8(g) 2C2H4(g) ∆H2
2C2H4(g) ∆H2
①已知烃的裂解是吸热反应,则∆H1_______ ∆H2 (填“>”、 “=”或“<”) 。
②若某温度下反应达到平衡时C4H8、 C3H6、 C2H4的体积分数分别为20%、70%、 10%, 平衡时总压强为p,请计算该温度下反应II的平衡常数Kp=_______ (Kp为用气体的分压表示的平衡常数,分压=气体的体积分数×体系总压)
③工业上用丁烯裂解制乙烯时,通常在保持压强不变的情况下,向反应体系充适量水蒸气以提高平衡转化率,其原理是_______ 。
(2)甲烷的转化和利用在天然气化工行业有非常重要的作用。甲烷重整技术主要是利用甲烷和其他原料来制备合成气(CO和H2混合气体)。常见的重整技术有甲烷-水蒸气重整,其反应为:CH4(g)+H2O(g) CO(g) + 3H2(g) ∆H>0;图为反应压强为0.3 MPa,投料比
CO(g) + 3H2(g) ∆H>0;图为反应压强为0.3 MPa,投料比 为1,在三种不同催化剂催化作用下,经过相同反应时间,甲烷—水蒸气重整反应中CH4转化率随温度变化的关系。
为1,在三种不同催化剂催化作用下,经过相同反应时间,甲烷—水蒸气重整反应中CH4转化率随温度变化的关系。
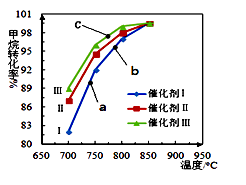
下列说法正确的是_______ 。
A.在相同条件下,三种催化剂I、II、 III的催化效率由高到低的顺序是I> II>III
B.b点CH4的转化率高于a点,原因是b、a两点均未达到平衡状态,b点温度高,反应速率较快,故CH4的转化率较大
C.C点一定未达到平衡状态
D.催化剂只改变反应速率不改变平衡移动,所以在850℃时,不同催化剂(I、II、III)作用下达平衡时CH4的转化率相同
(3)由甲烷制得的合成气(CO和H2),在500 ℃下合成甲醇的反应原理为:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g);在1L的密闭容器中,充入1molCO2和3molH2,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。

①CO2平衡时的体积分数为_______ 。
②下列能说明该反应已达到平衡状态的是_______ 。
A.v正(CH3OH) =3v逆(H2)
B.CO2、H2、CH3OH和H2O浓度之比为1:3:1:1
C.容器内气体的压强不再变化
D.气体的密度不再变化
③500℃、在2个容积都是2L的密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如表:
则乙容器中反应起始向 _______ (填“正反应”或“逆反应”)方向进行, c1_______ (填“>”“<”或“=”)c2。
(1)工业由丁烯(C4H8)高温裂解制备丙烯(C3H6)和乙烯(C2H4),其主要反应原理为:
反应I:C4H8(g)
反应II:C4H8(g)
①已知烃的裂解是吸热反应,则∆H1
②若某温度下反应达到平衡时C4H8、 C3H6、 C2H4的体积分数分别为20%、70%、 10%, 平衡时总压强为p,请计算该温度下反应II的平衡常数Kp=
③工业上用丁烯裂解制乙烯时,通常在保持压强不变的情况下,向反应体系充适量水蒸气以提高平衡转化率,其原理是
(2)甲烷的转化和利用在天然气化工行业有非常重要的作用。甲烷重整技术主要是利用甲烷和其他原料来制备合成气(CO和H2混合气体)。常见的重整技术有甲烷-水蒸气重整,其反应为:CH4(g)+H2O(g)

下列说法正确的是
A.在相同条件下,三种催化剂I、II、 III的催化效率由高到低的顺序是I> II>III
B.b点CH4的转化率高于a点,原因是b、a两点均未达到平衡状态,b点温度高,反应速率较快,故CH4的转化率较大
C.C点一定未达到平衡状态
D.催化剂只改变反应速率不改变平衡移动,所以在850℃时,不同催化剂(I、II、III)作用下达平衡时CH4的转化率相同
(3)由甲烷制得的合成气(CO和H2),在500 ℃下合成甲醇的反应原理为:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g);在1L的密闭容器中,充入1molCO2和3molH2,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。

①CO2平衡时的体积分数为
②下列能说明该反应已达到平衡状态的是
A.v正(CH3OH) =3v逆(H2)
B.CO2、H2、CH3OH和H2O浓度之比为1:3:1:1
C.容器内气体的压强不再变化
D.气体的密度不再变化
③500℃、在2个容积都是2L的密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如表:
| 容器 | 容器甲 | 容器乙 |
| 反应物起始投入量 | 1mol CO2, 3mol H2 | 0.5mol CO2,1mol H2,1molCH3OH,1mol H2O |
| CH3OH的平衡浓度/mol·L-1 | c1 | c2 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网