解答题-原理综合题 适中0.65 引用1 组卷120
2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。回答下列问题:
(1)在一定温度下,向体积固定的密闭容器中加入足量的C(s)和1mol (g),发生下列反应生成水煤气
(g),发生下列反应生成水煤气
I.

II.

①反应I在该温度下能够自发进行的原因为_______ 。
②

_______ 。
③下列说法正确的是_______ 。
A.将炭块粉碎,可加快反应速率
B.平衡时向容器中充入惰性气体,反应I的平衡逆向移动
C.混合气体的密度保持不变时,说明反应体系已达到平衡
D.平衡时 的体积分数可能大于
的体积分数可能大于
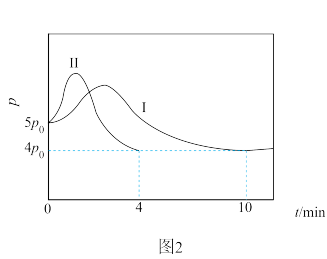
④反应平衡时, (g)的转化率为50%,CO的物质的量为0.1mol,此时反应II的平衡常数
(g)的转化率为50%,CO的物质的量为0.1mol,此时反应II的平衡常数
_______ 。
(2)一种脱除和利用水煤气中 方法的示意图如下:
方法的示意图如下:

①某温度下,吸收塔中 溶液吸收一定量的
溶液吸收一定量的 后,
后, ,则该溶液的pH=
,则该溶液的pH=__ (该温度下 的
的 ,
, )。
)。
②再生塔中产生 的离子方程式为
的离子方程式为_______ 。
③利用电化学原理,将 电催化还原为
电催化还原为 ,阴极上除发生AgCl转化为Ag的反应外,另一个反应式为
,阴极上除发生AgCl转化为Ag的反应外,另一个反应式为_______ 。
(1)在一定温度下,向体积固定的密闭容器中加入足量的C(s)和1mol
I.
II.
①反应I在该温度下能够自发进行的原因为
②
③下列说法正确的是
A.将炭块粉碎,可加快反应速率
B.平衡时向容器中充入惰性气体,反应I的平衡逆向移动
C.混合气体的密度保持不变时,说明反应体系已达到平衡
D.平衡时
④反应平衡时,
(2)一种脱除和利用水煤气中

①某温度下,吸收塔中
②再生塔中产生
③利用电化学原理,将
22-23高三上·江苏扬州·阶段练习
类题推荐
2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。
(1)已知:①H2O(g)= H2O(l) △H= -44 kJ/mol;
②部分物质的燃烧热如下表:
则反应C(s)+H2O(g)= CO(g)+H2(g)的△H =_______ kJ/mol。
(2)在一定温度下,向体积为2 L,的密闭容器中加入足量的C(s)和1 mol H2O(g),起始压强为0.2 MPa时,发生下列反应生成水煤气:
I.C(s)+H2O(g) CO(g)+H2(g) △H1
CO(g)+H2(g) △H1
II.CO(g)+H2O(g) CO2(g)+H2(g)△H2
CO2(g)+H2(g)△H2
①能说明容器中反应已达到平衡的标志是_______ (填字母序号)。
A.容器内气体的平均相对分子质量不变
B.混合气体的密度保持不变
C.v(H2O)消耗=v(H2)生成
D.生成CO和H2的物质的量之比为1:1
②反应10 min时达到平衡,此时,H2O(g)的转化率为50%,CO的物质的量为0.1mol。反应10 min内的平均化学反应速率v(CO2)=_______ ; 此温度下反应I的平衡常数Kp=_______ ( 以分压表示,分压=总压×物质的量分数)。
(3)一种脱除和利用水煤气中CO2方法的示意图如下:
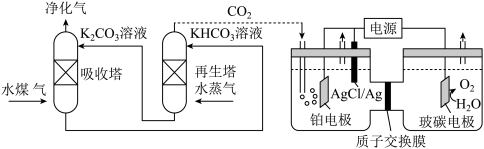
①某温度下,吸收塔中K2CO3溶液吸收一定 量的CO2后, c( ):c (
):c ( )=1:2,则该溶液的pH=
)=1:2,则该溶液的pH=________ ( 该温度下H2CO3的Ka1=4.6×10-7, K。a2=5.0 ×10-11) 。
②利用电化学原理,将CO2电催化还原为C2H4,阳极反应式为________ ,每消耗1 mol CO2转移的电子为_______ mol。
(1)已知:①H2O(g)= H2O(l) △H= -44 kJ/mol;
②部分物质的燃烧热如下表:
| 物质 | C(s) | CO(g) | H2(g) |
| 燃烧热/ (kJ/mol) | -393. 5 | -283. 0 | -285. 8 |
(2)在一定温度下,向体积为2 L,的密闭容器中加入足量的C(s)和1 mol H2O(g),起始压强为0.2 MPa时,发生下列反应生成水煤气:
I.C(s)+H2O(g)
II.CO(g)+H2O(g)
①能说明容器中反应已达到平衡的标志是
A.容器内气体的平均相对分子质量不变
B.混合气体的密度保持不变
C.v(H2O)消耗=v(H2)生成
D.生成CO和H2的物质的量之比为1:1
②反应10 min时达到平衡,此时,H2O(g)的转化率为50%,CO的物质的量为0.1mol。反应10 min内的平均化学反应速率v(CO2)=
(3)一种脱除和利用水煤气中CO2方法的示意图如下:

①某温度下,吸收塔中K2CO3溶液吸收一定 量的CO2后, c(
②利用电化学原理,将CO2电催化还原为C2H4,阳极反应式为
煤的气化是一种重要的制氢途径。生成水煤气的反应如下:
Ⅰ。

Ⅱ。

回答下列问题:
(1) 的
的
___________ 。
(2)恒温恒容下,下列关于反应Ⅱ的说法正确的是___________(填标号)。
(3)在一定温度下,向1L密闭容器中加入足量的C(s)和amol (g)发生反应Ⅰ、Ⅱ,经过tmin达到平衡,
(g)发生反应Ⅰ、Ⅱ,经过tmin达到平衡, (g)的转化率为50%,此时CO的物质的量为bmol。
(g)的转化率为50%,此时CO的物质的量为bmol。
①0~tmin内, 的平均反应速率为
的平均反应速率为___________  ;
;
②反应Ⅱ的平衡常数
___________ 。
(4)一种脱除和利用水煤气中 方法的示意图如下:
方法的示意图如下:
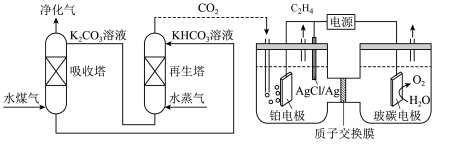
①吸收塔中 溶液的作用是吸收
溶液的作用是吸收 ,反应的离子方程式为
,反应的离子方程式为___________ ;
②阳极反应式为___________ 。
Ⅰ。
Ⅱ。
回答下列问题:
(1)
(2)恒温恒容下,下列关于反应Ⅱ的说法正确的是___________(填标号)。
| A.压强保持不变时,说明该反应已达平衡 |
| B.平衡时向容器中充入惰性气体,平衡不移动 |
| C.混合气体的平均摩尔质量不变时,说明该反应已达平衡 |
| D.平衡时向容器中充入 |
①0~tmin内,
②反应Ⅱ的平衡常数
(4)一种脱除和利用水煤气中

①吸收塔中
②阳极反应式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网