填空题 适中0.65 引用2 组卷662
Ⅰ.现有常温下pH=2的盐酸(甲)和pH=2的醋酸溶液(乙),请根据下列操作回答问题:
(1)常温下 溶液加水稀释过程,下列表达式的数值一定变小的是_______(填字母)。
溶液加水稀释过程,下列表达式的数值一定变小的是_______(填字母)。
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡_______ (填“向左”“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中 的值将
的值将_______ (填“增大”“减小”或“无法确定”)。
(3)相同条件下,取等体积的甲、乙两溶液,分别加水稀释100倍,所得溶液的pH大小关系为pH(甲)_______ pH(乙)(填“>”“<”或“=”)。
Ⅱ.已知次磷酸( )是一元中强酸,请回答下列问题
)是一元中强酸,请回答下列问题
(4)写出其电离方程式:_______ 。
(5)如图所示为二元酸 溶液中各微粒的物质的量分数(
溶液中各微粒的物质的量分数( )随溶液pH的变化曲线(25℃)。
)随溶液pH的变化曲线(25℃)。
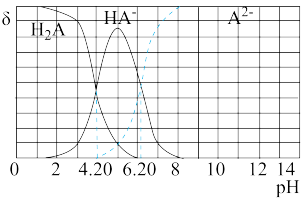
当溶液pH=7时,
_______ 。
(1)常温下
| A. | B. | C. | D. |
(3)相同条件下,取等体积的甲、乙两溶液,分别加水稀释100倍,所得溶液的pH大小关系为pH(甲)
Ⅱ.已知次磷酸(
(4)写出其电离方程式:
(5)如图所示为二元酸

当溶液pH=7时,
22-23高二上·山东烟台·阶段练习
类题推荐
现有常温下pH=2的盐酸甲和pH=2的醋酸溶液乙,请根据下列操作回答问题:
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是________ 。
A. c(H+) B. c(H+)/ c(CH3COOH)
C. c(H+)·c(OH-) D. c(OH-)/ c(H+)
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡______ (填“向左”、“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(CH3COOH)的比值将______ (填“增大”、“减小”或“无法确定”)。
(3)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为:pH(甲)_____ pH(乙)( 填“>”、“<”或“=”)。
(4)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)_________ V(乙)( 填“>”、“<”或“=”)。
(5)已知25℃时,两种酸的电离平衡常数如下:
下列四种离子结合H+能力最强的是______________ 。
A. HCO3- B. CO32- C. ClO- D. CH3COO-
写出下列反应的离子方程式:
CH3COOH+Na2CO3(少量):_________________ ;
HClO+Na2CO3(少量):___________________ 。
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是
A. c(H+) B. c(H+)/ c(CH3COOH)
C. c(H+)·c(OH-) D. c(OH-)/ c(H+)
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡
(3)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为:pH(甲)
(4)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)
(5)已知25℃时,两种酸的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K1 | 1.8×10-5 | 4.3×10-7 | 3.0×10-8 |
| K2 | —— | 5.6×10-11 | —— |
下列四种离子结合H+能力最强的是
A. HCO3- B. CO32- C. ClO- D. CH3COO-
写出下列反应的离子方程式:
CH3COOH+Na2CO3(少量):
HClO+Na2CO3(少量):
分现有常温下c(H+)=0.01mol/L的盐酸甲和c(H+)=0.01mol/L的醋酸溶液乙,回答下列问题:
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据变大的是___________ 。
A.c(H+) B.c(H+)/c(CH3COOH)
C.c(H+)·c(OH-) D.c(OH-)/c(H+)
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡________ (填“向左”、“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(CH3COOH)的比值将 _________________ (填“增大”、“减小”或“无法确定”)。
(3)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为:pH(甲)_________ pH(乙)( 填“>”、“<”或“=”)。
(4)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)____________ V(乙)( 填“>”、“<”或“=”)。
(5)已知25℃时,三种酸的电离平衡常数如下:
下列四种离子结合H+能力最强的是______________ 。
A.HCO B.CO
B.CO C.ClO- D.CH3COO-
C.ClO- D.CH3COO-
请写出在次氯酸钠溶液中通入少量二氧化碳气体的离子方程式:________________ 。
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据变大的是
A.c(H+) B.c(H+)/c(CH3COOH)
C.c(H+)·c(OH-) D.c(OH-)/c(H+)
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡
(3)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为:pH(甲)
(4)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)
(5)已知25℃时,三种酸的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K1 | 1.8×10-5 | 4.3×10-7 | 3.0×10-8 |
| K2 | 5.6×10-11 |
下列四种离子结合H+能力最强的是
A.HCO
请写出在次氯酸钠溶液中通入少量二氧化碳气体的离子方程式:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


