解答题-实验探究题 适中0.65 引用1 组卷154
化学反应过程既是物质的转化过程,也是化学能与热能,电能等其他形式能量的转化过程。请根据要求回答下列与能量转化有关的问题:
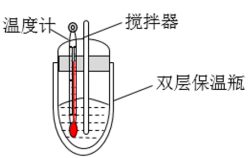
I.利用如图所示装置测定中和热,取 稀硫酸与
稀硫酸与 溶液进行实验,实验数据如表。
溶液进行实验,实验数据如表。
回答下列问题:
(1)若近似认为 稀硫酸与
稀硫酸与 溶液的密度均为
溶液的密度均为 (忽略溶液混合后体积变化),反应所得溶液的比热容
(忽略溶液混合后体积变化),反应所得溶液的比热容 ,则实验测定中和热的数值为
,则实验测定中和热的数值为_______  (保留1位小数)。
(保留1位小数)。
(2)上述实验结果与中和热的标准数值 有偏差,产生偏差的原因不可能是因为_____。
有偏差,产生偏差的原因不可能是因为_____。
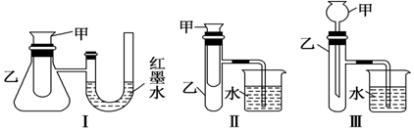
(3)如图三个装置中,不能证明“铁与稀硫酸反应是吸热反应还是放热反应”的是_______ 。
II.
(4)请用下图所示仪器装置设计一个包括:电解饱和食盐水并测定电解时产生的氢气的体积和检验氯气的氧化性的实验装置。
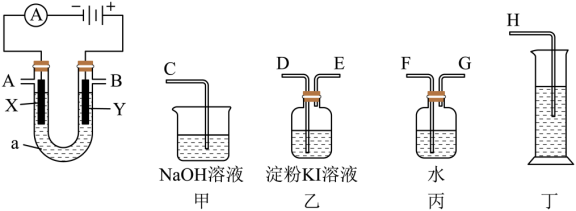
①所选仪器连接时,各接口的顺序是___________ (填各接口的字母代号):
A接______、_____接_____;B接_____、______接______;
②体现氯气的氧化性的实验现象为:_______ ,电解一段时间后,用丁测得气体体积为280mL(标准状况下);需加入_______ g(结果保留一位小数)的_______ 可使溶液复原。
| 温度 实验次数 | 起始温度 | 终止温度 | ||
| 平均值 | ||||
| 1 | 26.2 | 26.0 | 26.1 | 30.2 |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 |
| 4 | 26.4 | 26.2 | 26.3 | 30.3 |

回答下列问题:
(1)若近似认为
(2)上述实验结果与中和热的标准数值
| A.实验装置保温、隔热效果差 |
| B.用量筒量取NaOH溶液的体积时仰视读数 |
| C.分多次把NaOH溶液倒入内筒中 |
| D.测过稀硫酸的温度计未洗净直接用于测定NaOH溶液的温度 |

II.
(4)请用下图所示仪器装置设计一个包括:电解饱和食盐水并测定电解时产生的氢气的体积和检验氯气的氧化性的实验装置。

①所选仪器连接时,各接口的顺序是
A接______、_____接_____;B接_____、______接______;
②体现氯气的氧化性的实验现象为:
22-23高二上·山东德州·阶段练习
类题推荐
根据要求回答下列问题:
Ⅰ.中和热是指在稀溶液中, 与
与 发生中和反应生成
发生中和反应生成 时的反应热。利用如图所示装置测定中和热,取
时的反应热。利用如图所示装置测定中和热,取 稀硫酸与
稀硫酸与 溶液进行实验,实验数据如表。
溶液进行实验,实验数据如表。

回答下列问题:
(1)上述实验中温度变化的平均值为___________  ,若近似认为
,若近似认为 稀硫酸与
稀硫酸与 溶液的密度均为
溶液的密度均为 (忽略溶液混合后体积变化),反应所得溶液的比热容
(忽略溶液混合后体积变化),反应所得溶液的比热容 ,则中和热
,则中和热 的数值为
的数值为___________  (保留1位小数)。
(保留1位小数)。
(2)上述实验结果与中和热数值 有偏差,产生偏差的原因不可能是因为___________ (填标号)。
有偏差,产生偏差的原因不可能是因为___________ (填标号)。
Ⅱ. 在下图所示装置中,试管 、
、 中的电极为多孔的惰性电极,
中的电极为多孔的惰性电极, 、
、 为两个铜夹,夹在被
为两个铜夹,夹在被 溶液浸湿的滤纸条上,滤纸条的中部滴有
溶液浸湿的滤纸条上,滤纸条的中部滴有 液滴;电源有、
液滴;电源有、 两极。若在
两极。若在 、
、 中充满
中充满 溶液后倒立于盛
溶液后倒立于盛 溶液的水槽中,断开
溶液的水槽中,断开 ,闭合
,闭合 、
、 ,通直流电,实验现象如图所示,则:
,通直流电,实验现象如图所示,则:

(3) 是电源的
是电源的___________ 极。
(4)在 溶液浸湿的滤纸条中部的
溶液浸湿的滤纸条中部的 处现象为
处现象为___________ 。写出电极 的电极反应式
的电极反应式___________ 。
(5)断开 、
、 ,闭合
,闭合 ,一段时间后KOH溶液
,一段时间后KOH溶液
___________ (填“变大”“变小”或“不变”)。
Ⅰ.中和热是指在稀溶液中,

| 温度 实验次数 | 起始温度 | 终止温度 | ||
| 平均值 | ||||
| 1 | 26.2 | 26.0 | 26.1 | 30.2 |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 |
| 4 | 26.4 | 26.2 | 26.3 | 30.3 |
(1)上述实验中温度变化的平均值为
(2)上述实验结果与中和热数值
| A.实验装置保温、隔热效果差 |
| B.用量筒量取NaOH溶液的体积时仰视读数 |
| C.分多次把NaOH溶液倒入内筒中 |
| D.测过稀硫酸的温度计未洗净直接用于测定NaOH溶液的温度 |
Ⅱ. 在下图所示装置中,试管

(3)
(4)在
(5)断开
回答下列问题:
(1)实验室用50mL0.50mol/L盐酸与50mL某浓度的NaOH溶液在如图所示装置中反应,通过测定反应过程中所放出的热量来计算中和热。该装置缺少一种仪器,该仪器的名称为________ ;实验室提供了0.50mol/L和0.55mol/L两种浓度的NaOH溶液,应选择_______ mol/L的溶液进行实验。
(2)用50mL0.50mol•L-1盐酸与50mL上述所选浓度的NaOH溶液进行中和热的测定。实验数据如表:
回答下列问题:
①若近似认为稀盐酸与NaOH溶液的密度均为1g•cm-3(忽略溶液混合后体积变化),反应所得溶液的比热容c=4.18J•(g•℃)-1,则中和热△H=_______ kJ•mol-1(保留1位小数)。
②上述实验数值结果与理论值57.3kJ•mol-1有偏差,产生偏差的原因不可能是_______ (填字母序号)。
A.实验装置保温、隔热效果差
B.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
C.用温度计测定盐酸起始温度后直接测定NaOH溶液的温度
D.用量筒量取盐酸的体积时仰视
(3)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L1mol•L-1的稀盐酸恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2、△H3的大小关系为_______ 。
(4)将V1mL1.0mol•L-1盐酸和V2mL未知浓度的NaOH溶液混合均匀后测量并记录温度,实验结果如图所示(实验中始终保持V1+V2=50),通过分析图象可知,做该实验时环境温度_______ (填“高于”“低于”或“等于”)22℃,该NaOH溶液的浓度约为_______ mol•L-1。

(1)实验室用50mL0.50mol/L盐酸与50mL某浓度的NaOH溶液在如图所示装置中反应,通过测定反应过程中所放出的热量来计算中和热。该装置缺少一种仪器,该仪器的名称为

(2)用50mL0.50mol•L-1盐酸与50mL上述所选浓度的NaOH溶液进行中和热的测定。实验数据如表:
| 温度 实验次数 | 起始温度t1/℃ | 终止温度t/℃ | ||
| HCl溶液 | NaOH溶液 | 平均值 | ||
| 1 | 26.0 | 26.2 | 26.1 | 29.4 |
| 2 | 26.0 | 26.4 | 26.2 | 30.5 |
| 3 | 25.9 | 25.9 | 25.9 | 29.3 |
| 4 | 26.2 | 26.4 | 26.3 | 29.5 |
①若近似认为稀盐酸与NaOH溶液的密度均为1g•cm-3(忽略溶液混合后体积变化),反应所得溶液的比热容c=4.18J•(g•℃)-1,则中和热△H=
②上述实验数值结果与理论值57.3kJ•mol-1有偏差,产生偏差的原因不可能是
A.实验装置保温、隔热效果差
B.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
C.用温度计测定盐酸起始温度后直接测定NaOH溶液的温度
D.用量筒量取盐酸的体积时仰视
(3)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L1mol•L-1的稀盐酸恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2、△H3的大小关系为
(4)将V1mL1.0mol•L-1盐酸和V2mL未知浓度的NaOH溶液混合均匀后测量并记录温度,实验结果如图所示(实验中始终保持V1+V2=50),通过分析图象可知,做该实验时环境温度

Ⅰ.中和热的测定:测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
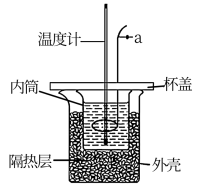
(1)仪器a的名称为___________ ,实验中还需要用到的玻璃仪器是___________ 。
(2)取50mL0.50mol/L NaOH溶液和30mL0.50mol/L稀硫酸进行实验,实验数据如表。
①请填写表中的空白:
②近似认为0.50mol/L NaOH溶液和0.50mol/L稀硫酸的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃)。则中和热ΔH=_____ (保留小数点后一位)。
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因不可能是_____ (填字母序号)。
A.实验装置保温、隔热效果差
B.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
C.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
D.用量筒量取NaOH溶液的体积时仰视读数
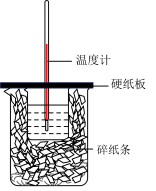
Ⅱ.某同学探究影响硫代硫酸钠溶液与稀硫酸反应速率的因素时,设计如下系列实验:
(3)回答下列问题:
①写出硫代硫酸钠与稀硫酸反应的化学方程式:_____ 。
②该实验①、②可探究___________ 对反应速率的影响,因此V3=___________ ;实验①、③可探究___________ 对反应速率的影响,因此V5=___________ 。

(1)仪器a的名称为
(2)取50mL0.50mol/L NaOH溶液和30mL0.50mol/L稀硫酸进行实验,实验数据如表。
①请填写表中的空白:
| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
| 稀硫酸 | NaOH溶液 | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因不可能是
A.实验装置保温、隔热效果差
B.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
C.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
D.用量筒量取NaOH溶液的体积时仰视读数
Ⅱ.某同学探究影响硫代硫酸钠溶液与稀硫酸反应速率的因素时,设计如下系列实验:
| 实验序号 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
| ③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
①写出硫代硫酸钠与稀硫酸反应的化学方程式:
②该实验①、②可探究
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


