填空题 适中0.65 引用1 组卷409
阅读下面一段材料并回答问题。
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 。
(2)制备 需要在
需要在_______ (填“酸性”、“碱性”或“中性”)环境中进行。
(3)下列关于 的说法中,不正确的是
的说法中,不正确的是_______ 。
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)消毒净化 水,至少需要
水,至少需要 的质量为
的质量为_______ kg。
(5)高铁酸钠 是一种新型的净水剂,可以通过下述反应制取:
是一种新型的净水剂,可以通过下述反应制取:

①该反应中氧化剂是_____ (用化学式表示,下同),____ 元素被氧化,还原产物为____ 。
②用双线桥法在方程式中标出电子转移的情况:_____ 。
(6)将 与水反应的化学方程式补充完整并用双线桥表示出电子转移的方向和数目
与水反应的化学方程式补充完整并用双线桥表示出电子转移的方向和数目____ 。

| 高铁酸钾使用说明书 【化学式】 【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气 【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放5mg …… |
(1)
(2)制备
(3)下列关于
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)消毒净化
(5)高铁酸钠
①该反应中氧化剂是
②用双线桥法在方程式中标出电子转移的情况:
(6)将
22-23高一上·宁夏石嘴山·阶段练习
类题推荐
I.摩擦剂是牙膏的主体成分,SiO2是一种常见的摩擦剂。
(1)Si在元素周期表中的位置是_______ 。
(2)根据用途推测SiO2在水中的溶解性:_______ (填“易溶”或“难溶”)。
(3)制备SiO2的方法如图:
Na2SiO3溶液 H2SiO3沉淀
H2SiO3沉淀 SiO2
SiO2
①写出反应I的离子方程式_______ 。
②比较酸性强弱:H2SO4_______ H2SiO3(填“>”或“<”)。
(4)为满足不同需求,牙膏中还会添加一些特殊物质,如含氟牙膏中添加氟化亚锡(SnF2)。锡的原子结构示意图如图。

下列说法正确的是_______ (填序号)。
a.Sn元素的最高正化合价为+4
b.Sn的原子半径比Si大
c.Sn和Si均可以作半导体材料
II.阅读下面一段材料并回答问题。
高铁酸钾使用说明书
(1)K2FeO4中铁元素的化合价为_______ 。
(2)制备K2FeO4需要在_______ (填“酸性”、“碱性”或“中性”)环境中进行。
(3)下列关于K2FeO4的说法中,不正确 的是_______ 。
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)将K2FeO4与水反应的化学方程式补充完整: 4K2FeO4 + H2O = Fe(OH)3(胶体)+_____ + KOH
______
(5)消毒净化500 m3水,至少需要K2FeO4的质量为_______ kg。
(1)Si在元素周期表中的位置是
(2)根据用途推测SiO2在水中的溶解性:
(3)制备SiO2的方法如图:
Na2SiO3溶液
①写出反应I的离子方程式
②比较酸性强弱:H2SO4
(4)为满足不同需求,牙膏中还会添加一些特殊物质,如含氟牙膏中添加氟化亚锡(SnF2)。锡的原子结构示意图如图。

下列说法正确的是
a.Sn元素的最高正化合价为+4
b.Sn的原子半径比Si大
c.Sn和Si均可以作半导体材料
II.阅读下面一段材料并回答问题。
高铁酸钾使用说明书
| 【化学式】K2FeO4 【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用 【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1 L水投放5 mg K2FeO4即可达到卫生标准 |
(2)制备K2FeO4需要在
(3)下列关于K2FeO4的说法中,
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)将K2FeO4与水反应的化学方程式补充完整: 4K2FeO4 + H2O = Fe(OH)3(胶体)+_____ + KOH
(5)消毒净化500 m3水,至少需要K2FeO4的质量为
回答下列问题:
(1)向沸水中逐滴滴加适量饱和FeCl3溶液,继续加热至液体呈透明的红褐色,形成该分散系的分散质粒子的直径范围是_______ 。利用_______ 效应,证明该分散系。
(2)①56g氮气在标准状况下的体积为_______ ;密度为_______ 。
②3.9gNa2O2中阴、阳离子的个数比为_______ 。
③现有标准状况下CO和CO2混合气体6.72L,其质量为11.6g, 则此混合气体中,CO2和CO的物质的量之比是_______ 。
(3)阅读下列《高铁酸钾使用说明书》,回答问题:
①K2FeO4中铁元素的化合价为_______ 。
②制备K2FeO4需要在_______ (填“酸性”、“碱性”或“中性”)环境中进行。
③下列关于K2FeO4的说法中,不正确的是_______ 。
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快,安全性好、无异味
④将K2FeO4与水反应的化学方程式补充完整:_______ 。
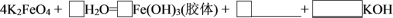
(1)向沸水中逐滴滴加适量饱和FeCl3溶液,继续加热至液体呈透明的红褐色,形成该分散系的分散质粒子的直径范围是
(2)①56g氮气在标准状况下的体积为
②3.9gNa2O2中阴、阳离子的个数比为
③现有标准状况下CO和CO2混合气体6.72L,其质量为11.6g, 则此混合气体中,CO2和CO的物质的量之比是
(3)阅读下列《高铁酸钾使用说明书》,回答问题:
| 高铁酸钾使用说明书 [化学式] K2FeO4 [性状]暗紫色具有金属光泽的粉末,无臭无味 [产品特点]干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用 [用途]主要用于饮用水消毒净化、城市生活污水和工业污水处理 [用量]消毒净化1 L水投放5 mg K2FeO4即可达到卫生标准 |
②制备K2FeO4需要在
③下列关于K2FeO4的说法中,不正确的是
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快,安全性好、无异味
④将K2FeO4与水反应的化学方程式补充完整:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


