填空题 适中0.65 引用1 组卷246
汽车尾气中氮氧化合物、碳氧化合物的处理与利用是各国研究的热点。
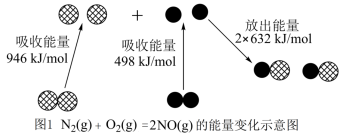
(1)NO生成过程的能量变化如图1所示。该条件下,1molN2和1molO2完全反应生成NO会____ (选填“吸收”或“放出”)____ kJ的能量。
(2)CO与NO在催化剂作用下反应可实现汽车尾气净化:2CO(g)+2NO(g) 2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
①反应进行到10s时,正反应速率____ 逆反应速率(选填“>”“<”或“=”),0~10s内用CO2表示的平均反应速率是____ mol/(L•s)。
②该条件下,NO的最大转化率为____ 。
③下列措施一定能增大该反应速率的是____ (填标号)。
A.及时分离出CO2 B.适当升高温度 C.适当压缩容器的容积 D.充入1molHe
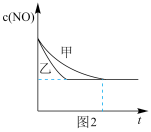
④某同学在其它条件一定的情况下,分别用甲、乙两种催化剂完成该反应,绘出NO浓度随时间变化关系如图2所示,催化剂____ (选填“甲”或“乙”)的催化效果更好。
(3)用电化学气敏传感器测定汽车尾气中CO含量,原理如图3所示,根据燃料电池的原理,推测电极B是该电池的____ 极(选填“正”或“负”),电极A的电极反应为____ 。

(1)NO生成过程的能量变化如图1所示。该条件下,1molN2和1molO2完全反应生成NO会

(2)CO与NO在催化剂作用下反应可实现汽车尾气净化:2CO(g)+2NO(g)
| t/s | 0 | 10 | 20 | 30 | 40 | 50 |
| n(NO)/mol | 0.40 | 0.35 | 0.31 | 0.30 | 0.30 | 0.30 |
①反应进行到10s时,正反应速率
②该条件下,NO的最大转化率为
③下列措施一定能增大该反应速率的是
A.及时分离出CO2 B.适当升高温度 C.适当压缩容器的容积 D.充入1molHe
④某同学在其它条件一定的情况下,分别用甲、乙两种催化剂完成该反应,绘出NO浓度随时间变化关系如图2所示,催化剂

(3)用电化学气敏传感器测定汽车尾气中CO含量,原理如图3所示,根据燃料电池的原理,推测电极B是该电池的

22-23高三上·四川·开学考试
类题推荐
汽车尾气中氮氧化合物、碳氧化合物的处理与利用是各国研究的热点。
(1)已知断裂1molN≡N、H-H、N-H分别需要吸收945kJ、436kJ、391kJ的能量,在一定条件下消耗了1molN2和3molH2生成2molNH3,该过程会________ (填“吸收”或“释放”)_________ kJ的能量。
(2)汽车排气管内安装的催化转化器可处理尾气的主要污染物(NO和CO),发生反应:2NO(g)+2CO(g)⇌2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
①下列能判断该反应达到化学平衡状态的是___________ (填序号)。
A.反应速率v(NO)=v(CO)
B.混合气体的压强不再改变
C.混合气体中NO的物质的量分数保持不变
D.混合气体的密度不再改变
②10s-20s内用N2表示该反应的平均反应速率为___________ 。
③该条件下,CO的最大转化率为___________ 。
④下列措施一定能增大该反应速率的是___________ (填序号)。
A.适当升高温度 B.充入Ne
C.适当减小容器的容积 D.及时分离出CO2、N2
(3)CO2是一种能引起温室效应的气体,有一种室温下“可呼吸”的Na-CO2电池装置可吸收一定量的CO2,装置如图所示,电池的总反应为3CO2+4Na=2Na2CO3+C。
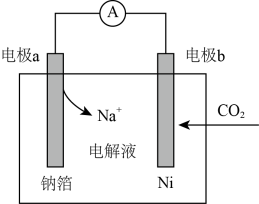
①电极a为___________ 极(填“正”或“负”)。
②电极b发生的电极反应为___________ 。
(1)已知断裂1molN≡N、H-H、N-H分别需要吸收945kJ、436kJ、391kJ的能量,在一定条件下消耗了1molN2和3molH2生成2molNH3,该过程会
(2)汽车排气管内安装的催化转化器可处理尾气的主要污染物(NO和CO),发生反应:2NO(g)+2CO(g)⇌2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
| t/s | 0 | 10 | 20 | 30 | 40 | 50 |
| n(NO)/mol | 0.40 | 0.35 | 0.31 | 0 30 30 | 0.30 | 0.30 |
A.反应速率v(NO)=v(CO)
B.混合气体的压强不再改变
C.混合气体中NO的物质的量分数保持不变
D.混合气体的密度不再改变
②10s-20s内用N2表示该反应的平均反应速率为
③该条件下,CO的最大转化率为
④下列措施一定能增大该反应速率的是
A.适当升高温度 B.充入Ne
C.适当减小容器的容积 D.及时分离出CO2、N2
(3)CO2是一种能引起温室效应的气体,有一种室温下“可呼吸”的Na-CO2电池装置可吸收一定量的CO2,装置如图所示,电池的总反应为3CO2+4Na=2Na2CO3+C。

①电极a为
②电极b发生的电极反应为
回答下列问题:
(1)航天员呼吸产生的CO2利用Bosch反应:CO2(g)+2H2(g) C(s)+2H2O(g) △H,再电解水可实现O2的循环利用。热力学中规定由最稳定单质生成1mol某物质的焓变称为该物质的标准生成焓(符号:△fH
C(s)+2H2O(g) △H,再电解水可实现O2的循环利用。热力学中规定由最稳定单质生成1mol某物质的焓变称为该物质的标准生成焓(符号:△fH ),最稳定单质的标准生成焓规定为0。已知上述反应式中:△fH
),最稳定单质的标准生成焓规定为0。已知上述反应式中:△fH (CO2)=-394kJ•mol-1;△fH
(CO2)=-394kJ•mol-1;△fH (H2)=0kJ•mol-1;△fH
(H2)=0kJ•mol-1;△fH (C)=0kJ•mol-1;△fH
(C)=0kJ•mol-1;△fH (H2O)=-242kJ•mol-1,则△H=
(H2O)=-242kJ•mol-1,则△H=______ kJ•mol-1。
(2)已知:RlnKP=- +C(C为常数),根据上表实验数据得到如图,则该反应的反应热ΔH=
+C(C为常数),根据上表实验数据得到如图,则该反应的反应热ΔH=_____ kJ•mol-1。
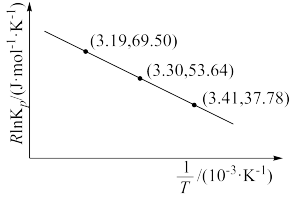
(3)CO与NO在催化剂作用下反应可实现汽车尾气净化:2CO(g)+2NO(g) 2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
①反应进行到10s时,正反应速率_____ 逆反应速率(选填“>”“<”或“=”),0~10s内用CO2表示的平均反应速率是_____ mol/(L•s)。
②该条件下,NO的最大转化率为_____ 。
③下列措施一定能增大该反应速率的是_____ (填标号)。
A.及时分离出CO2 B.适当升高温度 C.适当压缩容器的容积 D.充入1molHe
(4)二氧化氯(ClO2)是一种重要的氧化剂,可用于某些污染物的处理。ClO2可由图1所示装置制备(电极不反应)。
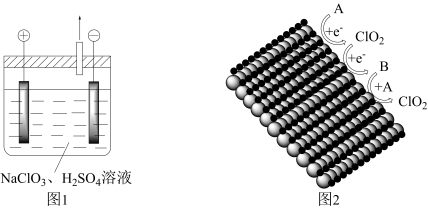
①电解时阳极附近溶液的pH_____ (填“减小”“增大”或“不变”)。
②阴极上产生ClO2的机理如图2所示(A、B均为含氯微粒,其他微粒未标出)。A→ClO2电极反应为_____ 。
(1)航天员呼吸产生的CO2利用Bosch反应:CO2(g)+2H2(g)
(2)已知:RlnKP=-
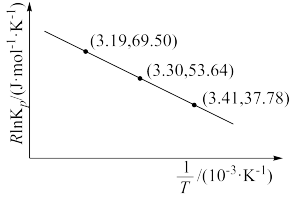
(3)CO与NO在催化剂作用下反应可实现汽车尾气净化:2CO(g)+2NO(g)
| t/s | 0 | 10 | 20 | 30 | 40 | 50 |
| n(NO)/mol | 0.40 | 0.36 | 0.33 | 0.31 | 0.31 | 0.31 |
②该条件下,NO的最大转化率为
③下列措施一定能增大该反应速率的是
A.及时分离出CO2 B.适当升高温度 C.适当压缩容器的容积 D.充入1molHe
(4)二氧化氯(ClO2)是一种重要的氧化剂,可用于某些污染物的处理。ClO2可由图1所示装置制备(电极不反应)。

①电解时阳极附近溶液的pH
②阴极上产生ClO2的机理如图2所示(A、B均为含氯微粒,其他微粒未标出)。A→ClO2电极反应为
汽车尾气中氮氧化合物、碳氧化合物的处理与利用是各国研究的热点。
(1)已知断裂1molN≡N、H-H、N-H分别需要吸收945kJ、436kJ、391kJ的能量,在一定条件下消耗了1molN2和3molH2生成2molNH3,该过程会_______ (填“吸收”或“释放”)_______ kJ的能量。
(2)汽车排气管内安装的催化转化器可处理尾气的主要污染物(NO和CO),发生反应:2NO(g)+2CO(g)⇌2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
①下列能判断该反应达到化学平衡状态的是_______ (填序号)。
A.反应速率v(NO)=v(CO)
B.混合气体的压强不再改变
C.混合气体中NO的物质的量分数保持不变
D.混合气体的密度不再改变
②10s-20s内用N2表示该反应的平均反应速率为_______ 。
③该条件下,CO的最大转化率为_______ 。
(3)直接供氨式碱性燃料电池的电池反应式是4NH3+3O2=2N2+6H2O,电解质溶液一般使用KOH溶液。负极电极反应式是_______ 。
(1)已知断裂1molN≡N、H-H、N-H分别需要吸收945kJ、436kJ、391kJ的能量,在一定条件下消耗了1molN2和3molH2生成2molNH3,该过程会
(2)汽车排气管内安装的催化转化器可处理尾气的主要污染物(NO和CO),发生反应:2NO(g)+2CO(g)⇌2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
| t/s | 0 | 10 | 20 | 30 | 40 | 50 |
| n(NO)/mol | 0.40 | 0.35 | 0.31 | 0 | 0.30 | 0.30 |
A.反应速率v(NO)=v(CO)
B.混合气体的压强不再改变
C.混合气体中NO的物质的量分数保持不变
D.混合气体的密度不再改变
②10s-20s内用N2表示该反应的平均反应速率为
③该条件下,CO的最大转化率为
(3)直接供氨式碱性燃料电池的电池反应式是4NH3+3O2=2N2+6H2O,电解质溶液一般使用KOH溶液。负极电极反应式是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 30
30

