填空题 较易0.85 引用1 组卷223
碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。请回答下列问题:
已知:①CO(g)+2H2(g)=CH3OH(g) ΔH1=-99.0kJ•mol-1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g)=CO(g)+H2O(g) ΔH3=+41.0kJ•mol-1
(1)反应①熵变ΔS____ 0,该反应自发进行的条件是____ (填“低温”“高温”或“任意温度”)。
(2)CH3OH的燃烧热为726kJ•mol-1,计算16g甲醇燃烧放出的热量为____ kJ。
(3)反应CO2(g)+H2(g)=CO(g)+H2O(l)的ΔH____ ΔH3(填“>”“<”“=”)。
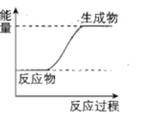
(4)根据盖斯定律计算反应②的ΔH2=____ kJ•mol-1,上述①②③反应中符合如图能量变化的是____ (填序号)。
已知:①CO(g)+2H2(g)=CH3OH(g) ΔH1=-99.0kJ•mol-1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g)=CO(g)+H2O(g) ΔH3=+41.0kJ•mol-1
(1)反应①熵变ΔS
(2)CH3OH的燃烧热为726kJ•mol-1,计算16g甲醇燃烧放出的热量为
(3)反应CO2(g)+H2(g)=CO(g)+H2O(l)的ΔH
(4)根据盖斯定律计算反应②的ΔH2=

21-22高二上·甘肃甘南·期中
类题推荐
化学反应与能量变化密切相关。回答下列问题:
(1)反应物和生成物均为气态的某可逆反应,在不同条件下的反应历程分别为A、B,如图所示。
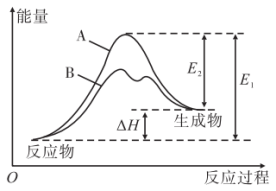
①历程A中正反应的活化能为_____________ (用图中字母表示)。
②B历程表明此反应采用的条件为_____________ (填标号)。
A.升高温度 B.降低温度 C.增大反应物浓度 D.使用催化剂
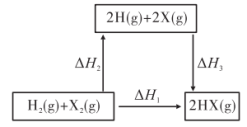
(2)在如图的转化关系中,X代表卤素。△H2_____ 0(填“>”、“=”或“<”);△H1、△H2和△H3三者存在的关系为_____________ 。
(3)甲醇(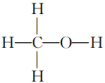 )是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
)是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g) CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
已知反应①中的相关的化学键键能数据如下:
①计算△H1=_________ kJ·mol-1;
②已知△H3=+41.1 kJ·mol-1,则△H2=________ kJ·mol-1。
(1)反应物和生成物均为气态的某可逆反应,在不同条件下的反应历程分别为A、B,如图所示。

①历程A中正反应的活化能为
②B历程表明此反应采用的条件为
A.升高温度 B.降低温度 C.增大反应物浓度 D.使用催化剂
(2)在如图的转化关系中,X代表卤素。△H2

(3)甲醇(
 )是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
)是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:①CO(g)+2H2(g)
②CO2(g)+3H2(g)
③CO2(g)+H2(g)
已知反应①中的相关的化学键键能数据如下:
| 化学键 | H-H | C-O | C O O | H-O | C-H |
| E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
①计算△H1=
②已知△H3=+41.1 kJ·mol-1,则△H2=
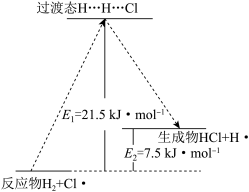
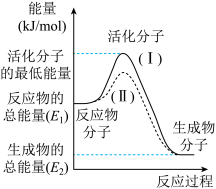
(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察图示,然后回答问题:
①图中所示反应是_____ (填“吸热”或“放热”)反应,该反应的ΔH=____ (用含E1、E2的代数式表示)。
②由上图可知曲线Ⅱ较曲线Ⅰ低,这是由于________ 。
(2)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:①CO(g)+2H2(g) CH3OH(g)ΔH1 ②CO2(g)+3H2(g)
CH3OH(g)ΔH1 ②CO2(g)+3H2(g) CH3OH(g)+H2O(g)ΔH2③CO2(g)+H2(g)
CH3OH(g)+H2O(g)ΔH2③CO2(g)+H2(g) CO(g)+H2O(g)ΔH3。已知反应①中相关的化学键键能数据如下:
CO(g)+H2O(g)ΔH3。已知反应①中相关的化学键键能数据如下:
由此计算ΔH1= _____ kJ·mol-1;已知ΔH2=-58 kJ·mol-1,则ΔH3=___ kJ·mol-1。
①图中所示反应是
②由上图可知曲线Ⅱ较曲线Ⅰ低,这是由于
(2)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:①CO(g)+2H2(g)
| 化学键 | H-H | C-O | H-O | C-H | |
| E/ kJ·mol-1 | 436 | 343 | 1076 | 465 | 413 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网