单选题 适中0.65 引用1 组卷237
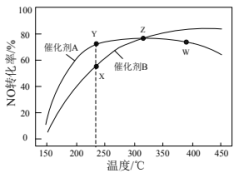
燃煤电厂锅炉尾气中含有氮氧化物(主要成分NO),可通过主反应4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) △H=-1627.7kJ·mol-1除去。温度高于300℃时会发生副反应:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-904.7kJ·mol-1。在恒压、反应物起始物质的量之比一定的条件下,反应相同时间,NO的转化率在不同催化剂作用下随温度变化的曲线如图所示。下列有关说法一定正确的是

| A.N2(g)+O2(g)=2NO(g) △H=-180.7kJ·mol-1 |
| B.图中X点所示条件下,反应时间足够长,NO的转化率能达到Y点的值 |
| C.关于X、Y、Z三点,KX=KY,Z点反应达到化学平衡状态 |
| D.图中Z点到W点NO的转化率降低的原因是主反应的平衡逆向移动 |
21-22高二上·江苏扬州·期中
类题推荐
燃煤电厂锅炉尾气中含有的NO,以氨还原法除去,发生的反应如下:
反应Ⅰ:4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) ΔH=-1627.7 kJ·mol-1
反应II:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH=-904.74 kJ·mol-1
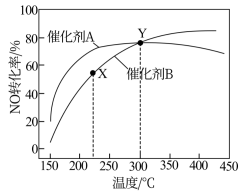
在恒压、反应物起始物质的量之比一定的条件下,反应相同时间,NO的转化率在不同催化剂作用下随温度变化的曲线如图所示。下列说法正确的是
反应Ⅰ:4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) ΔH=-1627.7 kJ·mol-1
反应II:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH=-904.74 kJ·mol-1
在恒压、反应物起始物质的量之比一定的条件下,反应相同时间,NO的转化率在不同催化剂作用下随温度变化的曲线如图所示。下列说法正确的是

| A.其他条件不变,升高温度,NO的平衡转化率一定降低 |
| B.催化剂B条件下,提高X点NO的转化率的方法可以是增大压强或延长反应时间 |
| C.在Y点所示条件下,使用催化剂A或催化剂B,反应均达平衡 |
| D.高效节能除去尾气中的NO,应选择催化剂B |
氨催化氧化是硝酸工业的基础,氨气在 催化剂作用下发生主反应Ⅰ和副反应Ⅱ
催化剂作用下发生主反应Ⅰ和副反应Ⅱ
Ⅰ.4NH3(g)+5O2(g) 4NO(g)+6H2O(g)△H1=-905 kJ•mol-1
4NO(g)+6H2O(g)△H1=-905 kJ•mol-1
Ⅱ.4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H2
2N2(g)+6H2O(g) △H2
(1)已知:
则△H2=___________ 。
(2)以 为催化剂,在
为催化剂,在 密闭容器中充入
密闭容器中充入 和
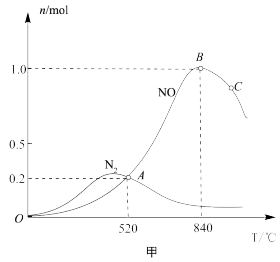
和 ,测得有关物质的量与温度的关系如图甲所示。
,测得有关物质的量与温度的关系如图甲所示。
① 该催化剂在高温时对反应
该催化剂在高温时对反应___________ 更有利(填“Ⅰ”或“Ⅱ”)。
② 时,
时, 的转化率为
的转化率为______ 。
③ 时,反应 Ⅱ的平衡常数
时,反应 Ⅱ的平衡常数
_____ (列出计算式即可)。
④下列说法正确的是___________ (填序号)。
A.工业上氨催化氧化生成 时,最佳温度应控制在
时,最佳温度应控制在 左右
左右
B.增大 和
和 的初始投料比可以提高
的初始投料比可以提高 生成
生成 的平衡转化率
的平衡转化率
C.投料比不变,增加反应物的浓度可以提高 生成
生成 的平衡转化率
的平衡转化率
D.使用催化剂时,可降低反应的活化能,加快其反应速率
(3)在有氧条件下,新型催化剂 能催化
能催化 与
与 反应生成
反应生成 。反应原理为
。反应原理为
①将一定比例的 、
、 与
与 的混合气体,匀速通入装有催化剂
的混合气体,匀速通入装有催化剂 的反应器(如图乙所示)中发生上述反应,反应相同时间
的反应器(如图乙所示)中发生上述反应,反应相同时间 的去除率随反应温度的变化曲线如图丙所示。
的去除率随反应温度的变化曲线如图丙所示。
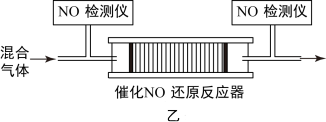
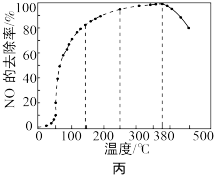
当反应温度高于 时,
时, 的去除率迅速下降的原因可能是
的去除率迅速下降的原因可能是___________ (填序号)。
A. 百分含量减小 B.副反应增多 C.催化剂活性降低 D.反应活化能增大
百分含量减小 B.副反应增多 C.催化剂活性降低 D.反应活化能增大
②已知:上述反应的平衡常数与温度的关系为 。若该反应在某温度下达到平衡,升高温度时,平衡
。若该反应在某温度下达到平衡,升高温度时,平衡___________ (填“正向”“逆向”或“不”)移动,原因是___________  逆反应速率将
逆反应速率将___________ (填“增大”“减小”或“不变”)
Ⅰ.4NH3(g)+5O2(g)
Ⅱ.4NH3(g)+3O2(g)
(1)已知:
| 断裂 | |||
则△H2=
(2)以

①
②
③
④下列说法正确的是
A.工业上氨催化氧化生成
B.增大
C.投料比不变,增加反应物的浓度可以提高
D.使用催化剂时,可降低反应的活化能,加快其反应速率
(3)在有氧条件下,新型催化剂
①将一定比例的
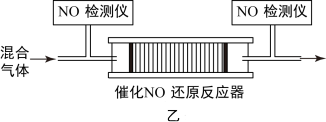

当反应温度高于
A.
②已知:上述反应的平衡常数与温度的关系为
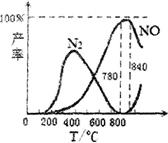
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图。
①4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=﹣905kJ/mol
4NO(g)+6H2O(g) △H=﹣905kJ/mol
②4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H=﹣1268kJ/mol
2N2(g)+6H2O(g) △H=﹣1268kJ/mol
下列说法中不正确的是

①4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H=﹣905kJ/mol
4NO(g)+6H2O(g) △H=﹣905kJ/mol②4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) △H=﹣1268kJ/mol
2N2(g)+6H2O(g) △H=﹣1268kJ/mol下列说法中不正确的是
A.N2(g)+O2(g) 2NO(g) △H=+181.5kJ/mol 2NO(g) △H=+181.5kJ/mol |
| B.加压有利于NH3生成NO,不利于NH3生成N2 |
| C.工业上氨催化氧化生成NO时,温度应控制在780~840℃之间 |
| D.工业上通常提高氧气的浓度,以提高NH3的转化率 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


