解答题-工业流程题 较难0.4 引用17 组卷1387
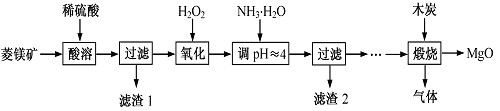
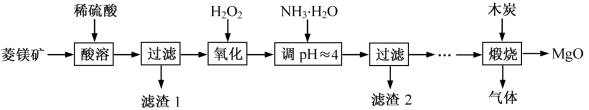
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下:

(1)MgCO3与稀硫酸反应的离子方程式为_________________________ 。
(2)加入H2O2氧化时,发生反应的化学方程式为_________________________ 。
(3)滤渣2 的成分是___________ (填化学式)。
(4)煅烧过程存在以下反应:
2MgSO4+C 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C MgO+S↑+3CO↑
MgO+S↑+3CO↑
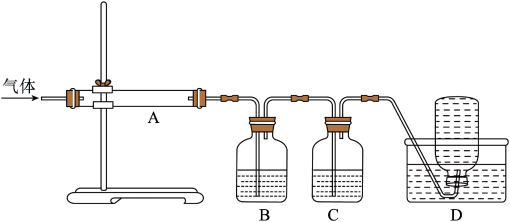
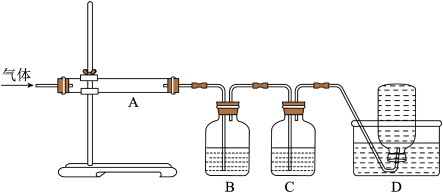
利用下图装置对煅烧产生的气体进行分步吸收或收集。
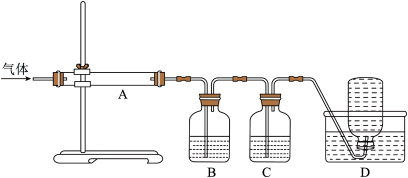
①D中收集的气体可以是__________ (填化学式)。
②B中盛放的溶液可以是__________ (填字母)。
a.NaOH 溶液 b.Na2CO3溶液 c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:_____________________________ 。

(1)MgCO3与稀硫酸反应的离子方程式为
(2)加入H2O2氧化时,发生反应的化学方程式为
(3)滤渣2 的成分是
(4)煅烧过程存在以下反应:
2MgSO4+C
 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑MgSO4+C
 MgO+SO2↑+CO↑
MgO+SO2↑+CO↑ MgSO4+3C
 MgO+S↑+3CO↑
MgO+S↑+3CO↑利用下图装置对煅烧产生的气体进行分步吸收或收集。

①D中收集的气体可以是
②B中盛放的溶液可以是
a.NaOH 溶液 b.Na2CO3溶液 c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:
2013·江苏·高考真题
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网