解答题-原理综合题 适中0.65 引用1 组卷27
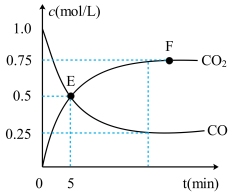
汽车尾气及颗粒物等是造成近年来重度雾霾的原因之一。在汽车排气管中安装催化净化装置可以一定程度上减少对环境的伤害,其反应原理为2CO(g)+2NO(g)⇌N2(g)+2CO2(g) △H=−744kJ/mol。一定温度下,向aL恒容密闭容器中充入2molCO和2molNO模拟汽车尾气的净化,测得CO、CO2的物质的量浓度随时间变化如图所示。
回答下列问题:
(1)写出N2的电子式_______ ,a=_______ 。
(2)0~5min这段时间内用NO表示的平均反应速率为v(NO)=_______ 。
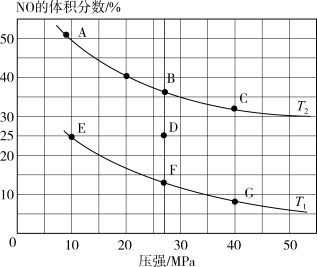
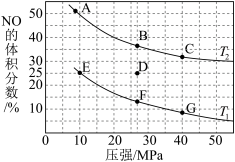
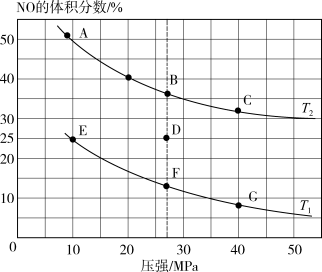
(3)为研究汽车尾气转化为无毒无害物质的有关反应,在密闭容器中充入10molCO和8molNO发生反应,如图所示为平衡时NO的体积分数与温度、压强的关系。回答下列问题:
①该反应达平衡后,为了在提高反应速率同时提高NO的转化率,可采取的措施_______ (填字母代号)。
a.改用高效催化剂 b.升高温度
c.缩小容器的体积 d.增加CO的浓度
②压强为10MPa、温度为T1下,若反应进行到20min达到平衡状态,请计算该温度下平衡常Kp=_______ (保留两位有效数字;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③若在D点对反应容器降温的同时缩小体积至体系压强增大,重新达到的平衡状态可能是图中A~G点中的_______ 点。

回答下列问题:
(1)写出N2的电子式
(2)0~5min这段时间内用NO表示的平均反应速率为v(NO)=
(3)为研究汽车尾气转化为无毒无害物质的有关反应,在密闭容器中充入10molCO和8molNO发生反应,如图所示为平衡时NO的体积分数与温度、压强的关系。回答下列问题:

①该反应达平衡后,为了在提高反应速率同时提高NO的转化率,可采取的措施
a.改用高效催化剂 b.升高温度
c.缩小容器的体积 d.增加CO的浓度
②压强为10MPa、温度为T1下,若反应进行到20min达到平衡状态,请计算该温度下平衡常Kp=
③若在D点对反应容器降温的同时缩小体积至体系压强增大,重新达到的平衡状态可能是图中A~G点中的
21-22高二上·山西长治·阶段练习
类题推荐  是常见的大气污染物,处理
是常见的大气污染物,处理 有助于减少雾霾天气的形成。
有助于减少雾霾天气的形成。
已知:Ⅰ.

Ⅱ.

Ⅲ.

回答下列问题:
(1)
___________  。
。
(2)若在某绝热恒容密闭容器内进行反应Ⅲ,下列图象能表示该反应到达平衡状态的是___________。
(3)T℃时,在容积为2L的密闭容器中,加入2mol NO和2mol CO发生反应Ⅲ,5min后反应达到平衡,测得平衡时体系压强是起始压强的0.8倍。
①
___________ 。
②T℃时,该反应的平衡常数K=___________ ,如果这时向该密闭容器中再充入2mol NO和 ,此时
,此时
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)为研究汽车尾气转化为无毒无害物质的有关反应,在密闭容器中充入10mol CO和8mol NO发生反应,如图所示为平衡时NO的体积分数与温度、压强的关系。
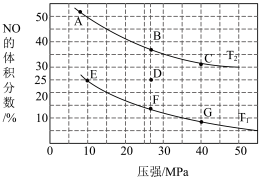
回答下列问题:
①该反应达平衡后,为了在提高反应速率同时提高NO的转化率,可采取的措施___________ (填字母代号)。
a.改用高效催化剂 b.升高温度
c.缩小容器的体积 d.增加CO的浓度
②压强为10MPa、温度为 下,若反应进行到20min达到平衡状态,请计算该温度下平衡常数
下,若反应进行到20min达到平衡状态,请计算该温度下平衡常数
___________ (保留两位有效数字;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③若在D点对反应容器降温的同时缩小体积至体系压强增大,重新达到的平衡状态可能是图中A~G点中的___________ 点。
(5)在某恒容密闭容器中进行反应
 。已知该反应的
。已知该反应的 ,
, (
( 、
、 运分别为正、逆向反应速率常数)。
运分别为正、逆向反应速率常数)。
①加入催化剂,该反应的
___________ (填“增大”“减小”或“不变”)。
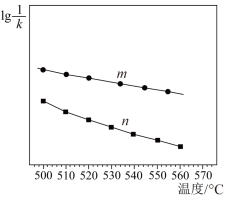
②该反应的 、
、 随温度变化的曲线如图所示,则
随温度变化的曲线如图所示,则___________ 表示 随温度变化的曲线。
随温度变化的曲线。
已知:Ⅰ.
Ⅱ.
Ⅲ.
回答下列问题:
(1)
(2)若在某绝热恒容密闭容器内进行反应Ⅲ,下列图象能表示该反应到达平衡状态的是___________。
A. | B.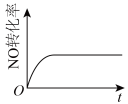 | C. | D.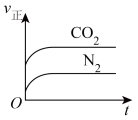 |
(3)T℃时,在容积为2L的密闭容器中,加入2mol NO和2mol CO发生反应Ⅲ,5min后反应达到平衡,测得平衡时体系压强是起始压强的0.8倍。
①
②T℃时,该反应的平衡常数K=
(4)为研究汽车尾气转化为无毒无害物质的有关反应,在密闭容器中充入10mol CO和8mol NO发生反应,如图所示为平衡时NO的体积分数与温度、压强的关系。

回答下列问题:
①该反应达平衡后,为了在提高反应速率同时提高NO的转化率,可采取的措施
a.改用高效催化剂 b.升高温度
c.缩小容器的体积 d.增加CO的浓度
②压强为10MPa、温度为
③若在D点对反应容器降温的同时缩小体积至体系压强增大,重新达到的平衡状态可能是图中A~G点中的
(5)在某恒容密闭容器中进行反应
①加入催化剂,该反应的
②该反应的

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网