填空题 适中0.65 引用1 组卷179
常见晶体的结构分析
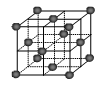
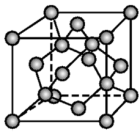
(1)金刚石晶体

①在一个晶胞中,碳原子位于立方体的8个顶点、6个面心以及晶胞内部,由“均摊法”可求出该晶胞中实际含有的碳原子数为_______ ,晶体中碳原子个数与C-C键数之比为_______ 。
②晶体中C-C-C夹角为_______ ,碳原子采取了_______ 杂化。
(2)二氧化硅晶体(如图):
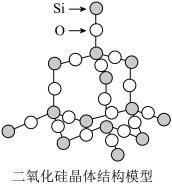
晶体中Si原子与O原子个数比为_______ ,1molSiO2晶体中含Si-O键数目为_______ (用NA表示阿伏加德罗常数)。
(3)Si原子与H原子结合时,Si呈正化合价,则电负性:Si_______ H(选填“<”或“>”)。锗(Ge)与Si是同一主族的元素。Ge元素可能的性质或应用有_______ 。
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.其气态氢化物的稳定性低于硅的气态氢化物
(4)A、B、C、D为四种晶体,依据下列晶体性质推断属于离子晶体的是_______。
(1)金刚石晶体

①在一个晶胞中,碳原子位于立方体的8个顶点、6个面心以及晶胞内部,由“均摊法”可求出该晶胞中实际含有的碳原子数为
②晶体中C-C-C夹角为
(2)二氧化硅晶体(如图):

晶体中Si原子与O原子个数比为
(3)Si原子与H原子结合时,Si呈正化合价,则电负性:Si
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.其气态氢化物的稳定性低于硅的气态氢化物
(4)A、B、C、D为四种晶体,依据下列晶体性质推断属于离子晶体的是_______。
| A.固态时能导电,能溶于盐酸 |
| B.固态时不导电,液态时能导电,可溶于水 |
| C.能溶于苯,不溶于水 |
| D.固态、液态时均不导电,熔点为3500℃ |
21-22高二下·天津宁河·阶段练习
类题推荐
(一)硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问题:
(1)晶体硅和碳化硅熔点较高的是_______ (填化学式);
(2)硅和卤素单质反应可以得到SiX4。SiX4的熔沸点如下表:
①沸点依次升高的原因是_______
②SiCl4与N-甲基咪唑( )反应可以得到M2+,其结构如图所示:
)反应可以得到M2+,其结构如图所示:

N-甲基咪唑分子中碳原子的杂化轨道类型为_______ ,H、C、N的电负性由大到小的顺序为_______ ,1个M2+中含有_______ 个σ键;
(二)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物I可与氧化汞生成化合物Ⅱ。
 (I)
(I)  (Ⅱ)
(Ⅱ) 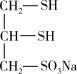 (Ⅲ)
(Ⅲ)  (Ⅳ)
(Ⅳ)
(3)H2S、CH4、H2O的沸点由高到低顺序为_______ 。
(4)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有_______ 。
A.在I中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
(5)化合物AlN是人工合成的半导体材料,它的晶胞结构如图所示,(其中白球所示原子位于立方体的顶点或面心,黑球所示原子位于立方体内)。若AlN的晶胞参数为apm,则晶体的密度为_______ g/cm3(用NA表示阿伏加德罗常数)。

(1)晶体硅和碳化硅熔点较高的是
(2)硅和卤素单质反应可以得到SiX4。SiX4的熔沸点如下表:
| SiF4 | SiCl4 | SiBr4 | SiI4 | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
①沸点依次升高的原因是
②SiCl4与N-甲基咪唑(
 )反应可以得到M2+,其结构如图所示:
)反应可以得到M2+,其结构如图所示:
N-甲基咪唑分子中碳原子的杂化轨道类型为
(二)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物I可与氧化汞生成化合物Ⅱ。
 (I)
(I)  (Ⅱ)
(Ⅱ) 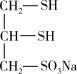 (Ⅲ)
(Ⅲ)  (Ⅳ)
(Ⅳ)(3)H2S、CH4、H2O的沸点由高到低顺序为
(4)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有
A.在I中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
(5)化合物AlN是人工合成的半导体材料,它的晶胞结构如图所示,(其中白球所示原子位于立方体的顶点或面心,黑球所示原子位于立方体内)。若AlN的晶胞参数为apm,则晶体的密度为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网