解答题-原理综合题 较难0.4 引用1 组卷198
乙烷裂解制乙烯具有成本低。收率高、投资少、污染小等优点。目前裂解方法有电催化、光催化裂解、直接裂解、氧气或二氧化碳氧化乙烷裂解等。回答下列问题:
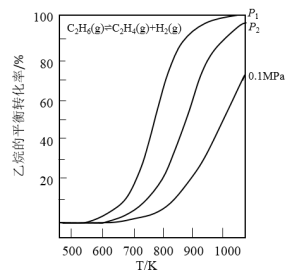
(1)乙烷直接裂解时温度、压强及平衡转化率的关系如图所示:

①反应的ΔH_______ 0,p1______ p2(填“>”、“<”或 “=”)。
②T°C时,将乙烷与氦气的混合气体(乙烷的物质的量分数为m% )通入一密闭容器中发生反应C2H6(g) C2H4(g)+H2(g)。平衡时容器压强为p KPa,此时乙烷的平衡转化率为α,则乙烯的平衡分压为
C2H4(g)+H2(g)。平衡时容器压强为p KPa,此时乙烷的平衡转化率为α,则乙烯的平衡分压为______ KPa,反应的平衡常数Kp=______ KPa(用分压表示,分乐=总压×物质的量分数)。
(2)已知乙烷直接裂解、CO2氧化裂解和O2氧化裂解反应如下:
(I) C2H6(g) C2H4(g)+H2(g) ΔH1
C2H4(g)+H2(g) ΔH1
(II) CO2(g)+C2H6(g) C2H4(g)+CO(g)+H2O(g) ΔH2
C2H4(g)+CO(g)+H2O(g) ΔH2
(III) 2C2H6(g)+O2(g) 2C2H4(g)+2H2O(g) ΔH3
2C2H4(g)+2H2O(g) ΔH3
①反应(I)、(II)的平衡常数分别为K1、K2,则反应CO2(g)+H2(g) CO(g)+H2O(g)的平衡常数为K=
CO(g)+H2O(g)的平衡常数为K=_______ (用含K1、K2的代数式表示)。
②上述反应体系在一定条件下建立平衡后,下列说法正确的有______ 。
A.加入反应(I)的催化剂,可降低反应的焓变
B.恒压掺入Ar能提高反应(II)的平衡产率
C.降低温度,反应(III)的正反应速率降低、逆反应速率增大
D.增加乙烷的浓度,反应(I) (II)(III)的平衡均向右移动
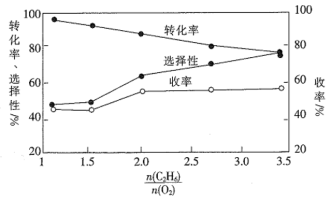
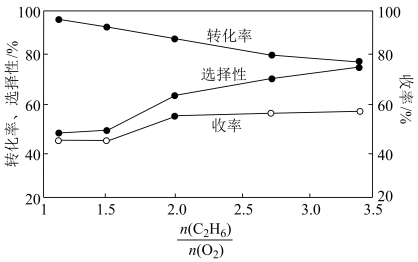
③在800°C时发生反应(III),乙烷的转化率、乙烯的选择性和收率随投料比 的变化关系如图所示,控制
的变化关系如图所示,控制 =2,而不采用选择性更高的
=2,而不采用选择性更高的 =3.5,除可防止积碳外,另一原因是
=3.5,除可防止积碳外,另一原因是_____ ; <2时,
<2时, 越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是
越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是______ 。
(1)乙烷直接裂解时温度、压强及平衡转化率的关系如图所示:

①反应的ΔH
②T°C时,将乙烷与氦气的混合气体(乙烷的物质的量分数为m% )通入一密闭容器中发生反应C2H6(g)
(2)已知乙烷直接裂解、CO2氧化裂解和O2氧化裂解反应如下:
(I) C2H6(g)
(II) CO2(g)+C2H6(g)
(III) 2C2H6(g)+O2(g)
①反应(I)、(II)的平衡常数分别为K1、K2,则反应CO2(g)+H2(g)
②上述反应体系在一定条件下建立平衡后,下列说法正确的有
A.加入反应(I)的催化剂,可降低反应的焓变
B.恒压掺入Ar能提高反应(II)的平衡产率
C.降低温度,反应(III)的正反应速率降低、逆反应速率增大
D.增加乙烷的浓度,反应(I) (II)(III)的平衡均向右移动
③在800°C时发生反应(III),乙烷的转化率、乙烯的选择性和收率随投料比

21-22高三下·广东佛山·阶段练习
类题推荐
乙烯是一种重要的基本化工原料,乙烯的产量可以衡量一个国家的石油化工发展水平,研究工业制取乙烯有重要的意义。
I.工业用H2和CO2在一定条件下合成乙烯:6H2(g)+2CO2(g) CH2=CH2(g)+4H2O(g) ΔH1
CH2=CH2(g)+4H2O(g) ΔH1
已知:①2H2(g)+O2(g)=2H2O(1) ΔH2=-571.4kJ·mol-1
②CH2=CH2(g)+3O2(g)→2CO2(g)+2H2O(1) ΔH3=-1411kJ·mol-1
③H2O(g)=H2O(1) ΔH4=-44kJ·mol-1
(1)ΔH1=_______
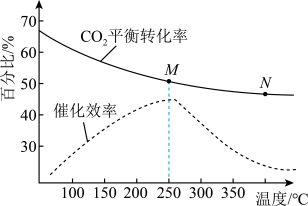
(2)在恒容密闭容器中充入体积比为3:1的H2和CO2,不同温度对CO2的平衡转化率和催化剂催化效率的影响如图所示,下列说法正确的是_______(不定项选择)。
II.工业用甲烷催化法制取乙烯:2CH4(g) C2H4(g)+2H2(g) ΔH>0,T℃时,向4L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
C2H4(g)+2H2(g) ΔH>0,T℃时,向4L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
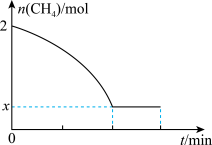
(3)实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2),k正、k逆为速率常数,只与温度有关,T℃时k正与k逆的比值为____ (用含x的代数式表示);若将温度升高,速率常数增大的倍数:k正_____ (填“>”“=”或“<”)k逆。
III.乙烷裂解制乙烯:C2H6(g) C2H4(g)+H2(g)。
C2H4(g)+H2(g)。
(4)T℃时,将乙烷与氦气体积比2:1混合后,通入一恒压容器中发生反应。平衡时容器压强为P Pa,若乙烷的平衡转化率为50%,反应的平衡常数Kp=_____ (用分压表示,分压=总压×物质的量分数)。
I.工业用H2和CO2在一定条件下合成乙烯:6H2(g)+2CO2(g)
已知:①2H2(g)+O2(g)=2H2O(1) ΔH2=-571.4kJ·mol-1
②CH2=CH2(g)+3O2(g)→2CO2(g)+2H2O(1) ΔH3=-1411kJ·mol-1
③H2O(g)=H2O(1) ΔH4=-44kJ·mol-1
(1)ΔH1=
(2)在恒容密闭容器中充入体积比为3:1的H2和CO2,不同温度对CO2的平衡转化率和催化剂催化效率的影响如图所示,下列说法正确的是_______(不定项选择)。

| A.为了提高乙烯的产率应尽可能选择低温 |
| B.生成乙烯的速率:v(M)可能小于v(N) |
| C.平衡常数:KM<KN |
| D.M点时的压强一定小于N点时的压强 |
II.工业用甲烷催化法制取乙烯:2CH4(g)

(3)实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2),k正、k逆为速率常数,只与温度有关,T℃时k正与k逆的比值为
III.乙烷裂解制乙烯:C2H6(g)
(4)T℃时,将乙烷与氦气体积比2:1混合后,通入一恒压容器中发生反应。平衡时容器压强为P Pa,若乙烷的平衡转化率为50%,反应的平衡常数Kp=
乙烯是一种重要的基本化工原料,乙烯的产量可以衡量一个国家的石油化工发展水平,研究工业制取乙烯有重要的意义。
I.工业用H2和CO2在一定条件下合成乙烯:6H2(g)+2CO2(g) CH2=CH2(g)+4H2O(g) ΔH1
CH2=CH2(g)+4H2O(g) ΔH1
已知:①2H2(g)+O2(g)=2H2O(1) ΔH2=-571.4kJ·mol-1
②CH2=CH2(g)+3O2(g)→2CO2(g)+2H2O(1) ΔH3=-1411kJ·mol-1
③H2O(g)=H2O(1) ΔH4=-44kJ·mol-1
(1)ΔH1=_______
(2)在密闭容器中充入体积比为3:1的H2和CO2,不同温度对CO2的平衡转化率和催化剂催化效率的影响如图所示,下列说法正确的是_______。
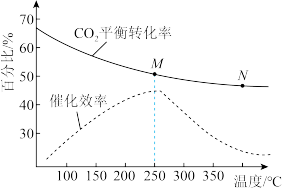
II.工业用甲烷催化法制取乙烯:2CH4(g)=C2H4(g)+2H2(g) ΔH>0,T℃时,向4L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:

(3)实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2),k正、k逆为速率常数,只与温度有关,T℃时k正与k逆的比值为_______ (用含x的代数式表示);若将温度升高,速率常数增大的倍数:k正_______ (填“>”“=”或“<”)k逆。
III.乙烷裂解制乙烯:C2H6(g) C2H4(g)+H2(g)。
C2H4(g)+H2(g)。
(4)T℃时,将乙烷与氦气体积比2:1混合后,通入一密闭容器中发生反应。平衡时容器压强为P0Pa,若乙烷的平衡转化率为50%,反应的平衡常数Kp=_____ (用分压表示,分压=总压×物质的量分数)。
IV.电化学法还原二氧化碳制乙烯原理如下图所示。

(5)阴极电极反应式为:_______ ,电路中转移0.6mol电子,两极共收集气体_______ L(标准状况)。
I.工业用H2和CO2在一定条件下合成乙烯:6H2(g)+2CO2(g)
已知:①2H2(g)+O2(g)=2H2O(1) ΔH2=-571.4kJ·mol-1
②CH2=CH2(g)+3O2(g)→2CO2(g)+2H2O(1) ΔH3=-1411kJ·mol-1
③H2O(g)=H2O(1) ΔH4=-44kJ·mol-1
(1)ΔH1=
(2)在密闭容器中充入体积比为3:1的H2和CO2,不同温度对CO2的平衡转化率和催化剂催化效率的影响如图所示,下列说法正确的是_______。

| A.为了提高乙烯的产率应尽可能选择低温 |
| B.生成乙烯的速率:v(M)可能小于v(N) |
| C.平衡常数:KM<KN |
| D.M点时的压强一定小于N点时的压强 |
II.工业用甲烷催化法制取乙烯:2CH4(g)=C2H4(g)+2H2(g) ΔH>0,T℃时,向4L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:

(3)实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2),k正、k逆为速率常数,只与温度有关,T℃时k正与k逆的比值为
III.乙烷裂解制乙烯:C2H6(g)
(4)T℃时,将乙烷与氦气体积比2:1混合后,通入一密闭容器中发生反应。平衡时容器压强为P0Pa,若乙烷的平衡转化率为50%,反应的平衡常数Kp=
IV.电化学法还原二氧化碳制乙烯原理如下图所示。

(5)阴极电极反应式为:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网