解答题-实验探究题 较易0.85 引用1 组卷141
海洋中蕴含丰富的资源。
Ⅰ.利用海水提取淡水、溴、镁和碘的部分过程如图所示:
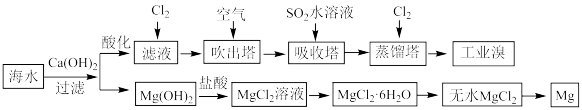
(1)海水中部分离子的含量如下:
其中,Mg2+的物质的量浓度是_______ mol/L。海水淡化的方法有_______ 、离子交换法和电渗析法等。
(2)提取溴元素时,热空气吹出并用SO2水溶液吸收的目的是_______ ,然后再通入Cl2。
(3)若要提取1mol溴,理论上至少需要标准状况下Cl2的体积为_______ L(忽略Cl2的溶解)。
(4)由无水MgCl2制取Mg的化学方程式为_______ 。
Ⅱ.海带中含有丰富的碘元素。从海带中提取碘单质的工业生产流程如图所示:
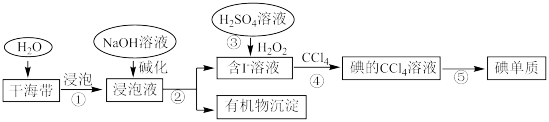
(5)步骤②的操作是_______ 。
(6)步骤③反应的离子方程式有 和
和_______ 。
(7)步骤④还可以选用的试剂是_______填字母序号)
Ⅰ.利用海水提取淡水、溴、镁和碘的部分过程如图所示:

(1)海水中部分离子的含量如下:
| 成分 | 含量(mg/L) | 成分 | 含量(mg/L) |
| Na+ | 10560 | Cl- | 18980 |
| Mg2+ | 1272 | Br- | 64 |
| Ca2+ | 400 | SO | 2560 |
(2)提取溴元素时,热空气吹出并用SO2水溶液吸收的目的是
(3)若要提取1mol溴,理论上至少需要标准状况下Cl2的体积为
(4)由无水MgCl2制取Mg的化学方程式为
Ⅱ.海带中含有丰富的碘元素。从海带中提取碘单质的工业生产流程如图所示:

(5)步骤②的操作是
(6)步骤③反应的离子方程式有
(7)步骤④还可以选用的试剂是_______填字母序号)
| A.苯 | B.乙醇 | C.己烷 | D.乙酸 |
22-23高二上·四川绵阳·开学考试
类题推荐
海洋中蕴含着丰富的资源。利用海水提取淡水、溴和镁的部分过程如图所示。

(1)海水淡化的方法有_________________ 、离子交换法和电渗析法等。
(2)用纯碱吸收浓缩海水吹出的Br2: 3Br2+ 6Na2CO3+3H2O=5NaBr+ NaBrO3+6NaHCO3。若吸收3 mol Br2时,转移的电子是_________________ mol。
(3)海水中部分离子的含量如下:
其中,Mg2+的物质的量浓度是____________ mol/L。若从100 L的海水中提取镁,理论上加入沉淀剂Ca(OH)2的质量是_______________ g。
(4)由Mg(OH)2得到单质Mg,以下方法最合适的是________________ (填序号)。
A. Mg(OH)2 MgO
MgO Mg
Mg
B. Mg(OH)2 MgO
MgO Mg
Mg
C. Mg(OH)2 无水MgCl2
无水MgCl2 Mg
Mg
D. Mg(OH)2 MgCl2溶液
MgCl2溶液 Mg
Mg

(1)海水淡化的方法有
(2)用纯碱吸收浓缩海水吹出的Br2: 3Br2+ 6Na2CO3+3H2O=5NaBr+ NaBrO3+6NaHCO3。若吸收3 mol Br2时,转移的电子是
(3)海水中部分离子的含量如下:
| 成分 | 含量( mg/L) | 成分 | 含量( mg/L) |
| Na+ | 10560 | Cl- | 18980 |
| Mg2+ | 1272 | Br- | 64 |
| Ca2+ | 400 | SO42- | 2560 |
其中,Mg2+的物质的量浓度是
(4)由Mg(OH)2得到单质Mg,以下方法最合适的是
A. Mg(OH)2
B. Mg(OH)2
C. Mg(OH)2
D. Mg(OH)2
海洋中蕴含丰富的资源,利用海水提取淡水、溴、镁和碘的部分过程如图所示:

(1)海水中部分离子的含量如下:
其中,Mg2+的物质的量浓度是________ mol·L-1。
(2)滤液中通入Cl2后发生反应的离子方程式为________ 。
(3)提取溴元素时,热空气吹出并用SO2水溶液吸收的目的是________ (用离子方程式表示)。
(4)若要提取1mol溴,理论上至少需要标准状况下Cl2的体积为________ L(忽略Cl2的溶解)。
(5)由无水MgCl2制取Mg的化学方程式为________ 。

(1)海水中部分离子的含量如下:
| 成分 | 含量(mg/L) | 成分 | 含量(mg/L) |
| Na+ | 10560 | Cl- | 18980 |
| Mg2+ | 1272 | Br- | 64 |
| Ca2+ | 400 | SO | 2560 |
(2)滤液中通入Cl2后发生反应的离子方程式为
(3)提取溴元素时,热空气吹出并用SO2水溶液吸收的目的是
(4)若要提取1mol溴,理论上至少需要标准状况下Cl2的体积为
(5)由无水MgCl2制取Mg的化学方程式为
海洋中蕴含着丰富的资源。利用海水提取淡水、溴和镁的部分过程如图所示。

(1)海水淡化的方法有_________________ 、离子交换法和电渗析法等。
(2)用纯碱吸收浓缩海水吹出的Br2:
3Br2+ 6Na2CO3+3H2O= 5NaBr+ NaBrO3+6NaHCO3。当吸收3 mol Br2时,反应中转移的电子数是_____________ 。
(3)海水中部分离子的含量如下:
其中,Mg2+的物质的量浓度是____________ 。若要从100 L的海水中提取镁,理论上需要加入沉淀剂Ca(OH)2的质量是_______________ 。
(4)由Mg(OH)2制单质Mg,以下方法最合适的是________________ (填序号)。
A.Mg(OH)2 MgO
MgO Mg
Mg
B.Mg(OH)2 MgO
MgO Mg
Mg
C.Mg(OH)2 无水MgCl2
无水MgCl2 Mg
Mg
D.Mg(OH)2 MgCl2溶液
MgCl2溶液 Mg
Mg

(1)海水淡化的方法有
(2)用纯碱吸收浓缩海水吹出的Br2:
3Br2+ 6Na2CO3+3H2O= 5NaBr+ NaBrO3+6NaHCO3。当吸收3 mol Br2时,反应中转移的电子数是
(3)海水中部分离子的含量如下:
| 成分 | 含量( mg/L) | 成分 | 含量( mg/L) |
| Na+ | 10560 | Cl- | 18980 |
| Mg2+ | 1272 | Br- | 64 |
| Ca2+ | 400 | SO42- | 2560 |
(4)由Mg(OH)2制单质Mg,以下方法最合适的是
A.Mg(OH)2
B.Mg(OH)2
C.Mg(OH)2
D.Mg(OH)2
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


