填空题 适中0.65 引用4 组卷163
酸性锌锰干电池是一种常用的一次电池,其结构如图所示。该电池在放电过程产生MnOOH和Zn(NH3)2Cl2。回答下列问题:
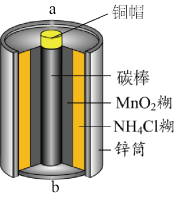
(1)该电池的正极为____ (填“a”或“b”)极,该电池总反应的化学方程式为____ 。
(2)如图为电解100mL2.0mol·L-1CuSO4溶液的装置,该装置的电源为上述酸性锌锰干电池。
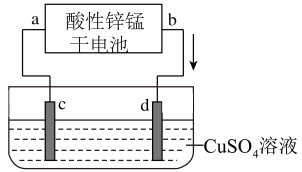
①电解一段时间后,石墨电极d出现的现象为____ ;石墨电极c上的电极反应式为____ 。
②当上述电池消耗3.25gZn时,电解后溶液中c(H+)为_____ (忽略电解前后溶液体积变化)。欲将电解后的溶液恢复至原溶液,应加入的试剂是____ ,其质量为____ g。

(1)该电池的正极为
(2)如图为电解100mL2.0mol·L-1CuSO4溶液的装置,该装置的电源为上述酸性锌锰干电池。

①电解一段时间后,石墨电极d出现的现象为
②当上述电池消耗3.25gZn时,电解后溶液中c(H+)为
22-23高三上·河北保定·阶段练习
类题推荐
酸性锌锰干电池是一种一次电池,其结构如图所示。该电池在放电过程产生MnOOH和Zn(NH3)2Cl2。回答下列问题:

(1)电池反应的化学方程式为____ 。
(2)如图为电解500mL1mol/LCuSO4溶液的装置,该装置的电源为上述酸性锌锰干电池。当电池负极消耗16.25gZn时,电解后溶液的pH=____ (忽略电解前后溶液体积变化)。将电解后的溶液恢复至原溶液时,应加入的试剂是____ ,其质量为____ 。

(3)用该废电池的锌皮(含少量杂质铁)可制备化工原料ZnSO4•7H2O。其流程如图:

已知部分物质的Ksp如表:
①氧化时的离子方程式____ 。
②试剂X最好选用____ (填化学式),调pH的范围是____ (假定Zn2+浓度为0.1mol/L,离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全)。
③若上述流程中不加H2O2氧化的后果是____ ,原因是____ 。

(1)电池反应的化学方程式为
(2)如图为电解500mL1mol/LCuSO4溶液的装置,该装置的电源为上述酸性锌锰干电池。当电池负极消耗16.25gZn时,电解后溶液的pH=

(3)用该废电池的锌皮(含少量杂质铁)可制备化工原料ZnSO4•7H2O。其流程如图:

已知部分物质的Ksp如表:
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
②试剂X最好选用
③若上述流程中不加H2O2氧化的后果是
A、B、C三种强电解质,它们在水中电离出的离子的离子如下表所示:
在如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、B、C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了16.0 g。常温下各烧杯中溶液的pH与电解时间t的关系如图所示。据此回答下列问题:
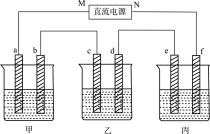
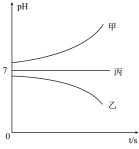
(1)b电极上的电极反应式为:_____ ;
(2)计算电极e上生成的气体在标况下的体积为_____ ;
(3)写出乙烧杯中的电解反应方程式:_____ ;
(4)要使丙烧杯中的C溶液恢复到原来的浓度,需要向丙烧杯中加入____ (填加入物质的名称和质量)。
(5)酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物,该电池放电产生的MnOOH。电池反应的离子方程式为:____ ;维持电流强度为0.5A,电池工作5min,理论上消耗锌_____ g(已知F=96500C·mol-1)。
阳离子 | Na+、K+、Cu2+、 |
阴离子 |
|


(1)b电极上的电极反应式为:
(2)计算电极e上生成的气体在标况下的体积为
(3)写出乙烧杯中的电解反应方程式:
(4)要使丙烧杯中的C溶液恢复到原来的浓度,需要向丙烧杯中加入
(5)酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物,该电池放电产生的MnOOH。电池反应的离子方程式为:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



