解答题-实验探究题 适中0.65 引用1 组卷202
席夫碱在有机合成、液晶材料、植物生长调节等多个领域有重要用途。学习小组在实验室中探究由对甲基苯胺(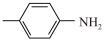 )与苯甲醛(
)与苯甲醛(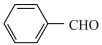 )在酸催化下制备对甲基苯胺缩苯甲醛席夫碱(
)在酸催化下制备对甲基苯胺缩苯甲醛席夫碱(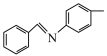 ,M
,M,有关信息和装置如表。
| 物质 | 相对分子质量 | 密度/(gcm-3) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 对甲基苯胺 | 107 | 0.96 | 44 | 200 | 微溶于水,易溶于乙醇 |
| 乙醇 | 46 | 0.78 | -114 | 78 | 溶于水 |
| 苯甲醛 | 106 | 1.0 | -26 | 179 | 微溶于水,与乙醇互溶 |
(1)实验步骤:
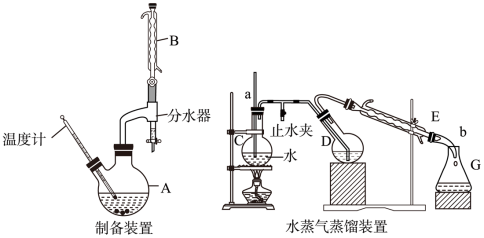
①按图安装好制备装置,检验装置的气密性。向A中加入6.0g对甲基苯胺、5.0mL苯甲醛、50mL乙醇和适量乙酸。其中分水器可接收并分离生成的水。乙醇的作用为
②控制反应温度为50℃,加热回流至反应结束。合适的加热方式为
(2)纯化产品:
①按图安装好水蒸气蒸馏装置,检验装置的气密性。将A中反应后余液转移至D中,在C中加入适量水,进行蒸馏,将产品中的乙醇、对甲基苯胺和苯甲醛蒸出。管a的作用为
②蒸馏操作结束后,需先打开止水夹再停止加热的原因为
③实验后将D中固体洗涤、干燥后,进一步通过
21-22高二上·广东深圳·期末
类题推荐
回答下列问题:
(1)利用如图装置制备对甲基苯胺缩苯甲醛席夫碱:向A中加入5.8g对甲基苯胺固体,4.6mL苯甲醛、50mL乙醇和适量乙酸,控制pH≈4.5,反应温度为50℃。分水器可接收并分离生成的水。___________ 。
②乙醇的作用是___________ ,A中发生反应的化学方程式为___________ 。
③为了得到较高的产品产率,需要通过水浴加热控制反应温度,水浴加热的优点是___________ ,判断反应结束的现象是___________ 。
(2)利用如图提纯产品:将A中反应后溶液转移至D中,在C中加入适量水,进行水蒸气蒸馏。___________ 。
②蒸馏结束后,为了防止D中液体倒吸进入C中,需进行的操作是___________ ,然后停止加热。
③蒸馏结束后,对D中的粗产品进行洗涤、干燥,再通过重结晶提纯后,得到纯产品5.5g。本实验的产品产率为___________ (保留三位有效数字)。
席夫碱主要是指含有亚胺或甲亚胺特性基团()的一类有机化合物,它在医学、催化、分析化学、腐蚀以及光致变色领域有重要应用。某化学兴趣研究小组利用对甲基苯胺(
 ,高热可燃)与苯甲醛(
,高热可燃)与苯甲醛( )在乙酸催化下制备对甲基苯胺缩苯甲醛席夫碱(
)在乙酸催化下制备对甲基苯胺缩苯甲醛席夫碱( ,
,),相关信息如表所示。
| 物质 | 分子式 | 相对分子质量 | 密度/( | 沸点/℃ | 溶解性 |
| 对甲基苯胺 | 107 | 0.96 | 200 | 微溶于水,溶于乙醇 | |
| 乙醇 | 46 | 0.78 | 78 | 溶于水 | |
| 苯甲醛 | 106 | 1.0 | 179 | 微溶于水,与乙醇互溶 |
(1)利用如图装置制备对甲基苯胺缩苯甲醛席夫碱:向A中加入5.8g对甲基苯胺固体,4.6mL苯甲醛、50mL乙醇和适量乙酸,控制pH≈4.5,反应温度为50℃。分水器可接收并分离生成的水。

②乙醇的作用是
③为了得到较高的产品产率,需要通过水浴加热控制反应温度,水浴加热的优点是
(2)利用如图提纯产品:将A中反应后溶液转移至D中,在C中加入适量水,进行水蒸气蒸馏。

②蒸馏结束后,为了防止D中液体倒吸进入C中,需进行的操作是
③蒸馏结束后,对D中的粗产品进行洗涤、干燥,再通过重结晶提纯后,得到纯产品5.5g。本实验的产品产率为
苯甲醛( )是一种重要的化工原料,某小组同学利用如图所示实验装置(夹持装置略去)由苯甲醇(
)是一种重要的化工原料,某小组同学利用如图所示实验装置(夹持装置略去)由苯甲醇( )制备苯甲醛。已知有机物的相关数据如表所示:
)制备苯甲醛。已知有机物的相关数据如表所示:
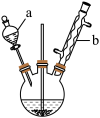
实验步骤:
①向容积为500mL的三颈烧瓶中加入90.0mL质量分数为5%的次氯酸钠溶液(稍过量),调节溶液的pH为9~10后,加入3.0mL苯甲醇、75.0mL二氯甲烷,不断搅拌。
②充分反应后,用二氯甲烷萃取水相3次,并将有机相合并。
③向所得有机相中加入无水硫酸镁,过滤,得到有机混合物。
④蒸馏有机混合物,得到2.08g苯甲醛产品。请回答下列问题:
(1)仪器b的名称为______ ,搅拌器的作用是______ 。
(2)苯甲醇与NaClO反应的化学方程式为_______ 。
(3)步骤①(向容积为500mL的三唝烧瓶中加入90.0mL;质量分数为5%的次氯酸钠溶液(稍过量),调节溶液的pH为9~10后,加入3.0mL苯甲醇、75.0mL二氯甲烷,不断搅拌)中,投料时,次氯酸钠不能过量太多,原因是______ ;步骤③(向所得有机相中加入无水硫酸镁,过滤,得到有机混合物)中加入无水硫酸镁,若省略该操作,可能造成的后果是______ 。
(4)步骤②(充分反应后,用二氯甲烷萃取水相3次,并将有机相合并)中,应选用的实验装置是______ (填序号),该操作中分离出有机相的操作名称是_______ 。
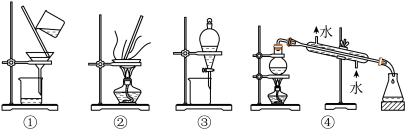
(5)步骤④(蒸馏有机混合物,得到2.08g苯甲醛产品)中,蒸馏温度应控制在______ 左右。
(6)本实验中,苯甲醛的产率为______ (保留三位有效数字)。
 )是一种重要的化工原料,某小组同学利用如图所示实验装置(夹持装置略去)由苯甲醇(
)是一种重要的化工原料,某小组同学利用如图所示实验装置(夹持装置略去)由苯甲醇( )制备苯甲醛。已知有机物的相关数据如表所示:
)制备苯甲醛。已知有机物的相关数据如表所示:
| 有机物 | 沸点(℃) | 密度(g•cm-3) | 相对分子质量 | 溶解性 |
| 苯甲醛 | 178.1 | 1.04 | 106 | 微溶于水,易溶于乙醇、醚和卤代烃 |
| 苯甲醇 | 205.7 | 1.04 | 108 | 微溶于水,易溶于乙醇、醚和卤代烃 |
| 二氯甲烷 | 39.8 | 1.33 | 85 | 难溶于水,易溶于有机溶剂 |
①向容积为500mL的三颈烧瓶中加入90.0mL质量分数为5%的次氯酸钠溶液(稍过量),调节溶液的pH为9~10后,加入3.0mL苯甲醇、75.0mL二氯甲烷,不断搅拌。
②充分反应后,用二氯甲烷萃取水相3次,并将有机相合并。
③向所得有机相中加入无水硫酸镁,过滤,得到有机混合物。
④蒸馏有机混合物,得到2.08g苯甲醛产品。请回答下列问题:
(1)仪器b的名称为
(2)苯甲醇与NaClO反应的化学方程式为
(3)步骤①(向容积为500mL的三唝烧瓶中加入90.0mL;质量分数为5%的次氯酸钠溶液(稍过量),调节溶液的pH为9~10后,加入3.0mL苯甲醇、75.0mL二氯甲烷,不断搅拌)中,投料时,次氯酸钠不能过量太多,原因是
(4)步骤②(充分反应后,用二氯甲烷萃取水相3次,并将有机相合并)中,应选用的实验装置是

(5)步骤④(蒸馏有机混合物,得到2.08g苯甲醛产品)中,蒸馏温度应控制在
(6)本实验中,苯甲醛的产率为
苯甲酸乙酯( )可用作食用香精。实验室以苯甲酸(熔点122.1℃)与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。制备方法如下:
)可用作食用香精。实验室以苯甲酸(熔点122.1℃)与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。制备方法如下:
步骤①:在烧瓶中加入苯甲酸12.2g、乙醇60.0mL、浓硫酸5.0mL、适量环己烷。按如图所示安装好装置,加热烧瓶,控制一定温度加热回流2h。
步骤②:将烧瓶中的反应液倒入盛有100.0mL水的烧杯中,加入Na2CO3至溶液呈中性。
步骤③:用分液漏斗分离出有机层,再用乙醚萃取水层中的残留产品,二者合并,加到图乙的蒸馏装置中,加入沸石与无水硫酸镁,加热蒸馏制得产品5.0mL。
回答下列问题:
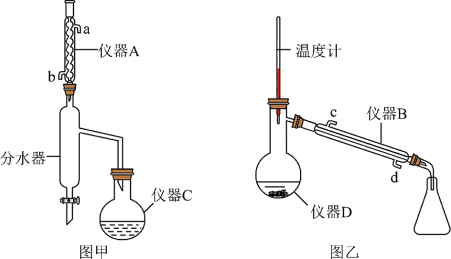
(1)仪器A的名称为___________ ,冷凝水的出水口为___________ (填“a”或“b”),本实验中浓硫酸的作用是___________ 。
(2)环己烷、乙醇和水可形成共沸物,沸点为62.1℃,仪器C的最佳加热方式为___________ 。
(3)写出制备苯甲酸乙酯反应的化学方程式:___________ 。
(4)图甲中分水器的“分水”原理是冷凝液在分水器中分层,上层有机层从支管处流回烧瓶,下层水层从分水器下口放出,反应结束的标志是___________ 。
(5)步骤②中加入Na2CO3的作用是___________ 。
(6)该实验中苯甲酸乙酯的产率为___________ %(保留三位有效数字)。
 )可用作食用香精。实验室以苯甲酸(熔点122.1℃)与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。制备方法如下:
)可用作食用香精。实验室以苯甲酸(熔点122.1℃)与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。制备方法如下:步骤①:在烧瓶中加入苯甲酸12.2g、乙醇60.0mL、浓硫酸5.0mL、适量环己烷。按如图所示安装好装置,加热烧瓶,控制一定温度加热回流2h。
步骤②:将烧瓶中的反应液倒入盛有100.0mL水的烧杯中,加入Na2CO3至溶液呈中性。
步骤③:用分液漏斗分离出有机层,再用乙醚萃取水层中的残留产品,二者合并,加到图乙的蒸馏装置中,加入沸石与无水硫酸镁,加热蒸馏制得产品5.0mL。
| 物质名称 | 苯甲酸 | 乙醇 | 环己烷 | 苯甲酸乙酯 |
| 相对分子质量 | 122 | 46 | 84 | 150 |
| 密度/g·cm-3 | 1.2659 | 0.7893 | 0.7318 | 1.0500 |
| 沸点/℃ | 249.2 | 78.3 | 80.8 | 212.61 |
(1)仪器A的名称为
(2)环己烷、乙醇和水可形成共沸物,沸点为62.1℃,仪器C的最佳加热方式为
(3)写出制备苯甲酸乙酯反应的化学方程式:
(4)图甲中分水器的“分水”原理是冷凝液在分水器中分层,上层有机层从支管处流回烧瓶,下层水层从分水器下口放出,反应结束的标志是
(5)步骤②中加入Na2CO3的作用是
(6)该实验中苯甲酸乙酯的产率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


