解答题-原理综合题 较难0.4 引用1 组卷116
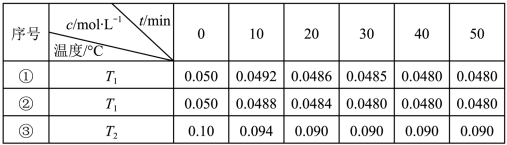
纳米级Cu2O由于具有优良的催化性能而受关注,表中为制取Cu2O的两种方法:
(1)工业上常用方法b制取Cu2O而很少用方法a,其原因是反应条件不易控制,若控温不当易生成____ 而使Cu2O产率降低。
(2)已知:①2Cu(s)+ O2(g)=Cu2O(s) △H1=-169kJ·mol-1
O2(g)=Cu2O(s) △H1=-169kJ·mol-1
②C(s)+ O2(g)=CO(g) △H2=-110.5kJ·mol-1
O2(g)=CO(g) △H2=-110.5kJ·mol-1
③Cu(s)+ O2(g)=CuO(s) △H3=-157kJ·mol-1
O2(g)=CuO(s) △H3=-157kJ·mol-1
则方法a中发生的反应:2CuO(s)+C(s)=Cu2O(s)+CO(g) △H=____ 。
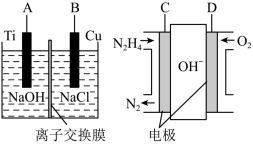
(3)方法b是用液态肼燃料电池为电源,通过离子交换膜电解法控制电解液中OH—的浓度来制备纳米Cu2O,装置如图所示:
①上述装置中B电极应连____ (填“C”或“D”)电极。
②该离子交换膜为____ (填“阴”或“阳”)离子交换膜,该电解池的阴极反应式____ 。
③原电池中负极反应式为____ 。
| 方法a | 用炭粉在高温条件下还原CuO |
| 方法b | 电解法,反应为2Cu+H2O |
(1)工业上常用方法b制取Cu2O而很少用方法a,其原因是反应条件不易控制,若控温不当易生成
(2)已知:①2Cu(s)+
②C(s)+
③Cu(s)+
则方法a中发生的反应:2CuO(s)+C(s)=Cu2O(s)+CO(g) △H=
(3)方法b是用液态肼燃料电池为电源,通过离子交换膜电解法控制电解液中OH—的浓度来制备纳米Cu2O,装置如图所示:

①上述装置中B电极应连
②该离子交换膜为
③原电池中负极反应式为
22-23高二上·福建泉州·开学考试
类题推荐
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的两种方法:
(1)已知:2Cu(s) + 1/2 O2(g) = Cu2O(s) △H = -169KJ/mol
C(s) +1/2 O2(g) = CO(g) △H= -110.5kJ/mol
Cu(s) + 1/2 O2(g) = CuO(s) △H = -157kJ/mol
则方法Ⅰ反应的热化学方程式为______________________ 。
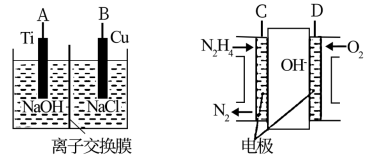
(2)方法Ⅱ采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。
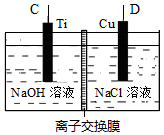
①上述装置中D电极应连接肼燃料电池的_______ 极(填“A”或“B”),该电解池中离子交换膜为______ 离子交换膜(填“阴”或“阳”)。
②该电解池的阳极反应式为_______________________________ ,肼燃料电池中A极发生的电极反应为___________________________________ 。
③当反应生成14.4 g Cu2O时,至少需要肼______ mol。
方法Ⅰ | 用炭粉在高温条件下还原CuO |
方法Ⅱ | 电解法的反应为2Cu+H2O |
(1)已知:2Cu(s) + 1/2 O2(g) = Cu2O(s) △H = -169KJ/mol
C(s) +1/2 O2(g) = CO(g) △H= -110.5kJ/mol
Cu(s) + 1/2 O2(g) = CuO(s) △H = -157kJ/mol
则方法Ⅰ反应的热化学方程式为
(2)方法Ⅱ采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。


图甲 图乙
①上述装置中D电极应连接肼燃料电池的
②该电解池的阳极反应式为
③当反应生成14.4 g Cu2O时,至少需要肼
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
(1)已知:①2Cu(s)+ O2(g)=Cu2O(s);△H = -169kJ·mol-1
O2(g)=Cu2O(s);△H = -169kJ·mol-1
②C(s)+ O2(g)=CO(g);△H = -110.5kJ·mol-1
O2(g)=CO(g);△H = -110.5kJ·mol-1
③Cu(s)+ O2(g)=CuO(s);△H = -157kJ·mol-1
O2(g)=CuO(s);△H = -157kJ·mol-1
则方法a发生反应的热化学方程式是:____________ 。
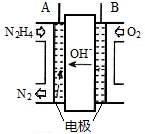
(2)方法c采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示:
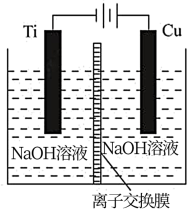
该离子交换膜为__________ 离子交换膜(填“阴”或“阳”),该电池的阳极反应式为___________ ,钛极附近的pH值______ (填“增大”“减小”或“不变”)。
(3)方法d为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2。该制法的化学方程式为________ 。
| 方法a | 用炭粉在高温条件下还原CuO |
| 方法b | 用葡萄糖还原新制的Cu(OH)2制备Cu2O |
| 方法c | 电解法,反应为 |
| 方法d | 用肼(N2H4)还原新制的Cu(OH)2 |
(1)已知:①2Cu(s)+
②C(s)+
③Cu(s)+
则方法a发生反应的热化学方程式是:
(2)方法c采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示:

该离子交换膜为
(3)方法d为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2。该制法的化学方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 Cu2O+H2↑
Cu2O+H2↑