解答题-无机推断题 较易0.85 引用3 组卷660
X、Y、Z、W、Q是元素周期表中原子序数依次增大的五种短周期主族元素,相关信息如表。
(1)元素Y在元素周期表中的位置是____ 。
(2)Z在氧气中完全燃烧所得产物的电子式为____ 。
(3)Y、W、Q的简单离子半径由大到小的顺序是____ (用离子符号表示)。
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。
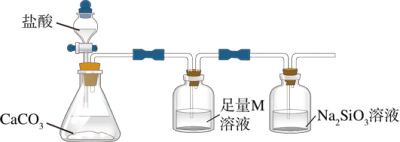
已知:H2SiO3是一种难溶于水的白色物质。
①M为____ (填化学式),其作用是____ 。
②能说明X元素的非金属性比硅元素强的实验现象是____ 。
(5)元素Z与W相比,金属性较弱的是____ (填元素名称),请写出能证明这一结论的实验事实_____ (列举一条)。
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是内层电子数的2倍 |
| Y | 其单质与氢气在暗处能剧烈化合并发生爆炸 |
| Z | 短周期元素中原子半径最大 |
| W | 其氧化物是两性氧化物 |
| Q | 同周期元素中,最高价氧化物对应水化物的酸性最强 |
(2)Z在氧气中完全燃烧所得产物的电子式为
(3)Y、W、Q的简单离子半径由大到小的顺序是
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。

已知:H2SiO3是一种难溶于水的白色物质。
①M为
②能说明X元素的非金属性比硅元素强的实验现象是
(5)元素Z与W相比,金属性较弱的是
21-22高一上·山东临沂·期末
类题推荐
元素周期表在学习、研究和生产实践中有很重要的作用。X、Y、Z、W、Q是原子序数依次增大的5种短周期主族元素,相关信息如表。
请回答下列问题:
(1)元素Y在元素周期表中的位置是______ 。
(2)Z的最高价氧化物的水化物含______ 键(填字母,下同),属于______ 。
A.离子键 B.共价键 C.离子化合物 D.共价化合物
(3)镓(Ga)与W同主族,其氢氧化物为两性氢氧化物。请写出氢氧化镓与NaOH反应的化学方程式:______ 。
(4)某同学为了探究X元素最高价氧化物与Na2SiO3溶液的反应,设计了如图所示装置进行实验。(已知:A为Q元素的氢化物。)
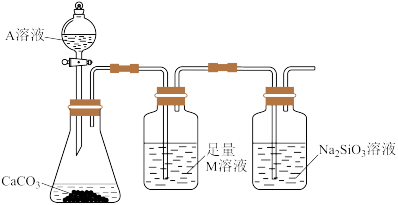
M为______ ,其作用是______ 。
| 元素编号 | 原子结构或元素及其化合物特性 |
| X | L层电子数是内层电子数的2倍 |
| Y | 地壳中含量最多的元素 |
| Z | 短周期元素中原子半径最大 |
| W | 氧化物是两性氧化物 |
| Q | 同周期元素中,最高价氧化物对应水化物的酸性最强 |
(1)元素Y在元素周期表中的位置是
(2)Z的最高价氧化物的水化物含
A.离子键 B.共价键 C.离子化合物 D.共价化合物
(3)镓(Ga)与W同主族,其氢氧化物为两性氢氧化物。请写出氢氧化镓与NaOH反应的化学方程式:
(4)某同学为了探究X元素最高价氧化物与Na2SiO3溶液的反应,设计了如图所示装置进行实验。(已知:A为Q元素的氢化物。)

M为
元素周期表在学习、研究和生产实践中有很重要的作用。X、Y、Z、W、Q是原子序数依次增大的5种短周期主族元素,相关信息如下表。
请回答下列问题:
(1)元素Y在元素周期表中的位置是_______ 。
(2)单质Z通常保存在_______ 里,以隔绝空气。Z的最高价氧化物的水化物含_______ 键(填字母,下同),属于_______ 。
A.离子键 B.共价键 C.离子化合物 D.共价化合物
(3)镓 与W同主族,其氢氧化物为两性氢氧化物。请写出氢氧化镓与
与W同主族,其氢氧化物为两性氢氧化物。请写出氢氧化镓与 反应的化学方程式:
反应的化学方程式:_______ 。
(4)某同学为了探究X元素最高价氧化物与 溶液的反应,设计了如图所示装置进行实验。(已知:A为Q元素的氢化物。)
溶液的反应,设计了如图所示装置进行实验。(已知:A为Q元素的氢化物。)
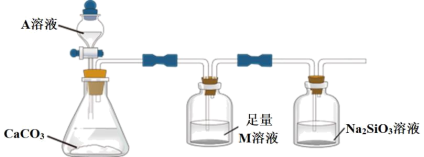
M为_______ ,其作用是_______ 。
| 元素编号 | 原子结构或元素及其化合物特性 |
| X | L层电子数是内层电子数的2倍 |
| Y | 地壳中含量最多的元素 |
| Z | 短周期元素中原子半径最大 |
| W | 氧化物是两性氧化物 |
| Q | 同周期元素中,最高价氧化物对应水化物的酸性最强 |
(1)元素Y在元素周期表中的位置是
(2)单质Z通常保存在
A.离子键 B.共价键 C.离子化合物 D.共价化合物
(3)镓
(4)某同学为了探究X元素最高价氧化物与

M为
现有部分元素的性质与原子或分子结构的相关信息如表所示:
(1)T、X、Y、Z形成的简单离子半径由大到小的顺序是_______ 。(用离子符号表示)
(2)元素Y与元素Z相比,金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是_______ 填字母序号。
A.Y单质的熔点比Z单质的低
B.Y的化合价比Z的低
C.常温下Y单质与水反应很剧烈,而Z单质与水很难反应
D.Y最高价氧化物对应的水化物的碱性比Z的强
(3)T与Y两种元素能形成既含离子键又含非极性共价键的常见化合物,写出该化合物的电子式_______ 。Y与和T同主族短周期元素M也能形成类似结构的化合物,请写出该化合物与硫酸反应的化学方程式_______ 。
(4)元素X与氢元素以原子个数共1∶2化合时,形成可用于火箭燃料的化合物W(W的相对分子质量为32)。元素T和氢元素以原子个数比1∶1化合形成化合物Q。Q与W发生氧化还原反应生成X的单质和的T另一种氢化物,请写出Q与W反应的化学方程式_______ 。
| 元素编号 | 元素性质与原子(或分子)结构的相关信息 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质分子为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 其离子是第三周期金属元素的离子中半径最小的 |
(2)元素Y与元素Z相比,金属性较强的是
A.Y单质的熔点比Z单质的低
B.Y的化合价比Z的低
C.常温下Y单质与水反应很剧烈,而Z单质与水很难反应
D.Y最高价氧化物对应的水化物的碱性比Z的强
(3)T与Y两种元素能形成既含离子键又含非极性共价键的常见化合物,写出该化合物的电子式
(4)元素X与氢元素以原子个数共1∶2化合时,形成可用于火箭燃料的化合物W(W的相对分子质量为32)。元素T和氢元素以原子个数比1∶1化合形成化合物Q。Q与W发生氧化还原反应生成X的单质和的T另一种氢化物,请写出Q与W反应的化学方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


