解答题-原理综合题 适中0.65 引用1 组卷117
次鳞酸 )是一种精细化工产品。
)是一种精细化工产品。
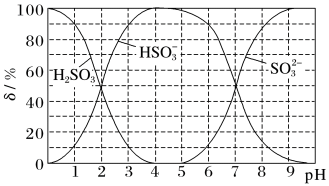
(1) 溶液中的含鳞微粒只有
溶液中的含鳞微粒只有 和
和 ,则该溶液量
,则该溶液量_______ 性(填“酸”“碱”或“中”),原因是_______ (用离子方程式解释); 为
为_______ (填“正盐”或“酸式盐”), 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为_______ 。
(2) 时,将相同物质的量浓度的
时,将相同物质的量浓度的 溶液和盐酸分别加水稀释至相同的倍数,此时
溶液和盐酸分别加水稀释至相同的倍数,此时 溶液的
溶液的
_______ (填“大于”“小于”或“等于”)盐酸的 。
。
(3)常温下, 溶液中
溶液中
_______ [用含 和
和 的代数式表示]。
的代数式表示]。
(1)
(2)
(3)常温下,
21-22高二上·安徽亳州·期末
类题推荐
(Ⅰ)部分弱酸的电离平衡常数如下表:
(1)室温下①0.1 mol·L-1 HCOONa,②0.1 mol·L-1 NaClO,③0.1 mol·L-1 Na2CO3,④0.1 mol·L-1 NaHCO3溶液的pH由大到小的关系为______________________ 。
(2)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为____________________ 。
(3)少量CO2通入到过量的NaClO溶液中发生反应的离子方程式______________ 。
(4)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为__________________ 。
(Ⅱ)某小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2SO4溶液。
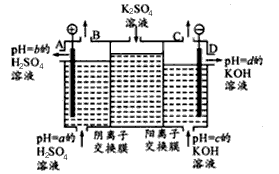
①该电解槽中通过阴离子交换膜的离子数_______ (填“>”“<”或“一”)通过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为_____________ ;
③电解一段时间后,B出口与C出口产生气体的质量比为______________ 。
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25 ℃) | Ka=1.77 ×10-4 | Ka=4.0 ×10-8 | Ka1=4.3×10-7 Ka2=4.7×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(1)室温下①0.1 mol·L-1 HCOONa,②0.1 mol·L-1 NaClO,③0.1 mol·L-1 Na2CO3,④0.1 mol·L-1 NaHCO3溶液的pH由大到小的关系为
(2)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为
(3)少量CO2通入到过量的NaClO溶液中发生反应的离子方程式
(4)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为
(Ⅱ)某小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2SO4溶液。

①该电解槽中通过阴离子交换膜的离子数
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为
③电解一段时间后,B出口与C出口产生气体的质量比为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网