单选题 适中0.65 引用2 组卷215
通过下列反应合成CO和CH4,可实现CO2的再转化:
①CO2(g)+4H2(g) CH4(g)+2H2O(g) △H<0
CH4(g)+2H2O(g) △H<0
②CO2(g)+H2(g) CO(g)+H2O(g) △H>0
CO(g)+H2O(g) △H>0
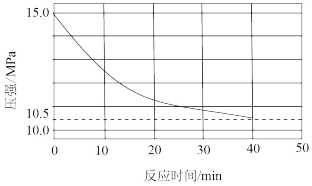
在密闭容器中通入3 mol的H2和1 mol的CO2,分别在压强为1 MPa 和10 MPa下进行反应。实验中对平衡体系的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4在三种物质中的体积分数影响如图所示。
下列说法不正确的是
①CO2(g)+4H2(g)
②CO2(g)+H2(g)
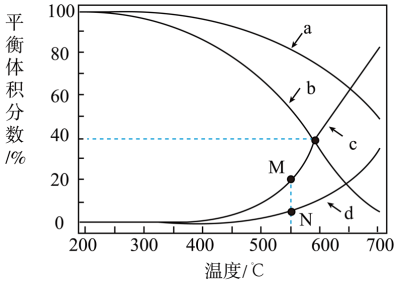
在密闭容器中通入3 mol的H2和1 mol的CO2,分别在压强为1 MPa 和10 MPa下进行反应。实验中对平衡体系的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4在三种物质中的体积分数影响如图所示。

下列说法不正确的是
| A.曲线a表示10 MPa条件下CH4的体积分数随温度的变化 |
| B.曲线a、d交点纵坐标可能为40% |
| C.550°C时M点位于N点上方是由于压强降低时,平衡①逆向移动导致平衡②正向移动 |
| D.由曲线b、c的交点可计算该温度下反应②的平衡常数为2.4 |
21-22高三上·江苏·阶段练习
类题推荐
在2020年中央经济工作会议上,我国明确提出“碳达峰”与“碳中和”目标。使利用CO2合成高价值化学品更突显其重要性。
Ⅰ.工业上可以利用CO2和H2合成CH3OH:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)ΔH<0。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应起始物质的量如表:
(1)达到平衡时,CO2的体积分数φ①_____ φ②(填“>”“<”或“=”)。
(2)当_____ = v逆(H2)时,说明反应在条件②达到平衡状态。
v逆(H2)时,说明反应在条件②达到平衡状态。
Ⅱ.利用CH4超干重整CO2的催化转化如图所示:
(3)CH4与CO2超干重整反应的方程式为_____ 。
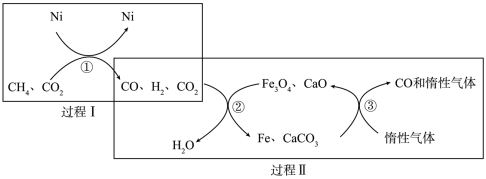
(4)有关转化过程,下列说法正确的是_____ (填序号)。
a.过程Ⅰ中CO2未参与反应
b.过程Ⅱ实现了含碳物质与含氢物质的分离
c.转化②中CaO消耗过程中的CO2,有利于反应正向进行
d.转化③中Fe与CaCO3反应的物质的量之比为4∶3
Ⅲ.通过下列反应可实现CO2的再转化,合成CO、CH4:
①CO2(g)+4H2(g)=CH4(g)+2H2O(g)ΔH<0
②CO2(g)+H2(g)=CO(g)+H2O(g)ΔH>0
在密闭容器中通入3mol的H2和1mol的CO2,分别在压强为1MPa和10MPa下进行反应。实验中对平衡体系的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4在三种物质中的体积分数影响如图所示。
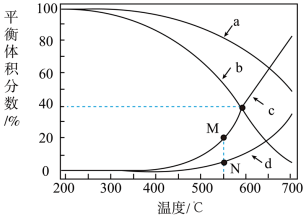
(5)1MPa时,表示CH4和CO平衡体积分数随温度变化关系的曲线分别是_____ 和_____ 。M点平衡体积分数高于N点的原因是_____ 。
(6)图中当CH4和CO平衡体积分数均为40%时,若容器的体积为1L,该温度下反应①的平衡常数K的值为_____ 。
Ⅰ.工业上可以利用CO2和H2合成CH3OH:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)ΔH<0。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应起始物质的量如表:
| 反应条件 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
| ①恒温恒容 | 1 | 3 | 0 | 0 |
| ②绝热恒容 | 0 | 0 | 1 | 1 |
(1)达到平衡时,CO2的体积分数φ①
(2)当
Ⅱ.利用CH4超干重整CO2的催化转化如图所示:
(3)CH4与CO2超干重整反应的方程式为

(4)有关转化过程,下列说法正确的是
a.过程Ⅰ中CO2未参与反应
b.过程Ⅱ实现了含碳物质与含氢物质的分离
c.转化②中CaO消耗过程中的CO2,有利于反应正向进行
d.转化③中Fe与CaCO3反应的物质的量之比为4∶3
Ⅲ.通过下列反应可实现CO2的再转化,合成CO、CH4:
①CO2(g)+4H2(g)=CH4(g)+2H2O(g)ΔH<0
②CO2(g)+H2(g)=CO(g)+H2O(g)ΔH>0
在密闭容器中通入3mol的H2和1mol的CO2,分别在压强为1MPa和10MPa下进行反应。实验中对平衡体系的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4在三种物质中的体积分数影响如图所示。

(5)1MPa时,表示CH4和CO平衡体积分数随温度变化关系的曲线分别是
(6)图中当CH4和CO平衡体积分数均为40%时,若容器的体积为1L,该温度下反应①的平衡常数K的值为
利用CO2合成高价值化学品,是重要的减碳方式。
(1)利用CO2和H2在催化剂的作用下合成甲醇,反应如下:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。已知反应相关的键能数据如表:
CH3OH(g)+H2O(g)。已知反应相关的键能数据如表:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=
CH3OH(g)+H2O(g) △H=___ 。
(2)某温度下,向体积为2L的恒容密闭容器中充入一定量的H2和CO2的混合气体,发生反应CO2(g)+2H2(g) CH2O(g)+H2O(g) △H=-6kJ·mol-1。容器内气体初始压强为1.2kPa,反应达到平衡时,CH2O的分压与起始时
CH2O(g)+H2O(g) △H=-6kJ·mol-1。容器内气体初始压强为1.2kPa,反应达到平衡时,CH2O的分压与起始时 的关系如图所示:
的关系如图所示:
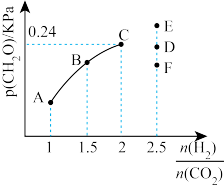
①当 =2时,反应达到平衡后,若再向容器中加入CO2(g)和H2O(g),使二者分压均增大0.05kPa,则达到新平衡时,H2的转化率将
=2时,反应达到平衡后,若再向容器中加入CO2(g)和H2O(g),使二者分压均增大0.05kPa,则达到新平衡时,H2的转化率将____ (填“增大”“减小”或“不变”)。
②当 =2.5时,反应达到平衡状态后,CH2O的分压可能是图象中的点
=2.5时,反应达到平衡状态后,CH2O的分压可能是图象中的点____ (填“D”、“E"或“F"),原因为___ 。
(3)通过下列反应也可实现CO2的再转化,合成CO、CH4。
I.CO2(g)+4H2(g) CH4(g)+2H2O(g) △H<0
CH4(g)+2H2O(g) △H<0
II.CO2(g)+H2(g) CO(g)+H2O(g) △H>0
CO(g)+H2O(g) △H>0
在密闭容器中通入3molH2和1molCO2,分别在压强为1MPa和10MPa下进行反应。实验中对平衡体系中的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4在三种物质中的体积分数的影响如图所示。
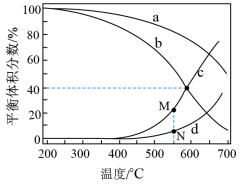
①1MPa时,表示CH4和CO平衡体积分数随温度变化关系的曲线分别是____ 和____ 。M点平衡体积分数高于N点的原因是____ 。
②图中当CH4和CO平衡体积分数均为40%时,若容器的体积为1L,则该温度下反应I的平衡常数K的值为____ 。
(1)利用CO2和H2在催化剂的作用下合成甲醇,反应如下:CO2(g)+3H2(g)
| 化学键 | H—H | C—O | C=O | H—O | C—H |
| 键能/(kJ·mol-1) | 436 | 343 | 803 | 464 | 414 |
CO2(g)+3H2(g)
(2)某温度下,向体积为2L的恒容密闭容器中充入一定量的H2和CO2的混合气体,发生反应CO2(g)+2H2(g)

①当
②当
(3)通过下列反应也可实现CO2的再转化,合成CO、CH4。
I.CO2(g)+4H2(g)
II.CO2(g)+H2(g)
在密闭容器中通入3molH2和1molCO2,分别在压强为1MPa和10MPa下进行反应。实验中对平衡体系中的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4在三种物质中的体积分数的影响如图所示。

①1MPa时,表示CH4和CO平衡体积分数随温度变化关系的曲线分别是
②图中当CH4和CO平衡体积分数均为40%时,若容器的体积为1L,则该温度下反应I的平衡常数K的值为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网