计算题 适中0.65 引用1 组卷570
回答下列问题:
(1)Cl2通入水中制氯水,反应的离子方程式:____ 。
(2)高铁酸钾(K2FeO4)被人们称为“绿色化学”净水剂。高铁酸钾在酸性至弱碱性条件下不稳定。工业上用KClO与Fe(NO3)3溶液反应制得K2FeO4,反应的离子方程式:____ 。
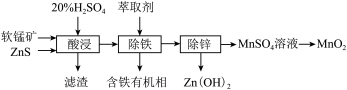
(3)以软锰矿(主要成分为MnO2、SiO2等)为原料制备高纯MnO2的流程如图:
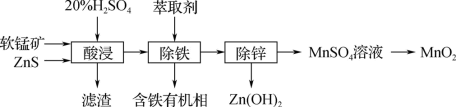
①滤渣中含大量硫单质,酸浸时主要反应的化学方程式:____ 。
②酸性条件下,用合适的氧化剂可以将MnSO4转化为高纯MnO2。用NaClO3作氧化剂时会同时产生NaCl,该反应的离子方程式:____ 。
(4)已知次氯酸可被FeSO4等物质还原。用下列实验方案测定某次试验所得溶液中次氯酸的物质的量浓度:量取10.00mL上述次氯酸溶液,并稀释至100mL,再从其中取出10.00mL于锥形瓶中,并加入10.00mL0.8000mol/L的FeSO4溶液,充分反应后,用0.05000mol/L的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液24.00mL,则原次氯酸溶液的浓度为____ (写出计算过程)。
(1)Cl2通入水中制氯水,反应的离子方程式:
(2)高铁酸钾(K2FeO4)被人们称为“绿色化学”净水剂。高铁酸钾在酸性至弱碱性条件下不稳定。工业上用KClO与Fe(NO3)3溶液反应制得K2FeO4,反应的离子方程式:
(3)以软锰矿(主要成分为MnO2、SiO2等)为原料制备高纯MnO2的流程如图:

①滤渣中含大量硫单质,酸浸时主要反应的化学方程式:
②酸性条件下,用合适的氧化剂可以将MnSO4转化为高纯MnO2。用NaClO3作氧化剂时会同时产生NaCl,该反应的离子方程式:
(4)已知次氯酸可被FeSO4等物质还原。用下列实验方案测定某次试验所得溶液中次氯酸的物质的量浓度:量取10.00mL上述次氯酸溶液,并稀释至100mL,再从其中取出10.00mL于锥形瓶中,并加入10.00mL0.8000mol/L的FeSO4溶液,充分反应后,用0.05000mol/L的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液24.00mL,则原次氯酸溶液的浓度为
22-23高三上·江苏淮安·阶段练习
类题推荐
工业以软锰矿(主要成分 ,含
,含 、
、 、
、 等杂质)和硫铁矿(主要成分为
等杂质)和硫铁矿(主要成分为 )为原料制备高纯
)为原料制备高纯 的流程如下。
的流程如下。
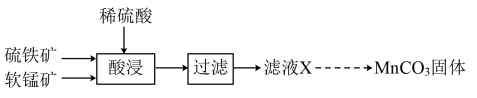
已知:
ⅰ.滤液X中的金属阳离子主要为 、
、 ,还含有少量的
,还含有少量的 和
和 。
。
ⅱ.常温下,溶液中部分金属离子开始沉淀时的pH见下表(金属离子浓度以1mol/L计算)。
(1)基态锰原子的核外电子排布式为___________ 。
(2)“过滤”所得滤渣中含有S、等,生成硫单质的离子方程式为___________ 。
(3)为获得高纯 (除杂时杂质离子浓度不大于
(除杂时杂质离子浓度不大于 ),请补充完整由滤液X制备高纯
),请补充完整由滤液X制备高纯 的实验方案:取滤液X,
的实验方案:取滤液X,___________ ,低温干燥,得高纯 。(实验中须使用的试剂:氨水、
。(实验中须使用的试剂:氨水、 固体、
固体、 、
、 溶液、蒸馏水)
溶液、蒸馏水)
(4)利用 制备
制备 过程中发生如下反应:
过程中发生如下反应: ,
,
 。为测定焙烧后所得氧化物的成分,设计如下实验:
。为测定焙烧后所得氧化物的成分,设计如下实验:
步骤1:取一定量固体,加入10.00mL 0.5000
 溶液,在酸性条件下充分反应。
溶液,在酸性条件下充分反应。
步骤2:用0.05000 的
的 滴定溶液中的
滴定溶液中的 ,滴定至终点时,消耗
,滴定至终点时,消耗 10.00mL。(
10.00mL。( 未配平)。
未配平)。
步骤3:加热条件下,加入适量 将溶液中
将溶液中 氧化为Mn(Ⅲ)。持续加热一段时间后冷却,用0.1500
氧化为Mn(Ⅲ)。持续加热一段时间后冷却,用0.1500 的
的 标准液滴定生成的Mn(Ⅲ),滴定至终点时,消耗标准溶液20.00mL。
标准液滴定生成的Mn(Ⅲ),滴定至终点时,消耗标准溶液20.00mL。
计算焙烧后产物中Mn和O的物质的量之比。(写出计算过程)________

已知:
ⅰ.滤液X中的金属阳离子主要为
ⅱ.常温下,溶液中部分金属离子开始沉淀时的pH见下表(金属离子浓度以1mol/L计算)。
| 金属离子 | ||||
| 开始沉淀pH | 1.5 | 3.3 | 6.5 | 8.3 |
(2)“过滤”所得滤渣中含有S、等,生成硫单质的离子方程式为
(3)为获得高纯
(4)利用
步骤1:取一定量固体,加入10.00mL 0.5000
步骤2:用0.05000
步骤3:加热条件下,加入适量
计算焙烧后产物中Mn和O的物质的量之比。(写出计算过程)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网