解答题-工业流程题 适中0.65 引用3 组卷490
磷酸锌常用作氯化橡胶合成高分子材料的阻燃剂。工业上利用烧渣灰(主要含ZnO,还含少量FeO、Al2O3、CuO及SiO2)为原料制取磷酸锌的工艺流程如图所示:
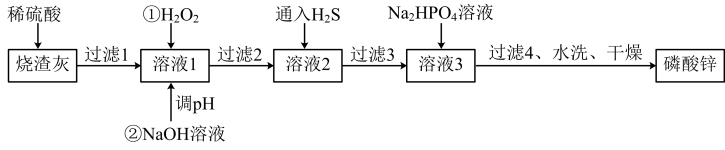
已知:①[Zn3(PO4)2]在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
(1)基态Zn原子的价电子排布式为______
(2)用硫酸浸烧渣灰,为提高酸浸时锌的浸出率,可以采取的措施是______ (填一条)。
(3)加入H2O2的作用_______
(4)经过滤2得到滤渣的主要成分是Fe(OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是______ 。
(5)加入Na2HPO4溶液发生反应的离子方程式为_____ 。
(6)洗涤磷酸锌沉淀时应选用____ (填“冷水”或“热水”),确认磷酸锌洗涤干净的操作是_____ 。
(7)通入H2S是为了除铜离子,25°C时,当通入H2S达到饱和时测得溶液的pH=1,c(H2S)=0.1mol·L-1,此时溶液中c(Cu2+)=6.3×10-15mol·L-1,则CuS的溶度积Ksp=______ (已知:25°C时,H2S的电离平衡常数Ka1=1×10-7,Ka2=1×10-15)。

已知:①[Zn3(PO4)2]在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.0 | 2.2 | 5.4 | 6.5 |
| 完全沉淀的pH | 5.0 | 3.6 | 6.7 | 8.5 |
(2)用硫酸浸烧渣灰,为提高酸浸时锌的浸出率,可以采取的措施是
(3)加入H2O2的作用
(4)经过滤2得到滤渣的主要成分是Fe(OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是
(5)加入Na2HPO4溶液发生反应的离子方程式为
(6)洗涤磷酸锌沉淀时应选用
(7)通入H2S是为了除铜离子,25°C时,当通入H2S达到饱和时测得溶液的pH=1,c(H2S)=0.1mol·L-1,此时溶液中c(Cu2+)=6.3×10-15mol·L-1,则CuS的溶度积Ksp=
22-23高三上·云南昆明·阶段练习
类题推荐
磷酸锌常用作氯化橡胶合成高分子材料的阻燃剂。工业上利用烧渣灰( 主要含ZnO,还含少量FeO、Al2O3、 CuO 及SiO2)为原料制取磷酸锌的工艺流程如图所示:
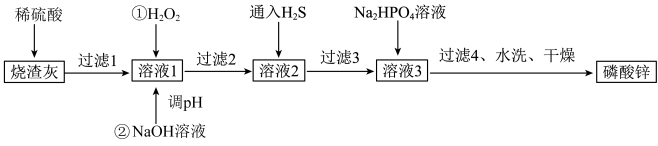
已知:①Zn3(PO4)2在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶液1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
回答下列问题:
(1)基态锌原子的价电子排布式为_____________ 。
(2)加入H2O2的作用是___________________________ 。
(3)经过滤2得到滤渣的主要成分是Fe( OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是___________ 。
(4)通入H2S的目的是除去Cu2+,写出该反应的离子方程式:_________________ 。
(5)洗涤磷酸锌沉淀时应选用________ (填“冷水”或“热水”),洗涤沉淀的操作是________________ 。
(6)图是碳化硅的晶胞结构,其晶体类型属于___________ 晶体。若碳化硅晶胞边长为a pm,阿伏加德罗常数的值为NA,则碳化硅晶体的密度为______________ g·cm-3 (列出计算式即可)。
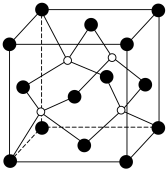

已知:①Zn3(PO4)2在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶液1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.0 | 2.2 | 5.4. | 6.5 |
| 完全沉淀的pH | 5.0 | 3.6 | 6.7 | 8.5 |
(1)基态锌原子的价电子排布式为
(2)加入H2O2的作用是
(3)经过滤2得到滤渣的主要成分是Fe( OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是
(4)通入H2S的目的是除去Cu2+,写出该反应的离子方程式:
(5)洗涤磷酸锌沉淀时应选用
(6)图是碳化硅的晶胞结构,其晶体类型属于

某大型企业以工业烧渣(主要含ZnO,还含少量Fe3O4、Al2O3、CuO及SiO2等)为原料制取有机高分子材料的阻燃剂——磷酸锌[Zn3(PO4)2]的工艺流程如图所示。

已知:室温下,几种金属离子开始沉淀与沉淀完全的pH如下表所示。
(1)在180 °C对“烧渣灰”进行酸溶最适合的酸是_______ (填“盐酸”、“硫酸”或“硝酸”)。
(2)加入双氧水的作用是作氧化剂,则发生反应的离子方程式为_______ ;可用NaClO代替双氧水,两者相比,_______ (填化学式)的氧化效率更高。(氧化效率以单位质量的氧化剂得到的电子数表示)
(3)加氨水过程中加热的目的是_______ ;“过滤2”得到的滤渣的主要成分为_______ (填化学式)。
(4)通入H2S的目的是_______ ;加入Na2 HPO4发生反应的离子方程式为_______ 。
(5)确认磷酸锌洗涤干净的操作是_______ 。
(6)在通入H2S之前,“溶液3”中A13+的浓度为_______ mol·L-1。

已知:室温下,几种金属离子开始沉淀与沉淀完全的pH如下表所示。
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.7 | 2.2 | 5.2 | 6.5 |
| 沉淀完全(c=1.0×10-5mol· L-1)的pH | 4.2 | 3.2 | 6.7 | 8.0 |
(2)加入双氧水的作用是作氧化剂,则发生反应的离子方程式为
(3)加氨水过程中加热的目的是
(4)通入H2S的目的是
(5)确认磷酸锌洗涤干净的操作是
(6)在通入H2S之前,“溶液3”中A13+的浓度为
自2021年美国央行的大量放水,大宗原材料价格猛涨,企业十分重视提高原材料的利用率。某大型企业以工业烧渣(主要含ZnO,还含少量Fe3O4、Al2O3、CuO及SiO2等)为原料制取有机高分子材料的阻燃剂一磷酸锌[Zn3(PO4)2]的工艺流程如图所示。
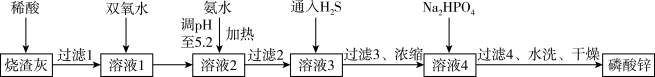
已知:室温下,几种金属离子开始沉淀与沉淀完全的pH如下表所示。
(1)在180 °C对“烧渣灰”进行酸溶最适合的酸是_______ (填“盐酸”、“硫酸”或“硝酸”)。
(2)加入双氧水的作用是作氧化剂,则发生反应的化学方程式为_______ ;可用NaClO代替双氧水,两者相比,_______ (填化学式)的氧化效率更高。(氧化效率以单位质量的氧化剂得到的电子数表示)
(3)加氨水过程中加热的目的是_______ ;“过滤2”得到的滤渣的主要成分为_______ (填化学式)。
(4)通入H2S的目的是_______ ;加入Na2 HPO4发生反应的离子方程式为_______ 。
(5)确认磷酸锌洗涤干净的操作是_______ 。
(6)在通入H2S之前,“溶液3”中A13+的浓度为_______ mol·L-1。

已知:室温下,几种金属离子开始沉淀与沉淀完全的pH如下表所示。
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.7 | 2.2 | 5.2 | 6.5 |
| 沉淀完全(c=1.0×10-5mol· L-1)的pH | 4.7 | 3.2 | 6.7 | 8.0 |
(2)加入双氧水的作用是作氧化剂,则发生反应的化学方程式为
(3)加氨水过程中加热的目的是
(4)通入H2S的目的是
(5)确认磷酸锌洗涤干净的操作是
(6)在通入H2S之前,“溶液3”中A13+的浓度为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


