解答题-实验探究题 适中0.65 引用1 组卷214
某研究小组用印刷电路板的腐蚀废液(主要含CuCl2、FeCl2、FeCl3)制备Cu(NH4)2SO4•H2O和FeCl2•4H2O。
I.制备流程图
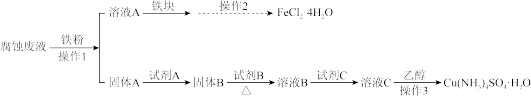
已知1.所加试剂均足量,且部分步骤有省略。
II.Cu(NH4)2SO4•H2O晶体纯度测定
①取a g Cu(NH4)2SO4•H2O晶体,加入适量1 mol·L-1稀硫酸,加热,待溶液冷却后配制成250 mL溶液。
②取25.00 mL溶液,加水50 mL,调节溶液至弱酸性(pH=3~4),加入过量20%KI溶液,避光静置几分钟。
③用c mol·L-1Na2S2O3标准溶液滴定至溶液呈淡黄色,再加入淀粉溶液,继续滴定至溶液变浅蓝色,再加入一定量10%KSCN溶液,蓝色变深,继续滴定至蓝色刚好消失,记录消耗Na2S2O3标准溶液的体积。
④平行滴定三次,消耗Na2S2O3标准溶液的平均体积为V mL。
已知2:①2Cu2++4I-=2CuI↓+I2;I2+2 =
= +2I-。
+2I-。
②CuI和CuSCN均为白色固体;Ksp(CuI)=1.1×10-12,Ksp(CuSCN)=4.8×10-15。
请回答:
(1)下列说法正确的是____ 。
(2)测定晶体纯度时,步骤②用KI溶液测定铜含量时,需在弱酸性(pH=3~4)溶液中进行的原因____ 。
(3)下列关于滴定分析的描述,正确的是____ 。
(4)结合离子反应方程式并用必要的文字说明滴定过程中加入KSCN溶液的作用____ 。
(5)Cu(NH4)2SO4•H2O(M=246 g•mol-1)晶体样品的纯度为____ %(用含a、c、V的代数式表示)。
I.制备流程图
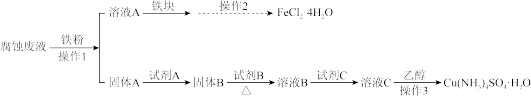
已知1.所加试剂均足量,且部分步骤有省略。
II.Cu(NH4)2SO4•H2O晶体纯度测定
①取a g Cu(NH4)2SO4•H2O晶体,加入适量1 mol·L-1稀硫酸,加热,待溶液冷却后配制成250 mL溶液。
②取25.00 mL溶液,加水50 mL,调节溶液至弱酸性(pH=3~4),加入过量20%KI溶液,避光静置几分钟。
③用c mol·L-1Na2S2O3标准溶液滴定至溶液呈淡黄色,再加入淀粉溶液,继续滴定至溶液变浅蓝色,再加入一定量10%KSCN溶液,蓝色变深,继续滴定至蓝色刚好消失,记录消耗Na2S2O3标准溶液的体积。
④平行滴定三次,消耗Na2S2O3标准溶液的平均体积为V mL。
已知2:①2Cu2++4I-=2CuI↓+I2;I2+2
②CuI和CuSCN均为白色固体;Ksp(CuI)=1.1×10-12,Ksp(CuSCN)=4.8×10-15。
请回答:
(1)下列说法正确的是
| A.操作2通过蒸发至出现晶膜后趁热过滤,快速冷却滤液结晶,可得较大FeCl2•4H2O晶体 |
| B.可用KSCN或K3[Fe(CN)6]溶液检验FeCl2•4H2O晶体中是否存在杂质Fe3+ |
| C.溶液C中加入乙醇可以降低Cu(NH4)2SO4•H2O在溶剂中的溶解性,促进晶体析出 |
| D.溶液B中逐滴滴加试剂C至过量的过程中先出现蓝色沉淀后变为深蓝色溶液,这一现象可以说明与Cu2+结合能力大小为:NH3>OH->H2O |
(3)下列关于滴定分析的描述,正确的是
| A.加入过量20%KI溶液可以增大I2的溶解性,减少实验滴定误差 |
| B.Na2S2O3标准溶液应盛放在碱式滴定管中 |
| C.滴定时,眼睛应一直观察滴定管中溶液体积的变化 |
| D.若滴定恰好完全时,滴定管尖端悬半滴未滴下,会导致测定结果偏低 |
(5)Cu(NH4)2SO4•H2O(M=246 g•mol-1)晶体样品的纯度为
22-23高三上·浙江·开学考试
类题推荐
某研究小组用印刷电路板的腐蚀废液(主要含 、
、 、
、 )制备
)制备 和
和 。
。
I.制备流程图(部分步骤有省略) 晶体纯度测定
晶体纯度测定
①取a g 晶体,加入适量1
晶体,加入适量1 稀硫酸,溶解后配成250mL溶液。
稀硫酸,溶解后配成250mL溶液。
②取25.00mL溶液,调节溶液至弱酸性(pH=3~4),加入过量KI溶液,避光静置几分钟。
③用c
 标准溶液滴定至溶液呈淡黄色,再加入淀粉溶液,继续滴定至溶液变浅蓝色,再加入一定量KSCN溶液,蓝色变深,继续滴定至蓝色刚好消失,平行滴定三次,消耗
标准溶液滴定至溶液呈淡黄色,再加入淀粉溶液,继续滴定至溶液变浅蓝色,再加入一定量KSCN溶液,蓝色变深,继续滴定至蓝色刚好消失,平行滴定三次,消耗 标准溶液的平均体积为V mL。
标准溶液的平均体积为V mL。
已知:
① 易溶于水,难溶于乙醇,受热易分解产生
易溶于水,难溶于乙醇,受热易分解产生 ;
;
② ,
, ;
;
③CuI和CuSCN均为白色固体,且对 的吸附能力不同。
的吸附能力不同。
请回答:
(1)滴定操作时用于盛放 标准溶液的仪器是
标准溶液的仪器是___________ 。
(2)下列说法正确的是___________。
(3)溶液C经过操作2生成 晶体的操作(选出正确操作并排序)是:
晶体的操作(选出正确操作并排序)是:___________ 。
将溶液C倒入烧杯中→___________→___________→___________→低温干燥
A.过滤
B.用乙醇洗涤沉淀
C.用蒸馏水洗涤沉淀
D.加热蒸发浓缩,冷却结晶
E.加入95%乙醇,并用玻璃棒摩擦烧杯内壁至晶体出现
(4)固体A中去除一种单质所用物质X不可行的是___________ 。
A.稀硫酸溶液 B.稀硝酸溶液 C.硫酸铜溶液
(5)加入KSCN溶液是为了将CuI固体表面吸附的 释放出来,提高测定结果的准确度,请用离子反应方程式说明理由
释放出来,提高测定结果的准确度,请用离子反应方程式说明理由___________ 。
(6) 晶体样品的纯度为
晶体样品的纯度为___________ (用含a、c、V的代数式表示)。
I.制备流程图(部分步骤有省略)

①取a g
②取25.00mL溶液,调节溶液至弱酸性(pH=3~4),加入过量KI溶液,避光静置几分钟。
③用c
已知:
①
②
③CuI和CuSCN均为白色固体,且对
请回答:
(1)滴定操作时用于盛放
(2)下列说法正确的是___________。
| A.操作1通过蒸发至出现晶膜后趁热过滤,快速冷却结晶,可得较大晶体 |
| B.加入过量KI溶液可以增大 |
| C.若滴定恰好完全时,滴定管尖端悬半滴未滴下,会导致测定结果偏高 |
| D.溶液B转化为溶液C的现象说明结合 |
(3)溶液C经过操作2生成
将溶液C倒入烧杯中→___________→___________→___________→低温干燥
A.过滤
B.用乙醇洗涤沉淀
C.用蒸馏水洗涤沉淀
D.加热蒸发浓缩,冷却结晶
E.加入95%乙醇,并用玻璃棒摩擦烧杯内壁至晶体出现
(4)固体A中去除一种单质所用物质X不可行的是
A.稀硫酸溶液 B.稀硝酸溶液 C.硫酸铜溶液
(5)加入KSCN溶液是为了将CuI固体表面吸附的
(6)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网