解答题-原理综合题 较难0.4 引用2 组卷255
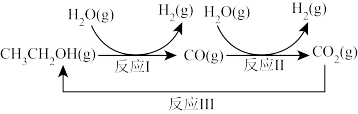
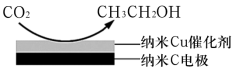
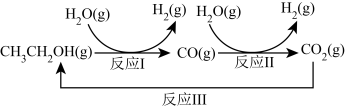
十九大报告提出要对环境问题进行全面、系统的可持续治理。绿色能源堤实施可持续发展的重要途径,利用生物乙醇来制取绿色能源氢气的部分反应过程如图所示:
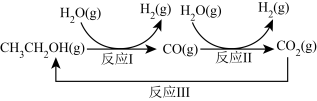
(1)已知:CO(g)+H2O(g) CO2(g)+H2(g) △H1=-41kJ/mol
CO2(g)+H2(g) △H1=-41kJ/mol
CH3CH2OH(g)+3H2O(g) 2CO2(g)+6H2(g) △H2=+174.1kJ/mol
2CO2(g)+6H2(g) △H2=+174.1kJ/mol
请写出反应Ⅰ的热化学方程式:________ 。
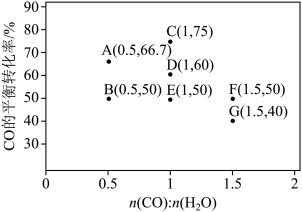
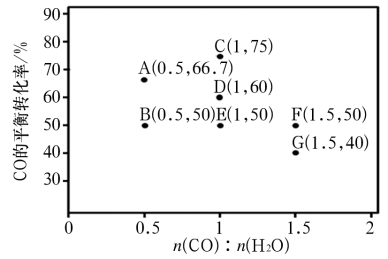
(2)反应Ⅱ,在进气比[n(CO):n(H2O)]不同时,测得相应的CO平衡转化率如图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)
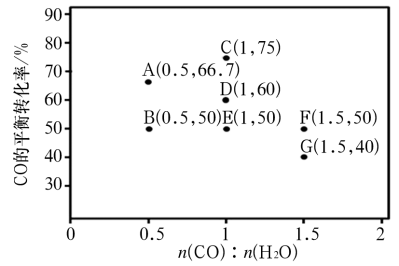
①若A、E和G三点对应的反应温度相同,则平衡常数KA=KE=KG=_______ (填数值)。在该温度下,要提高CO平衡转化率,除了改变进气比之外,还可采取的措施是:________ 。
②比较A、B两点对应的反应速率大小:vA_______ vB(填“<”“=”或“>”)。
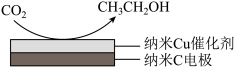
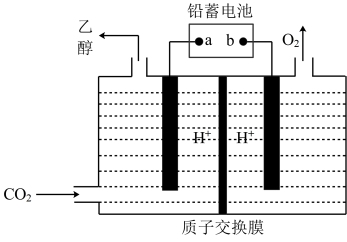
(3)以铅蓄电池为电源可将CO2转化为乙醇,其原理如图所示,电解所用电极材料均为惰性电极。该电解池阴极上的电极反应式为:_______ ;每生成0.5mol乙醇,理论上需消耗铅蓄电池中_______ mol硫酸。

(1)已知:CO(g)+H2O(g)
CH3CH2OH(g)+3H2O(g)
请写出反应Ⅰ的热化学方程式:
(2)反应Ⅱ,在进气比[n(CO):n(H2O)]不同时,测得相应的CO平衡转化率如图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)

①若A、E和G三点对应的反应温度相同,则平衡常数KA=KE=KG=
②比较A、B两点对应的反应速率大小:vA
(3)以铅蓄电池为电源可将CO2转化为乙醇,其原理如图所示,电解所用电极材料均为惰性电极。该电解池阴极上的电极反应式为:

21-22高二上·江苏南通·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


 CO2(g)+H2(g)
CO2(g)+H2(g)