解答题-原理综合题 较难0.4 引用1 组卷314
绿色能源是未来能源发展的重要方向,氢能是重要的绿色能源。
(1)氢气是一种环保的气体,不会污染大气且热值高。相关化学键的键能表示如表:
已知:H2O(g)=H2O(l)△H=-dkJ/mol,则氢气燃烧热的△H1=____ kJ/mol(用含a.、b、c、d的代数式表示)。
(2)催化制氢是目前大规模制取氢气的方法之一:CO(g)+H2O(g) CO2(g)+H2(g) △H2=-41.2kJ·mol-1;在T1℃时,将0.10molCO(g)与0.40molH2O(g)充入5L的容器中,反应平衡后H2的物质的量分数x(H2)=0.08。
CO2(g)+H2(g) △H2=-41.2kJ·mol-1;在T1℃时,将0.10molCO(g)与0.40molH2O(g)充入5L的容器中,反应平衡后H2的物质的量分数x(H2)=0.08。
①CO的平衡转化率α=____ %,反应平衡常数K=____ (结果保留2位有效数字)。
②保持容器容积不变,在反应初期,可以提高单位时间内CO转化率的措施有____ (填标号)。
A.增大水蒸气的浓度
B.通入“惰性气体”
C.升高温度
D.按原料起始比再通入0.10molCO(g)与0.40molH2O(g)
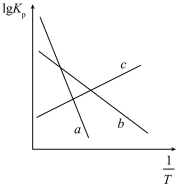
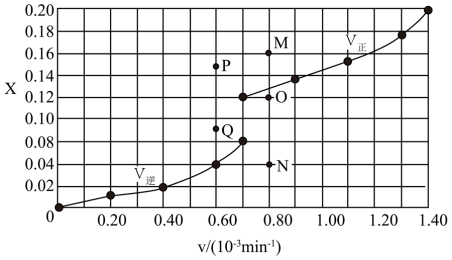
③由T1℃时上述实验数据计算得到v正~x(CO)和v逆~x(H2)的关系可用如图1表示。当升高到某一温度时,反应重新达到平衡后,相应的点分别为____ (填标号)。

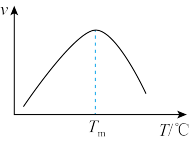
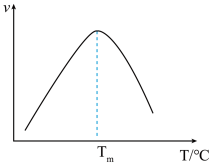
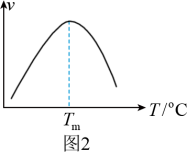
④研究表明,CO催化变换反应的速率方程为v=k[x(CO)·x(H2O)- ]式中x(CO)、x(H2O)、x(CO2)、x(H2)分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图2所示。温度升高时,CO催化变换反应的Kp
]式中x(CO)、x(H2O)、x(CO2)、x(H2)分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图2所示。温度升高时,CO催化变换反应的Kp____ (填“增大”或“减小”或“不变”)。根据速率方程分析,T>Tm时v逐渐减小的原因是____ 。
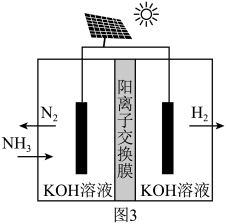
(3)氨电解法制氢气。利用电解原理,将氨转化为高纯氢气,其装置如图3所示。阳极的电极反应式为____ 。
(1)氢气是一种环保的气体,不会污染大气且热值高。相关化学键的键能表示如表:
| 化学键 | O=O | H—H | O—H |
| 键能E/(kJ·mol-1) | a | b | c |
已知:H2O(g)=H2O(l)△H=-dkJ/mol,则氢气燃烧热的△H1=
(2)催化制氢是目前大规模制取氢气的方法之一:CO(g)+H2O(g)
①CO的平衡转化率α=
②保持容器容积不变,在反应初期,可以提高单位时间内CO转化率的措施有
A.增大水蒸气的浓度
B.通入“惰性气体”
C.升高温度
D.按原料起始比再通入0.10molCO(g)与0.40molH2O(g)
③由T1℃时上述实验数据计算得到v正~x(CO)和v逆~x(H2)的关系可用如图1表示。当升高到某一温度时,反应重新达到平衡后,相应的点分别为

④研究表明,CO催化变换反应的速率方程为v=k[x(CO)·x(H2O)-

(3)氨电解法制氢气。利用电解原理,将氨转化为高纯氢气,其装置如图3所示。阳极的电极反应式为

2022·湖南长沙·一模
类题推荐
绿色能源是未来能源发展的重要方向,氢能是重要的绿色能源。
(1)氢气是一种环保的气体,不会污染大气且热值高。已知:H2O(g)=H2O(l) ΔH=-44 kJ·mol-1,相关化学键的键能表示如下:
表示氢气燃烧热的热化学方程式_______ 。
(2)催化制氢是目前大规模制取氢气的方法之一:CO(g)+H2O(g) CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1。在T1℃时,将0.10 mol CO与0.40 mol H2O充入5 L的容器中,反应平衡后CO的物质的量分数x(CO)=0.12。
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1。在T1℃时,将0.10 mol CO与0.40 mol H2O充入5 L的容器中,反应平衡后CO的物质的量分数x(CO)=0.12。_______ %。
②由T1℃时上述实验数据计算得到v正~x(CO)和v逆~x(H2)的关系可用图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为_______ (填字母)。
③研究表明,一氧化碳催化变换反应的速率方程为: ],Kp为平衡常数,k为反应的速率常数,在气体组成和催化剂一定的情况下,反应速率与温度变化的关系曲线如图所示。温度升高时,CO催化变换反应的Kp
],Kp为平衡常数,k为反应的速率常数,在气体组成和催化剂一定的情况下,反应速率与温度变化的关系曲线如图所示。温度升高时,CO催化变换反应的Kp_______ (填“增大”“减小”或“不变”),根据速率方程分析,T>Tm时,v逐渐减小的原因是_______ 。 CH4(g)+2H2O(g),在一定条件下该反应存在:v正(H2)=k1·c4(H2)·c(CO2),v逆(H2O)= k2·c2(H2O)·c(CH4),可知k1·c4(H2)·c(CO2)=k2·c2(H2O)·c(CH4),则该反应的平衡常数K=
CH4(g)+2H2O(g),在一定条件下该反应存在:v正(H2)=k1·c4(H2)·c(CO2),v逆(H2O)= k2·c2(H2O)·c(CH4),可知k1·c4(H2)·c(CO2)=k2·c2(H2O)·c(CH4),则该反应的平衡常数K=____ (用含k1,k2的代数式表示)。
(4)光催化H2O制H2技术也是研究热点。光催化材料还原H2O的机理如图所示,光照时,低能价带失去电子并产生空穴(h+,具有强氧化性)。在低能价带上,H2O直接转化为O2的电极反应式为_______ 。
(1)氢气是一种环保的气体,不会污染大气且热值高。已知:H2O(g)=H2O(l) ΔH=-44 kJ·mol-1,相关化学键的键能表示如下:
| 化学键 | O=O | H-H | O-H |
| 键能E/(kJ·mol-1) | 497 | 436 | 463 |
(2)催化制氢是目前大规模制取氢气的方法之一:CO(g)+H2O(g)

②由T1℃时上述实验数据计算得到v正~x(CO)和v逆~x(H2)的关系可用图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为
③研究表明,一氧化碳催化变换反应的速率方程为:

(4)光催化H2O制H2技术也是研究热点。光催化材料还原H2O的机理如图所示,光照时,低能价带失去电子并产生空穴(h+,具有强氧化性)。在低能价带上,H2O直接转化为O2的电极反应式为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网