解答题-工业流程题 适中0.65 引用1 组卷152
以镍铂靶材废料(含49.8%Pt、47.2%Ni,其余为等质量的Fe和Al)为原料制备海绵铂、硫酸镍晶体 ,流程如下:
,流程如下:
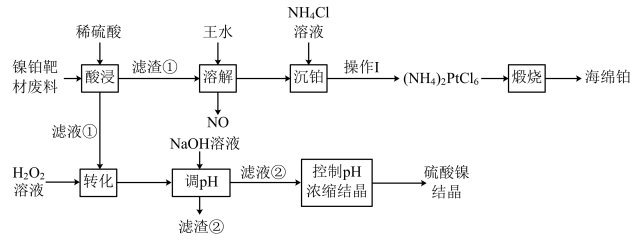
请回答下列问题:
(1) 的电子式为
的电子式为_______ , 中Pt的化合价为
中Pt的化合价为_______ 价。
(2)“酸浸”中加快反应速率的措施有_______ (答一条),“酸浸”会产生一种可燃气体,它是_______ (填化学式)。
(3)“溶解”时发生反应的化学方程式为_______ 。
(4)“滤液①”中含有的金属离子为_______ (填离子符号)。
(5)室温下“调pH”时,最先生成的沉淀是_______ (填化学式),“调pH”结束后,溶液中 ,此时溶液的pH最大为
,此时溶液的pH最大为_______ {已知室温下: ,
, ,
, }
}
(6)某工厂用1t该镍铂靶材废料进行上述工艺流程,最终制得硫酸镍晶体2135.6kg,则镍的损耗率为_______ 。

请回答下列问题:
(1)
(2)“酸浸”中加快反应速率的措施有
(3)“溶解”时发生反应的化学方程式为
(4)“滤液①”中含有的金属离子为
(5)室温下“调pH”时,最先生成的沉淀是
(6)某工厂用1t该镍铂靶材废料进行上述工艺流程,最终制得硫酸镍晶体2135.6kg,则镍的损耗率为
22-23高三上·河南·开学考试
类题推荐
利用某工业废料(主要成分为Co2O3,含有少量PbO、NiO、FeO)制备Co2O3和Ni(OH)2的流程如下。
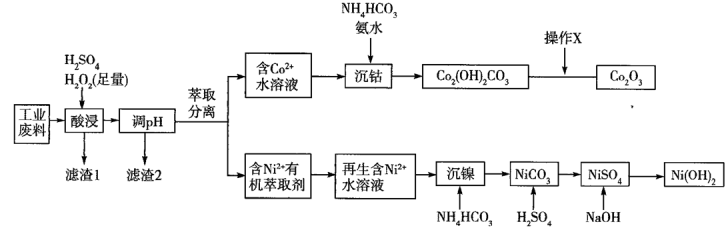
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如表。
回答下列问题:
(1)“酸浸”时为加快反应速率,可采取的措施是___________ (答两条)。
(2)“酸浸”时Co2O3和H2O2能发生氧化还原反应,该反应的离子方程式为___________ ;滤渣1的主要成分是___________ (填化学式)。
(3)“调pH”时,pH调节的最小值是___________ ;操作X是高温煅烧,如果在实验室中进行操作X,装Co2(OH)2CO3的仪器的名称是___________ 。
(4)“沉钴”时发生反应的离子方程式为___________ 。
(5)Ni(OH)2可用于制备镍氢电池,该电池充电时的总反应为Ni(OH)2+M=NiOOH+MH(M为储氢合金),电解液为KOH溶液,则放电时正极的电极反应式为___________ 。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如表。
| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Co(OH)2 | Ni(OH)2 |
| 完全沉淀时的pH | 9.7 | 3.7 | 9.0 | 9.2 |
(1)“酸浸”时为加快反应速率,可采取的措施是
(2)“酸浸”时Co2O3和H2O2能发生氧化还原反应,该反应的离子方程式为
(3)“调pH”时,pH调节的最小值是
(4)“沉钴”时发生反应的离子方程式为
(5)Ni(OH)2可用于制备镍氢电池,该电池充电时的总反应为Ni(OH)2+M=NiOOH+MH(M为储氢合金),电解液为KOH溶液,则放电时正极的电极反应式为
某油脂厂废弃的镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收镍制备硫酸镍晶体( )。
)。
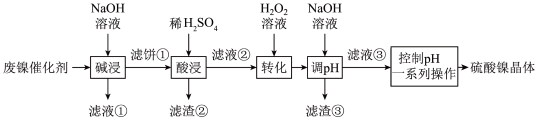
已知某些金属离子开始沉淀和沉淀完全的pH如下:
回答下列问题:
(1)提高“碱浸”速率有效措施有___________ (任写一种即可);“滤液②”中含有的金属离子有___________ 。
(2)写出“转化”中发生反应的离子方程式___________ 。
(3)若“转化”后溶液中 浓度为
浓度为 ,则“调pH”应控制的范围为
,则“调pH”应控制的范围为___________ 。
(4)获得硫酸镍晶体时,需经过控制pH、___________ 、___________ 、过滤等“一系列操作”。
(5)写出基态镍原子的电子排布式___________ ;基态铁原子的价电子排布式___________

已知某些金属离子开始沉淀和沉淀完全的pH如下:
金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
开始沉淀时(c=0.01mol·L-1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5mol·L-1)的 pH | 8.7 | 4.7 | 3.2 | 9.0 |
回答下列问题:
(1)提高“碱浸”速率有效措施有
(2)写出“转化”中发生反应的离子方程式
(3)若“转化”后溶液中
(4)获得硫酸镍晶体时,需经过控制pH、
(5)写出基态镍原子的电子排布式
三氧化二镍( )是重要的电子元件和蓄电池材料,工业上利用含镍废料(主要含Ni、Al、Fe的氧化物,
)是重要的电子元件和蓄电池材料,工业上利用含镍废料(主要含Ni、Al、Fe的氧化物, ,C等)制备
,C等)制备 的工艺流程如下所示:
的工艺流程如下所示:
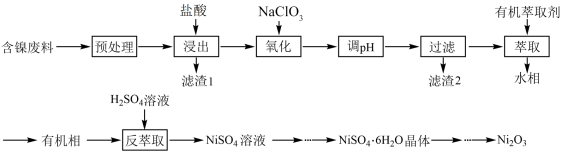
已知:①在该实验条件下 、Fe(Ⅲ)不能氧化Ni(Ⅱ)。
、Fe(Ⅲ)不能氧化Ni(Ⅱ)。
②常温下,溶液中 金属离子形成氢氧化物沉淀的pH如下表所示:
金属离子形成氢氧化物沉淀的pH如下表所示:
③萃取的原理为 。
。
回答下列问题:
(1)“预处理”时,可以用___________ (填化学式)溶液除去废料表面的油脂油污。
(2)“浸出”时,提高浸出效率可采取的措施有___________ (任写一种)。滤渣1的主要成分是___________ 。
(3)“氧化”时,加入 发生反应的离子方程式为
发生反应的离子方程式为___________ ,目的是___________ 。
(4)若常温下,“调pH”时,溶液中 浓度为
浓度为 ,为使
,为使 等杂质离子沉淀完全,则需控制溶液的pH范围是
等杂质离子沉淀完全,则需控制溶液的pH范围是___________ 。
(5)“萃取”时,操作若在实验室进行,需要用到的主要玻璃仪器有___________ 、烧杯。
(6)资料显示,硫酸镍结晶水合物的形态与温度有如下关系:
从 溶液获得稳定的
溶液获得稳定的 晶体的操作是:
晶体的操作是:___________ 。

已知:①在该实验条件下
②常温下,溶液中
| 离子 pH | ||||
| 开始沉淀pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 完全沉淀pH | 8.7 | … | 3.2 | 9.0 |
回答下列问题:
(1)“预处理”时,可以用
(2)“浸出”时,提高浸出效率可采取的措施有
(3)“氧化”时,加入
(4)若常温下,“调pH”时,溶液中
(5)“萃取”时,操作若在实验室进行,需要用到的主要玻璃仪器有
(6)资料显示,硫酸镍结晶水合物的形态与温度有如下关系:
| 温度 | 低于30.8℃ | 30.8~53.8℃ | 53.8~280℃ | 高于280℃ |
| 晶体形态 | 多种结晶水合物 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


