单选题 适中0.65 引用1 组卷52
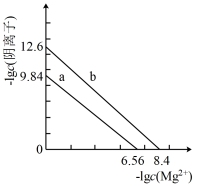
| A.Ksp[Mg3(AsO4)2]=10-19.68 |
| B.若Mg3(AsO4)2(s)+2 |
| C.向浓度相等的Na3AsO4、Na3PO4的废水中同时滴加相同浓度的Mg(NO3)2溶液, |
| D.要使废水中 |
21-22高二上·重庆巴南·阶段练习
类题推荐
完成下列问题。
(1)某温度下,纯水中的c(OH-)=1×10-6 mol/L,则此时c(H+)为_____ mol/L。若在温度不变时,往其中滴加盐酸使 c(H+)=1×10-4mol/L,则溶液中c(OH-)为_____ mol/L。若将此盐酸稀释 1 000 倍,则溶液的c(H+)约为______ mol/L。
(2)已知:Cu(OH)2(s) Cu2+(aq)+2OH-(aq),Ksp=2×10-20。
Cu2+(aq)+2OH-(aq),Ksp=2×10-20。
①某CuSO4溶液里c(Cu2+)=0.02 mol·L-1,如果要使其生成 Cu(OH)2沉淀,应调整溶液的pH,使之大于_____ 。
②要使0.2 mol·L-1CuSO4溶液中的Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为_____ 。
(3)重金属离子会对河流和海洋造成严重污染。某化工厂废水(pH=2.0)中含有Ag+、Pb2+等重金属离子,其浓度约为0.01 mol/L,排放前拟用沉淀法除去这两种离子,查找有关数据如下:
①你认为往废水中加入_____ (填字母),沉淀效果最好。
A.NaOH B.Na2S C.KI D.Ca(OH)2
②如果用生石灰处理上述废水,使溶液的pH=8,处理后废水中c(Pb2+)=_____ 。
(1)某温度下,纯水中的c(OH-)=1×10-6 mol/L,则此时c(H+)为
(2)已知:Cu(OH)2(s)
①某CuSO4溶液里c(Cu2+)=0.02 mol·L-1,如果要使其生成 Cu(OH)2沉淀,应调整溶液的pH,使之大于
②要使0.2 mol·L-1CuSO4溶液中的Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为
(3)重金属离子会对河流和海洋造成严重污染。某化工厂废水(pH=2.0)中含有Ag+、Pb2+等重金属离子,其浓度约为0.01 mol/L,排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S |
| Ksp | 8.3×10-12 | 5.6×10-8 | 6.3×10-50 |
| 难溶电解质 | PbI2 | Pb(OH)2 | PbS |
| Ksp | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
A.NaOH B.Na2S C.KI D.Ca(OH)2
②如果用生石灰处理上述废水,使溶液的pH=8,处理后废水中c(Pb2+)=
弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
Ⅰ.已知H2A在水中存在以下平衡:H2A=H++HA-,HA- H++A2-。
H++A2-。
(1)常温下NaHA溶液的pH_______(填序号)
(2)某温度下,若向0.1mol·L-1的NaHA溶液中逐滴滴加0.1mol·L-1KOH溶液至溶液呈中性(忽略混合后溶液的体积变化)。此时该混合溶液中的下列关系一定正确的是_______
(3)已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s) Ca2+(aq)+A2- ΔH>0。若要使该溶液中Ca2+浓度变小,可采取的措施有 _______
Ca2+(aq)+A2- ΔH>0。若要使该溶液中Ca2+浓度变小,可采取的措施有 _______
Ⅱ.含Cr2O 的废水毒性较大,某工厂废水中含5.0×10-3mol·L-1的Cr2O
的废水毒性较大,某工厂废水中含5.0×10-3mol·L-1的Cr2O 。为了使废水的排放达标,进行如下处理:Cr2O
。为了使废水的排放达标,进行如下处理:Cr2O
 Cr3+、Fe3+
Cr3+、Fe3+ Cr(OH)3、Fe(OH)3。
Cr(OH)3、Fe(OH)3。
(4)若处理后的废水中残留的c(Fe3+)=2.0×10-13mol·L-1,则残留的Cr3+的浓度为_______ ;(已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)
(5)已知室温时,Ksp[Mg(OH)2]=4.0×10-11。在0.1mol·L-1的MgCl2溶液中,逐滴加入NaOH溶液,当Mg2+完全沉淀时,溶液的pH是_______ 。(已知lg2=0.3)
Ⅰ.已知H2A在水中存在以下平衡:H2A=H++HA-,HA-
(1)常温下NaHA溶液的pH_______(填序号)
| A.大于7 |
| B.小于7 |
| C.等于7 |
| D.无法确定 |
| A.c(H+)·c(OH-)=1.0×10-14 |
| B.c(Na+)+c(K+)=c(HA-)+2c(A2-) |
| C.c(Na+)>c(K+) |
| D.c(Na+)+c(K+)=0.05mol·L-1 |
| A.升高温度 |
| B.降低温度 |
| C.加入NH4Cl晶体 |
| D.加入Na2A固体 |
Ⅱ.含Cr2O
(4)若处理后的废水中残留的c(Fe3+)=2.0×10-13mol·L-1,则残留的Cr3+的浓度为
(5)已知室温时,Ksp[Mg(OH)2]=4.0×10-11。在0.1mol·L-1的MgCl2溶液中,逐滴加入NaOH溶液,当Mg2+完全沉淀时,溶液的pH是
(1)已知某溶液中只有Na+、CH3COO−、H+、OH−四种离子。某同学推测该溶液中离子浓度可能有如下四种关系:
A.c(Na+)>c(CH3COO−)>c(OH−)>c(H+) B.c(Na+)>c(CH3COO−)>c(H+)>c(OH−)
C.c(Na+)>c(OH−)>c(CH3COO−)>c(H+) D.c(CH3COO−)>c(Na+)>c(H+)>c(OH−)
①若溶液中只溶解了一种溶质,该溶质的名称是_________ ,上述离子浓度大小关系中正确的是(填序号)_____ 。
②若上述关系中D是正确的,则溶液中溶质的化学式是________ 。
③若该溶液由体积相等的醋酸与NaOH溶液混合而成,且溶液恰好呈中性,则混合前c(CH3COOH)(填“>”“<”“=”,下同)___________ c(NaOH),混合后c(CH3COO−)与c(Na+)的关系是c(CH3COO−)__________ c(Na+)。
(2)Na2S可用于制造硫化染料、沉淀水体中的重金属等。
①Na2S溶液中S2−水解的离子方程式为____________________________________ 。
②室温时,几种重金属离子的硫化物的溶度积常数如下表:
则:向物质的量浓度相同的Fe2+、Pb2+、Cu2+、Hg2+的混合稀溶液中,逐滴加入Na2S稀溶液,首先沉淀的离子是____ ;用Na2S溶液沉淀废水中Pb2+,为使Pb2+沉淀完全[c(Pb2+)≤1×10−6mol/L],则应满足溶液中c(S2−)≥_____ mol/L;反应Cu2+(aq)+FeS(s)  Fe2+(aq)+CuS(s)的平衡常数K=
Fe2+(aq)+CuS(s)的平衡常数K=_______ 。
A.c(Na+)>c(CH3COO−)>c(OH−)>c(H+) B.c(Na+)>c(CH3COO−)>c(H+)>c(OH−)
C.c(Na+)>c(OH−)>c(CH3COO−)>c(H+) D.c(CH3COO−)>c(Na+)>c(H+)>c(OH−)
①若溶液中只溶解了一种溶质,该溶质的名称是
②若上述关系中D是正确的,则溶液中溶质的化学式是
③若该溶液由体积相等的醋酸与NaOH溶液混合而成,且溶液恰好呈中性,则混合前c(CH3COOH)(填“>”“<”“=”,下同)
(2)Na2S可用于制造硫化染料、沉淀水体中的重金属等。
①Na2S溶液中S2−水解的离子方程式为
| 金属硫化物 | FeS | PbS | CuS | HgS |
| Ksp | 6.3×10−18 | 1.0×10−28 | 6.3×10−36 | 1.6×10−52 |
②室温时,几种重金属离子的硫化物的溶度积常数如下表:
则:向物质的量浓度相同的Fe2+、Pb2+、Cu2+、Hg2+的混合稀溶液中,逐滴加入Na2S稀溶液,首先沉淀的离子是
 Fe2+(aq)+CuS(s)的平衡常数K=
Fe2+(aq)+CuS(s)的平衡常数K=组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


