解答题-实验探究题 较难0.4 引用1 组卷131
某学习小组拟研究FeSO4的分解实验探究,请你利用所学知识帮该小组完成以下实验方案。
[实验目的]探究FeSO4分解产物与温度关系。
[提出假设]
假设1:Fe2O3、SO3、SO2;假设2:FeO、SO3、SO2;假设3:Fe3O4、SO3、SO2。
[查阅资料]几种物质的物理性质如表所示。
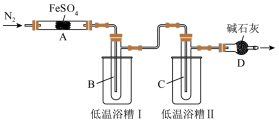
回答下列问题:
(1)根据所学知识判断,假设2肯定不成立,理由是_______ 。
(2)实验过程中,在检查装置气密性之后点燃A处酒精灯之前的操作是_______ ,(只填操作),当A处固体完全分解后通入N2的目的是_______ 。
(3)低温浴槽I收集的物质是_______ (填化学式),低温浴槽II控制的温度范围为_______ 。
(4)甲、乙组分别进行实验,实验数据如下(不考虑损失,固体已完全分解且固体产物为纯净物):
甲组实验中A装置得到固体产物是_______ (填化学式)。
(5)为进一步确认固体产物成分,取乙组实验得到的固体溶于稀硫酸,将溶液分成两份,进行如下实验:在一份溶液中滴加铁氰化钾K3[Fe(CN)6]溶液,产生蓝色沉淀。在另一份溶液中滴加NH4SCN溶液,观察到的现象是_______ 。
[实验结论]通过上述实验,FeSO4分解产物与温度有关。
[交流反思]FeSO4分解反应中是否有O2生成?
(6)为验证实验猜想,他们设计两种方案检验O2:
方案1:将D管导出的气体通入酸化的淀粉-KI溶液中。
方案2:用带火星的木条放在D管口处。
假设过程中持续缓缓通入N2,对比以上两种方案,其中方案_______ (填“1”或“2”)可行。
[实验目的]探究FeSO4分解产物与温度关系。
[提出假设]
假设1:Fe2O3、SO3、SO2;假设2:FeO、SO3、SO2;假设3:Fe3O4、SO3、SO2。
[查阅资料]几种物质的物理性质如表所示。
| 物质 | SO3 | SO2 | O2 | N2 |
| 熔点/℃ | 16.8 | -72.4 | -218.4 | -209.9 |
| 沸点/℃ | 44.8 | -10 | -182.9 | -195.8 |

回答下列问题:
(1)根据所学知识判断,假设2肯定不成立,理由是
(2)实验过程中,在检查装置气密性之后点燃A处酒精灯之前的操作是
(3)低温浴槽I收集的物质是
(4)甲、乙组分别进行实验,实验数据如下(不考虑损失,固体已完全分解且固体产物为纯净物):
| 实验 | A处温度/℃ | FeSO4质量/g | 低温浴槽I净增质量/g | 低温浴槽II净增质量/g |
| 甲 | T1 | 3.04 | 0.80 | 0.64 |
| 乙 | T2 | 4.56 | 1.60 | 0.64 |
(5)为进一步确认固体产物成分,取乙组实验得到的固体溶于稀硫酸,将溶液分成两份,进行如下实验:在一份溶液中滴加铁氰化钾K3[Fe(CN)6]溶液,产生蓝色沉淀。在另一份溶液中滴加NH4SCN溶液,观察到的现象是
[实验结论]通过上述实验,FeSO4分解产物与温度有关。
[交流反思]FeSO4分解反应中是否有O2生成?
(6)为验证实验猜想,他们设计两种方案检验O2:
方案1:将D管导出的气体通入酸化的淀粉-KI溶液中。
方案2:用带火星的木条放在D管口处。
假设过程中持续缓缓通入N2,对比以上两种方案,其中方案
21-22高二下·江西宜春·期末
类题推荐
某实验小组拟探究铁的化合物(FeS2O6)的分解产物,设计如下实验。已知几种物质的物理性质如表所示。
实验装置如图所示(加热和夹持装置省略)。
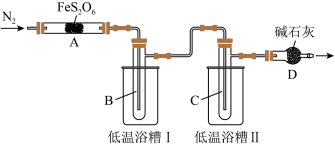
回答下列问题:
(1)点燃酒精灯之前,通入一段时间N2,其目的是________ 。
(2)低温浴槽II控制的温度范围为________ 。
(3)甲、乙、丙三组分别进行实验,测得相关实验数据如表(不考虑损失且不考虑生成O2,FeS2O6在该温度下完全反应):
①根据实验数据分析,甲组实验中A装置得到的纯净固体产物是_______ (填化学式)。
②经检测,乙组实验的固体产物为纯净物,写出A中发生的化学反应方程式:_______ 。
(4)为了进一步分析丙组实验得到的固体纯净物成分,他们取少量固体溶于稀硫酸中,将溶液分成两份,进行如表实验(不考虑O2的存在):
根据实验推知,丙组实验中FeS2O6分解生成的固体产物、SO3、SO2的物质的量之比为_______ 。
(5)为了进一步探究气体产物成分,将D仪器导出的气体通入酸化的KI-淀粉溶液中,一段时间后,若_______  填实验现象
填实验现象 ,则说明有O2生成。
,则说明有O2生成。
(6)将I中产物1100g溶于900g98%的浓硫酸所得产物为_______ ,其质量分数为_______ 。
| 物质 | SO3 | SO2 | O2 |
| 熔点/℃ | 16.8 | -75.5 | -218.4 |
| 沸点/℃ | 44.8 | -10 | -182.9 |

回答下列问题:
(1)点燃酒精灯之前,通入一段时间N2,其目的是
(2)低温浴槽II控制的温度范围为
(3)甲、乙、丙三组分别进行实验,测得相关实验数据如表(不考虑损失且不考虑生成O2,FeS2O6在该温度下完全反应):
| A处温度/℃ | FeS2O6质量/g | 低温浴槽I净增质量/g | 低温浴槽II净增质量/g | |
| 甲 | T1 | 2.16 | 0 | 0.64 |
| 乙 | T2 | 4.32 | 0.80 | 1.92 |
| 丙 | T3 | 6.48 | 1.60 | 2.56 |
②经检测,乙组实验的固体产物为纯净物,写出A中发生的化学反应方程式:
(4)为了进一步分析丙组实验得到的固体纯净物成分,他们取少量固体溶于稀硫酸中,将溶液分成两份,进行如表实验(不考虑O2的存在):
| 实验 | 操作 | 现象 |
| a | 在一份溶液中滴加K3[Fe(CN)6]溶液 | 产生蓝色沉淀 |
| b | 在另一份溶液中滴加NH4SCN溶液 | 溶液变红色 |
(5)为了进一步探究气体产物成分,将D仪器导出的气体通入酸化的KI-淀粉溶液中,一段时间后,若
(6)将I中产物1100g溶于900g98%的浓硫酸所得产物为
某实验小组拟探究铁的化合物(FeS2O6)的分解产物,设计如下实验。已知几种物质的物理性质如下表所示。
实验装置如图所示(加热和夹持装置省略)。
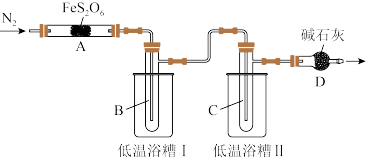
回答下列问题:
(1)仪器D的名称是_______ 。
(2)点燃酒精灯之前,通入一段时间N2,其目的是_______ 。
(3)低温浴槽II控制的温度范围为_______ 。
(4)甲、乙、丙三组分别进行实验,测得相关实验数据如下(不考虑损失且不考虑O2的存在,固体已完全分解):
①根据实验数据分析,甲组实验中A装置得到的纯净固体产物是_______ (填化学式)。
②经检测,乙组实验的固体产物为纯净物,写出A中发生的化学反应方程式:_______ 。
(5)为了进一步分析丙组实验得到的固体纯净物成分,他们取少量固体溶于稀硫酸中,将溶液分成两份,进行如下实验(不考虑O2的存在):
根据实验推知,丙组实验中FeS2O6分解生成的固体产物、SO3、SO2的物质的量之比为_______ 。
(6)为了进一步探究气体产物成分,将D仪器导出的气体通入酸化的KI-淀粉溶液中,一段时间后,若_______ (填实验现象),则说明有O2生成。
| 物质 | SO3 | SO2 | O2 |
| 熔点/°C | 16.8 | -75.5 | 218.4 |
| 沸点/°C | 44.8 | -10 | -182.9 |

回答下列问题:
(1)仪器D的名称是
(2)点燃酒精灯之前,通入一段时间N2,其目的是
(3)低温浴槽II控制的温度范围为
(4)甲、乙、丙三组分别进行实验,测得相关实验数据如下(不考虑损失且不考虑O2的存在,固体已完全分解):
| A处温度/°C | FeS2O6质量/g | 低温浴槽I净增质量/g | 低温浴槽II净增质量/g | |
| 甲 | T1 | 2.16 | 0 | 0.64 |
| 乙 | T2 | 4.32 | 0.80 | 1.92 |
| 丙 | T3 | 6.48 | 1.60 | 2.56 |
②经检测,乙组实验的固体产物为纯净物,写出A中发生的化学反应方程式:
(5)为了进一步分析丙组实验得到的固体纯净物成分,他们取少量固体溶于稀硫酸中,将溶液分成两份,进行如下实验(不考虑O2的存在):
| 实验 | 操作 | 现象 |
| a | 在一份溶液中滴加K3[Fe(CN)6]溶液 | 产生蓝色沉淀 |
| b | 在另一份溶液中滴加NH4SCN溶液 | 溶液变红色 |
(6)为了进一步探究气体产物成分,将D仪器导出的气体通入酸化的KI-淀粉溶液中,一段时间后,若
某实验小组拟探究过氧硫酸亚铁(FeS2O6)的分解产物,设计如下实验。已知几种物质的物理性质如表所示。
实验装置如图所示(加热装置省略)。
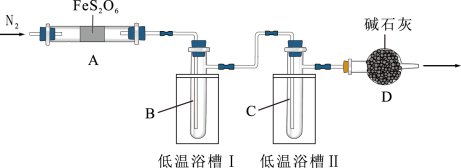
已知:低温浴槽Ⅰ收集的是SO3,低温浴槽Ⅱ收集的是SO2。
回答下列问题:
(1)仪器D的名称是____ 。
(2)点燃酒精灯之前,需先通入一段时间N2,其目的是____ 。
(3)低温浴槽Ⅰ控制的温度范围为____ 。
(4)甲、乙、丙三组分别进行实验,测得相关实验数据如表(不考虑损失,固体已完全分解且产物中不含O2):
①根据实验数据分析,甲组实验中装置A得到的纯净固体产物是____ (填化学式)。
②经检测,乙组实验得到的固体产物为纯净物,则装置A中发生反应的化学方程式为____ 。
(5)为了进一步分析丙组实验得到的固体成分,他们取少量该固体溶于稀硫酸中,将溶液分成两份,进行如表实验:
①____ 。
②____ 。
③若该固体为纯净物,则该固体的化学式为____ 。
| 物质 | SO3 | SO2 | O2 |
| 熔点/℃ | 16.8 | -72.4 | -218.4 |
| 沸点/℃ | 44.8 | -10 | -182.9 |

已知:低温浴槽Ⅰ收集的是SO3,低温浴槽Ⅱ收集的是SO2。
回答下列问题:
(1)仪器D的名称是
(2)点燃酒精灯之前,需先通入一段时间N2,其目的是
(3)低温浴槽Ⅰ控制的温度范围为
(4)甲、乙、丙三组分别进行实验,测得相关实验数据如表(不考虑损失,固体已完全分解且产物中不含O2):
| A处温度/℃ | FeS2O6的质量/g | 低温浴槽Ⅰ处净增质量/g | 低温浴槽Ⅱ处净增质量/g | |
| 甲 | T1 | 2.16 | 0 | 0.64 |
| 乙 | T2 | 4.32 | 0.80 | 1.92 |
| 丙 | T3 | 6.48 | 1.60 | 2.56 |
②经检测,乙组实验得到的固体产物为纯净物,则装置A中发生反应的化学方程式为
(5)为了进一步分析丙组实验得到的固体成分,他们取少量该固体溶于稀硫酸中,将溶液分成两份,进行如表实验:
| 实验 | 操作 | 现象 |
| a | 在一份溶液中滴加铁氰化钾{K3[Fe(CN)6]}溶液 | ① |
| b | 在另一份溶液中滴加NH4SCN溶液 | ② |
②
③若该固体为纯净物,则该固体的化学式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


