解答题-原理综合题 适中0.65 引用1 组卷107
I.请回答下列问题:把A、B、C、D四种金属按表中装置进行实验。
(1)根据表中信息判断四种金属活动性由大到小的顺序是_______ ;写出装置乙中正极的电极反应式:_______ 。
(2)若甲池中电极A为Zn、电极B为Cu、该装置工作时, 向
向_______ (填“A”或“B”极移动,经过一段时间后,若导线中转移了0.4mol电子,则产生的气体在标准状况下的体积为_______ L。如果该反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,该同学在烧杯中分别加入等体积的下列液体,你认为可行的是_______ (填字母)。
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.KNO3溶液
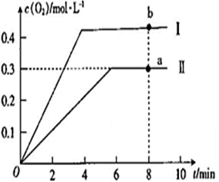
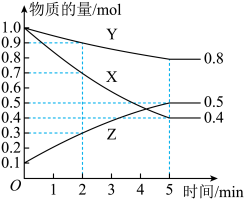
II.某温度时,在2L恒容密闭容器中,发生反应2M(g)+N(g) 2R(g),A、B气体的物质的量随时间变化的曲线如图,回答下列问题:
2R(g),A、B气体的物质的量随时间变化的曲线如图,回答下列问题:
(3)B为_______ (填“M”“N”或“R”)。
(4)Q点时,正、逆反应速率的大小关系为
_______ (填“>”“<”或“=”) 。
。
(5) 内,该反应的平均反应速率
内,该反应的平均反应速率
_______  。
。
(6)平衡时N的转化率为_______
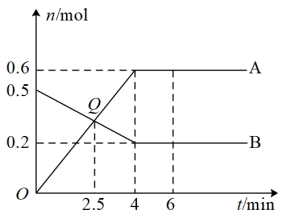
(7)在某绝热恒容密闭反应器中入2molM、1molN,发生反应2M(g)+N(g) 2R(g),反应速率随时间的变化的曲线如图。
2R(g),反应速率随时间的变化的曲线如图。

①由图可推知,该反应是_______ (填“吸热”或“放热”)反应。
②t2后反应速率降低的原因是_______ 。
| 装置 | 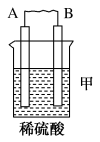 | 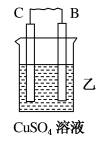 | 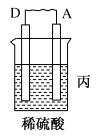 |
| 电子从A到B | C电极的质量增加 | 二价金属D不断溶解 |
(2)若甲池中电极A为Zn、电极B为Cu、该装置工作时,
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.KNO3溶液
II.某温度时,在2L恒容密闭容器中,发生反应2M(g)+N(g)

(3)B为
(4)Q点时,正、逆反应速率的大小关系为
(5)
(6)平衡时N的转化率为
(7)在某绝热恒容密闭反应器中入2molM、1molN,发生反应2M(g)+N(g)

①由图可推知,该反应是
②t2后反应速率降低的原因是
21-22高一下·新疆塔城·期末
类题推荐
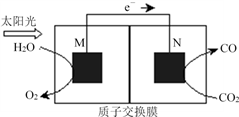
CO2和CO可作为工业合成甲醇(CH3OH)的直接碳源,还可利用CO2据电化学原理制备塑料,既减少工业生产对乙烯的依赖,又达到减少CO2排放的目的。
(1)利用CO2和H2反应合成甲醇的原理为:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。上述反应常用CuO和ZnO的混合物作催化剂。相同的温度和时间段内,催化剂中CuO的质量分数对CO2的转化率和CH3OH的产率影响的实验数据如下表所示:
由表可知,CuO的质量分数为_______ 催化效果最佳。
(2)利用CO和H2在一定条件下可合成甲醇,发生如下反应:CO(g)+2H2(g)⇌CH3OH(g),其两种反应过程中能量的变化曲线如下图a、b所示,下列说法正确的是_______
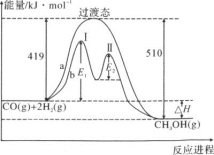
A.上述反应的ΔH=-91kJ·mol-1
B.a反应正反应的活化能为510kJ·mol-1
C.b过程中第I阶段为吸热反应,第II阶段为放热反应
D.b过程使用催化剂后降低了反应的活化能和ΔH
E.b过程的反应速率:第II阶段>第I阶段
(3)①在密闭容器中按物质的量之比1︰2充入CO和H2发生反应CO(g)+2H2(g)⇌CH3OH(g),【已知:v正=k1·p(CO)·p2(H2),v逆=k2·p(CH3OH)】,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图1所示,则压强P2___ P1(填“>”、“<”或“=”);在c点时,k1/k2=___ ;A、B、C三点KC的大小关系为___ ;300℃时进行该反应,若平衡时p(H2)=mKPa,则n(CH3OH):n(CO)=__ 。
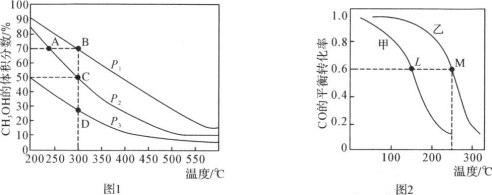
②甲和乙两个恒容密闭容器的体积相同,向甲中加入1molCO和2molH2,向乙中加入2molCO和4molH2,测得不同温度下CO的平衡转化率如图2所示,则L、M两点容器内压强:P(M)__ 2P(L);
(1)利用CO2和H2反应合成甲醇的原理为:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。上述反应常用CuO和ZnO的混合物作催化剂。相同的温度和时间段内,催化剂中CuO的质量分数对CO2的转化率和CH3OH的产率影响的实验数据如下表所示:
| ω(CuO)/% | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| CH3OH的产率 | 25% | 30% | 35% | 45% | 50% | 65% | 55% | 53% | 50% |
| CO2的转化率 | 10% | 13% | 15% | 20% | 35% | 45% | 40% | 35% | 30% |
由表可知,CuO的质量分数为
(2)利用CO和H2在一定条件下可合成甲醇,发生如下反应:CO(g)+2H2(g)⇌CH3OH(g),其两种反应过程中能量的变化曲线如下图a、b所示,下列说法正确的是

A.上述反应的ΔH=-91kJ·mol-1
B.a反应正反应的活化能为510kJ·mol-1
C.b过程中第I阶段为吸热反应,第II阶段为放热反应
D.b过程使用催化剂后降低了反应的活化能和ΔH
E.b过程的反应速率:第II阶段>第I阶段
(3)①在密闭容器中按物质的量之比1︰2充入CO和H2发生反应CO(g)+2H2(g)⇌CH3OH(g),【已知:v正=k1·p(CO)·p2(H2),v逆=k2·p(CH3OH)】,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图1所示,则压强P2

②甲和乙两个恒容密闭容器的体积相同,向甲中加入1molCO和2molH2,向乙中加入2molCO和4molH2,测得不同温度下CO的平衡转化率如图2所示,则L、M两点容器内压强:P(M)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网