解答题-结构与性质 适中0.65 引用1 组卷186
配位化合物在生产生活中有重要应用,请根据要求回答下列问题:
(1)基态镍原子的价电子排布式为_______ 。
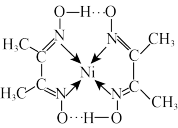
(2) 可以形成多种配离子,如[Ni(NH3)4]2+、[Ni(CN)4]2-、丁二酮肟镍分子(见图)等。
可以形成多种配离子,如[Ni(NH3)4]2+、[Ni(CN)4]2-、丁二酮肟镍分子(见图)等。
①1 mol[Ni(NH3)4]2+中含有_______ molσ键。
②[Ni(NH3)4]2+中H—N—H键角比NH3分子中H—N—H键角_______ (填“大”或“小”)。
③丁二酮肟镍分子内含有的作用力有_______ (填字母)。
a.配位键 b.离子键 c.氢键 d.范德华力
(3)光谱证实单质铝与强碱性溶液反应有[Al(OH)4]-生成,则Al(OH)4]-中存在_______ (填序号)
a.共价键 b.非极性键 c.配位键 d. 键 e. π键
键 e. π键
(4)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物的溶液中加BaCl2溶液时,则无明显现象。则第一种配合物的结构式可表示为_______ ,第二种配合物的结构式可表示为_______ 。若在第二种配合物的溶液中滴加AgNO3溶液,则产生的现象是_______ 。
(5)关于[Ti(NH3)5Cl]Cl2的说法中错误的是_______ 。
A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol[Ti(NH3)5Cl]Cl2的水溶液中加入足量AgNO3溶液,产生3mol白色沉淀
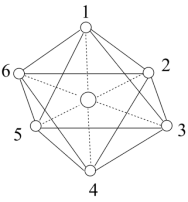
(6)已知[Co(NH3)6]3+的立体结构如图,其中1~6处的小圆圈表示NH3分子,且各相邻的NH3分子间的距离相等(图中虚线长度相等)。Co3+位于八面体的中心,若其中两个NH3被Cl-取代,所形成的[Co(NH3)4Cl2]+的结构的数目为_______ 。
(1)基态镍原子的价电子排布式为
(2)

①1 mol[Ni(NH3)4]2+中含有
②[Ni(NH3)4]2+中H—N—H键角比NH3分子中H—N—H键角
③丁二酮肟镍分子内含有的作用力有
a.配位键 b.离子键 c.氢键 d.范德华力
(3)光谱证实单质铝与强碱性溶液反应有[Al(OH)4]-生成,则Al(OH)4]-中存在
a.共价键 b.非极性键 c.配位键 d.
(4)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物的溶液中加BaCl2溶液时,则无明显现象。则第一种配合物的结构式可表示为
(5)关于[Ti(NH3)5Cl]Cl2的说法中错误的是
A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol[Ti(NH3)5Cl]Cl2的水溶液中加入足量AgNO3溶液,产生3mol白色沉淀
(6)已知[Co(NH3)6]3+的立体结构如图,其中1~6处的小圆圈表示NH3分子,且各相邻的NH3分子间的距离相等(图中虚线长度相等)。Co3+位于八面体的中心,若其中两个NH3被Cl-取代,所形成的[Co(NH3)4Cl2]+的结构的数目为

21-22高二下·福建莆田·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网







