解答题-实验探究题 适中0.65 引用2 组卷308
某小组同学探究影响 分解反应速率的因素。
分解反应速率的因素。
(1)在 作催化剂的条件下,
作催化剂的条件下, 发生分解反应的化学方程式为
发生分解反应的化学方程式为___________ 。
【实验方案】
(2)对比实验①和实验②,目的是探究___________ 对 分解反应速率的影响。
分解反应速率的影响。
(3)对比实验②和实验③,目的是探究 溶液的浓度对
溶液的浓度对 分解反应速率的影响,则实验③中x是
分解反应速率的影响,则实验③中x是___________ (填字母 )。
a.15 b.30
【实验过程及分析】在恒温恒容的密闭容器中完成以上实验,测量反应过程中容器内的气体压强随时间的变化,实验数据如下图所示。
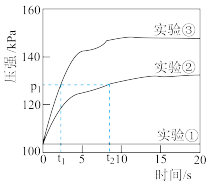
(4)上述实验方案中, 分解反应速率最快的是
分解反应速率最快的是___________ (填序号 )。
(5)能证明 溶液的浓度对
溶液的浓度对 分解反应速率有影响的证据是
分解反应速率有影响的证据是___________ 。
(1)在
【实验方案】
| 实验编号 | 蒸馏水 | 催化剂 | 温度/℃ | ||
| V/mL | V/mL | ||||
| ① | 3 | 10 | 20 | 无催化剂 | 20 |
| ② | 3 | 10 | 20 | 20 | |
| ③ | 3 | 15 | x | 20 | |
(3)对比实验②和实验③,目的是探究
a.15 b.30
【实验过程及分析】在恒温恒容的密闭容器中完成以上实验,测量反应过程中容器内的气体压强随时间的变化,实验数据如下图所示。

(4)上述实验方案中,
(5)能证明
21-22高一下·北京海淀·期末
类题推荐
某实验小组探究浓度、温度及催化剂对 分解速率的影响。回答下列问题:
分解速率的影响。回答下列问题:
(1)实验室可用过氧化钠固体与稀硫酸反应(温度不高于15℃)制取少量20% ,写出该反应的化学方程式:
,写出该反应的化学方程式:___________ 。
(2)将上述制得的 进行实验:其中实验I与实验II是为了探究浓度对
进行实验:其中实验I与实验II是为了探究浓度对 分解反应速率的影响,实验I与实验II是为了探究温度对
分解反应速率的影响,实验I与实验II是为了探究温度对 分解反应速率的影响。
分解反应速率的影响。
填写表中缺少的内容:①___________ ,②___________ ,③___________ 。
(3)探究 ,
, 对
对 分解反应速率影响的实验设计如图所示。有同学对该实验设计提出疑问,认为不能比较
分解反应速率影响的实验设计如图所示。有同学对该实验设计提出疑问,认为不能比较 ,
, 对
对 分解反应速率的影响,提出的疑问是
分解反应速率的影响,提出的疑问是___________ ,改进办法是___________ ,改进后,判断 ,
, 对
对 分解反应速率影响的依据是
分解反应速率影响的依据是___________ (填实验现象)。

(1)实验室可用过氧化钠固体与稀硫酸反应(温度不高于15℃)制取少量20%
(2)将上述制得的
| 实验编号 | 温度/℃ | 水的体积/ mL | ||
| 质量分数 | 体积/mL | |||
| I | 20% | 5.0 | 30 | 10.0 |
| II | 20% | ① | 30 | 5.0 |
| III | ② | ③ | 40 | 10.0 |
(3)探究

I.在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
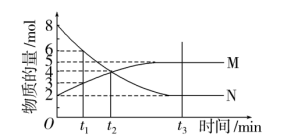
(1)比较 时刻,正逆反应速率大小
时刻,正逆反应速率大小
___________  。(填“>”“=”或“<”)
。(填“>”“=”或“<”)
(2)若 ,计算反应开始至
,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率___________ 。
(3) 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为___________ 。
(4)如果升高温度,则
___________ (填“增大”“减小”或“不变”)。
II.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
(5)①本实验待测数据可以是___________ ,实验Ⅰ和实验Ⅱ可以探究___________ 对锌与稀硫酸反应速率的影响。
②实验Ⅲ和实验Ⅳ的目的是___________ 。
(6)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中
___________ 。

(1)比较
(2)若
(3)
(4)如果升高温度,则
II.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
| 序号 | 纯锌粉/g | 温度/℃ | 硫酸铜固体/g | 加入蒸馏水/mL | |
| Ⅰ | 2.0 | 50.0 | 25 | 0 | 0 |
| Ⅱ | 2.0 | 40.0 | 25 | 0 | 10.0 |
| Ⅲ | 2.0 | 50.0 | 25 | 0.2 | 0 |
| Ⅳ | 2.0 | 50.0 | 25 | 4.0 | 0 |
②实验Ⅲ和实验Ⅳ的目的是
(6)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验序号 | 体积V/mL | ||||
| 水 | KI溶液 | 淀粉溶液 | |||
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 | 4.0 | 4.0 | 2.0 | |
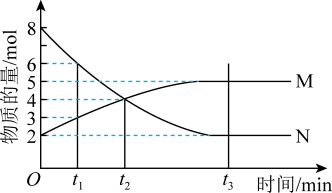
Ⅰ.在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图: 时刻,正逆反应速率大小
时刻,正逆反应速率大小
___________  。(填“>”“=”或“<”)
。(填“>”“=”或“<”)
(2)若 min,计算反应开始至
min,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率___________ 。
(3) 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为___________ 。
(4)写出反应的化学方程式___________ 。
(5)如果升高温度,则
___________ (填“增大”“减小”或“不变”)。
Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
(6)①本实验待测数据可以是___________ ,实验Ⅰ和实验Ⅱ可以探究___________ ,对锌与稀硫酸反应速率的影响。
②实验Ⅲ和实验Ⅳ的目的是___________ 。
(7)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中
___________ 。
(2)若
(3)
(4)写出反应的化学方程式
(5)如果升高温度,则
Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
| 序号 | 纯锌粉/g | 2.0 | 温度/℃ | 硫酸铜固体/g | 加入蒸馏水/mL |
| Ⅰ | 2.0 | 50.0 | 25 | 0 | 0 |
| Ⅱ | 2.0 | 40.0 | 25 | 0 | 10.0 |
| Ⅲ | 2.0 | 50.0 | 25 | 0.2 | 0 |
| Ⅳ | 2.0 | 50.0 | 25 | 4.0 | 0 |
(6)①本实验待测数据可以是
②实验Ⅲ和实验Ⅳ的目的是
(7)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验序号 | 体积V/mL | ||||
| 水 | KI溶液 | 淀粉溶液 | |||
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 | 4.0 | 4.0 | 2.0 | |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


