单选题 适中0.65 引用2 组卷304
已知 呈粉红色,
呈粉红色, 呈蓝色,
呈蓝色, 为无色。现将
为无色。现将 溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: 。用该溶液做实验,溶液的颜色变化如下:
。用该溶液做实验,溶液的颜色变化如下:

| A.等物质的量的 |
| B.由实验①可推知 |
| C.实验②是由于 |
| D.由实验③可知配离子的稳定性: |
21-22高二下·北京西城·期末
类题推荐
已知[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:[Co(H2O)6]2++4Cl- [CoCl4]2-+6H2O ΔH,用该溶液做实验,溶液的颜色变化如图:
[CoCl4]2-+6H2O ΔH,用该溶液做实验,溶液的颜色变化如图:
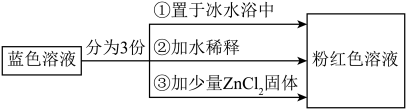
| A.由实验①可推知ΔH>0 |
| B.等物质的量的[Co(H2O)6]2+和[CoCl4]2-中,所含配位键数目不同 |
| C.实验②是由于加水稀释,使得Q<K,导致平衡逆向移动 |
| D.由实验③可知该实验条件下配离子的稳定性:[ZnCl4]2->[CoCl4]2- |
将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:[Co(H2O)6]2++4Cl- [CoCl4]2-+6H2O ΔH。用该溶液做实验,溶液的颜色变化如下:
[CoCl4]2-+6H2O ΔH。用该溶液做实验,溶液的颜色变化如下:
下列结论和解释正确的是
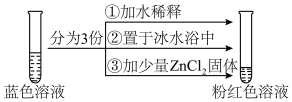
下列结论和解释正确的是
| A.[Co(H2O)6]2+配位数为6,中心离子为Co2+,配位原子为H |
| B.由实验①可知平衡逆向移动 |
| C.由实验②可推知ΔH<0 |
| D.由实验③可知配离子的稳定性:[ZnCl4]2-< [CoCl4]2- |
现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
[Co(H2O)6]2++4Cl- [CoCl4]2- +6H2O ΔH
[CoCl4]2- +6H2O ΔH
用该溶液做实验,溶液的颜色变化如下:

已知:无水CoCl2呈蓝色,[Co(H2O)6]2+呈粉红色, [CoCl4]2-呈蓝色,[ZnCl4]2-为无色。
以下结论和解释不正确的是
[Co(H2O)6]2++4Cl-
用该溶液做实验,溶液的颜色变化如下:

已知:无水CoCl2呈蓝色,[Co(H2O)6]2+呈粉红色, [CoCl4]2-呈蓝色,[ZnCl4]2-为无色。
以下结论和解释不正确的是
| A.由实验①可推知△H>0 |
| B.实验②主要是由于c(H2O)增大,导致上述平衡逆向移动 |
| C.由实验③可知配合离子的稳定性: [ZnC14]2->[CoCl4]2- |
| D.蓝色钴玻璃片加入的物质是Co(AlO2)2,可以吸收黄光 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


