解答题-工业流程题 较难0.4 引用1 组卷316
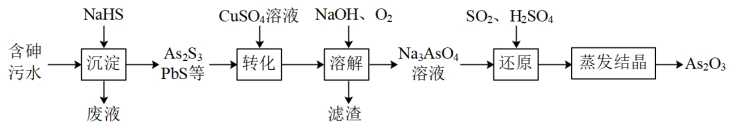
炼锌工厂产生的含砷酸性污水需做无害化处理后排放,一种提取砷并将其资源化的工艺流程如下:
回答下列问题:
(1)“沉淀”时,需控制溶液中HS—的浓度不能过高,原因为_______ 。
(2)“转化”时,As2S3在CuSO4溶液中转化为HAsO2,HAsO2中As元素的化合价为_______ ,该反应的化学方程式为_______ 。
(3)已知Ksp(CuS)=1×10-36、Ksp(PbS)=1×10-26、Ksp(PbSO4)=1×10-8,若“转化时,调节溶液中Cu2+浓度为10-8mol/L,SO 的浓度为0.1mol/L,此时c(Pb2+)=
的浓度为0.1mol/L,此时c(Pb2+)=_______ ,滤渣中的Pb的存在形式为_______ 。
(4)“溶解”时,发生反应的氧化剂和还原剂的物质的量之比为_______ ,实验测得Na3AsO4溶液呈碱性,其原因为_______ (用离子方程式表示)。
(5)该流程制得99g As2O3,则“还原”时消耗标准状况下SO2的体积为_______ 。

回答下列问题:
(1)“沉淀”时,需控制溶液中HS—的浓度不能过高,原因为
(2)“转化”时,As2S3在CuSO4溶液中转化为HAsO2,HAsO2中As元素的化合价为
(3)已知Ksp(CuS)=1×10-36、Ksp(PbS)=1×10-26、Ksp(PbSO4)=1×10-8,若“转化时,调节溶液中Cu2+浓度为10-8mol/L,SO
(4)“溶解”时,发生反应的氧化剂和还原剂的物质的量之比为
(5)该流程制得99g As2O3,则“还原”时消耗标准状况下SO2的体积为
2022·广东·模拟预测
类题推荐
某硫酸工厂的酸性废水中砷(As)元素含量极高,为控制砷的排放,可采用化学沉降法处理含砷废水,相关数据如下表。请回答以下问题:
表1 几种盐的Ksp
表2 工厂污染物排放浓度及允许排放标准
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=____ mol·L-1。
(2)若酸性废水中Fe3+的浓度为1.0×10-4 mol·L-1,则c( )=
)=____ mol·L-1。
(3)工厂排放出的酸性废水中的三价砷(弱酸H3AsO3)不易沉降,可投入MnO2先将其氧化成五价砷 (弱酸H3AsO4),此时MnO2被还原为Mn2+,该反应的离子方程式为_________________ 。
(4)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右,使五价砷以Ca3(AsO4)2的形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为____________ 。
②Ca3(AsO4)2在pH调节到8左右才开始沉淀,原因为____________________________________ 。
③砷酸(H3AsO4)分步电离的平衡常数(25 ℃)为Ka1=5.6×10-3,Ka2=1.7×10-7,Ka3=4.0×10-12,第三步电离的平衡常数表达式为Ka3=_________ ,Na3AsO4第一步水解的离子方程式为 +H2O
+H2O
 +OH-,该步水解的平衡常数(25 ℃)为
+OH-,该步水解的平衡常数(25 ℃)为____ 。
表1 几种盐的Ksp
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| CaSO4 | 9.1×10-6 |
| FeAsO4 | 5.7×10-21 |
| 污染物 | H2SO4 | As |
| 废水浓度 | 29.4 g·L-1 | 1.6 g·L-1 |
| 排放标准 | pH=6~9 | 0.5 mg·L-1 |
(2)若酸性废水中Fe3+的浓度为1.0×10-4 mol·L-1,则c(
(3)工厂排放出的酸性废水中的三价砷(弱酸H3AsO3)不易沉降,可投入MnO2先将其氧化成五价砷 (弱酸H3AsO4),此时MnO2被还原为Mn2+,该反应的离子方程式为
(4)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右,使五价砷以Ca3(AsO4)2的形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为
②Ca3(AsO4)2在pH调节到8左右才开始沉淀,原因为
③砷酸(H3AsO4)分步电离的平衡常数(25 ℃)为Ka1=5.6×10-3,Ka2=1.7×10-7,Ka3=4.0×10-12,第三步电离的平衡常数表达式为Ka3=

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网