解答题-结构与性质 适中0.65 引用1 组卷354
揭示土壤的成分从矿物开始。橄榄石属于镁铁质矿物的一种,主要成分是铁或镁的硅酸盐,同时含有锰、镍、钴等元素,晶体呈现粒状,属于岛状硅酸盐。回答下列问题:
(1)基态Co原子的核外电子占据的3d能级上的成对电子是_______ 个。
(2)Mn和Fe的各级电离能如下。
Mn与Fe相比,I1和I2较小,而I3较大,其原因是_______ 。
(3)在硅酸盐中,原硅酸根离子和多硅酸根离子结构如图所示(图中 表示氧原子,
表示氧原子, 表示Si-O),若多硅酸根离子Q中硅原子数为n,则该离子符号为
表示Si-O),若多硅酸根离子Q中硅原子数为n,则该离子符号为_______ ,在此结构中每个Si原子与_______ 个O原子相连,这几个O原子形成的空间结构是_______ 。
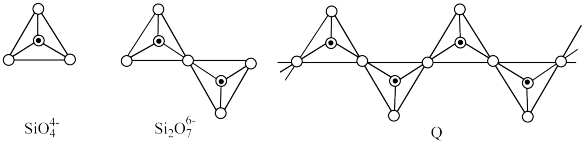
(4)下图是某橄榄石的晶胞结构,用NA表示阿伏加德罗常数的值。

① 中Si原子的杂化类型是
中Si原子的杂化类型是_______ 。
②该晶体的化学式为_______ 。Mg原子周围最近的Fe原子有_______ 个。
③该晶体的密度是_______ g·cm-3(用含a、b、NA的代数式表示)。
(1)基态Co原子的核外电子占据的3d能级上的成对电子是
(2)Mn和Fe的各级电离能如下。
| 电离能/(kJ ·mol-1) | I1 | I2 | I3 | I4 | I5 |
| Mn | 717.3 | 1509.0 | 3 248 | 4940 | 6990 |
| Fe | 762. 5 | 1561.9 | 2957 | 5 290 | 7240 |
(3)在硅酸盐中,原硅酸根离子和多硅酸根离子结构如图所示(图中
 表示氧原子,
表示氧原子, 表示Si-O),若多硅酸根离子Q中硅原子数为n,则该离子符号为
表示Si-O),若多硅酸根离子Q中硅原子数为n,则该离子符号为
(4)下图是某橄榄石的晶胞结构,用NA表示阿伏加德罗常数的值。

①
②该晶体的化学式为
③该晶体的密度是
2021·河南焦作·一模
类题推荐
完成下列问题。
(1)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)________ I1(Cu)(填“大于”或“小于”)。
(2)基态Fe2+的电子排布式为___________ 。
(3)在N、Mg、Al、Si四种元素中,有一种元素的电离能数据如下:
则该元素的元素符号是___________ 。
(4)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是___________ 、中心原子的杂化类型是___________ 。根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是___________ 。
(5)与O3分子互为等电子体的一种阴离子为___________ (填化学式)。
(6)Cu、N两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是___________ 。(用元素符号表示);若晶胞的棱长anm,阿伏加德罗常数为NA,则该晶体的密度为___________ g/cm3(用含a、NA的式子表示)。

(1)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)
(2)基态Fe2+的电子排布式为
(3)在N、Mg、Al、Si四种元素中,有一种元素的电离能数据如下:
| 电离能 | I1 | I2 | I3 | I4 | … |
| I0/kJ·mol−1 | 578 | 1817 | 2745 | 11575 | … |
则该元素的元素符号是
(4)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是
(5)与O3分子互为等电子体的一种阴离子为
(6)Cu、N两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是

第四周期过渡元素Mn、Fe、Ti、Ni可与C、H、O形成多种化合物。
(1)下列叙述正确的是______ 。(填字母)
A.CH2O与水分子间能形成氢键
B.CH2O和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个 键和1个大
键和1个大 键,C6H6是非极性分子
键,C6H6是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
(2)Mn和Fe的部分电离能数据如下表:
Mn原子价电子排布式为__________ ,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是___________________________ 。
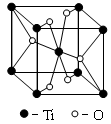
(3)根据元素原子的外围电子排布,可将元素周期表分区,其中Ti属于____________ 区。Ti的一种氧化物X,其晶胞结构如图所示,则X的化学式为____________ 。
(4)某铁的化合物结构简式如图所示
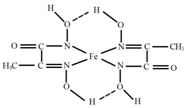
①组成上述化合物中各非金属元素电负性由大到小的顺序为___________ (用元素符号表示)。
②在图中用“→”标出亚铁离子的配位键_______ 。
(5)NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的配位数为_______ ,这几个O2-构成的空间构型为_____________ 。已知Ni2+与O2-的核间距为anm,NiO的摩尔质量为M g/mol,阿伏加德罗常数用NA表示,则该晶体的密度为________ g/cm3。
(1)下列叙述正确的是
A.CH2O与水分子间能形成氢键
B.CH2O和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
(2)Mn和Fe的部分电离能数据如下表:
| 元 素 | Mn | Fe | |
| 电离能/kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
Mn原子价电子排布式为
(3)根据元素原子的外围电子排布,可将元素周期表分区,其中Ti属于

(4)某铁的化合物结构简式如图所示

①组成上述化合物中各非金属元素电负性由大到小的顺序为
②在图中用“→”标出亚铁离子的配位键
(5)NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的配位数为
碳、氮、铁三种元素均可以形成一些结构独特、性能特殊的物质。回答下列问题:
(1)基态氮原子能量最高能级的电子云轮廓图为___________ 形;基态碳原子和铁原子所含未成对电子数之比为___________ 。
(2)铁与锰在元素周期表中属于相邻元素,二者电离能(I)如下表。
I3(Mn)>I3(Fe)的主要原因为___________ 。
(3)(CN)2分子中每个原子最外层均为8电子结构,则(CN)2分子中所含σ键与π键数目之比为___________ 。(CN)2的沸点为一21.2 °C,N2的沸点为一195.62 °C,(CN)2的沸点高于N2的原因为______ 。
(4)[Fe(CN)6]3-中化学键的类型为___________ ,配位体中碳原子的杂化方式为___________ 。
(5)铁原子与氮原子形成的一种晶胞如下图所示(白球代表铁原子,黑球代表氮原子)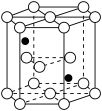 ,该晶体的化学式为
,该晶体的化学式为___________ ,已知该晶体的密度为d g· cm-3,正六棱柱底边边长为x cm,NA为阿伏加德罗常数的值,则该正六棱柱的高为___________ cm(用含x、d、NA的代数式表示,列出计算式即可)。
(1)基态氮原子能量最高能级的电子云轮廓图为
(2)铁与锰在元素周期表中属于相邻元素,二者电离能(I)如下表。
| 元素 | I1/(kJ·mol-1) | I2/(kJ·mol-1) | I3/(kJ·mol-1) |
| 锰 | 717.3 | 1509.9 | 3248 |
| 铁 | 762.5 | 1561.9 | 2 953 |
I3(Mn)>I3(Fe)的主要原因为
(3)(CN)2分子中每个原子最外层均为8电子结构,则(CN)2分子中所含σ键与π键数目之比为
(4)[Fe(CN)6]3-中化学键的类型为
(5)铁原子与氮原子形成的一种晶胞如下图所示(白球代表铁原子,黑球代表氮原子)
 ,该晶体的化学式为
,该晶体的化学式为组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


