解答题-原理综合题 适中0.65 引用1 组卷227
CO2是主要的温室气体,以CO2和H2为原料制造更高价值的化学产品是用来缓解温室效应的研究方向,回答下列问题:
(1)工业上常用CO2和H2为原料合成甲醇( ),过程中发生如下两个反应:
),过程中发生如下两个反应:
反应I:

反应II:

①则

_______  ;
;
②若反应II逆反应活化能Ea(逆)为 ,则该反应的Ea (正)活化能为
,则该反应的Ea (正)活化能为_______  。
。
(2)若将等物质的量的CO和H2混合气体充入恒温恒容密闭容器中进行反应: ,下列事实能说明此反应已达到平衡状态的是_______。
,下列事实能说明此反应已达到平衡状态的是_______。
(3)向2L容器中充入 和
和 ,若只发生反应I,测得反应在不同压强、不同温度下,平衡混合物中
,若只发生反应I,测得反应在不同压强、不同温度下,平衡混合物中 体积分数如图1所示,测得反应时逆反应速率与容器中
体积分数如图1所示,测得反应时逆反应速率与容器中 关系如图II所示:
关系如图II所示:
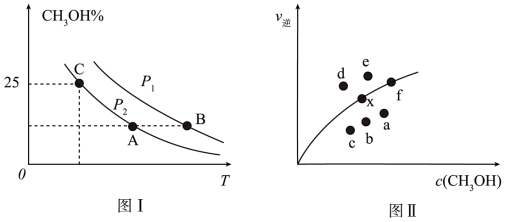
①图I中P1_______ P2(填“>”、“<”或“=”)。
②图II中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是_______ 。
③利用图I中C点对应的数据,计算求出对应温度下反应Ⅰ的平衡常数K=_______ 。
(1)工业上常用CO2和H2为原料合成甲醇(
反应I:
反应II:
①则
②若反应II逆反应活化能Ea(逆)为
(2)若将等物质的量的CO和H2混合气体充入恒温恒容密闭容器中进行反应:
| A.容器内气体密度保持不变 |
| B.混合气体的平均相对分子质量不变 |
| C.生成 |
| D.CO的体积分数保持不变 |

①图I中P1
②图II中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是
③利用图I中C点对应的数据,计算求出对应温度下反应Ⅰ的平衡常数K=
21-22高二下·福建福州·期末
类题推荐  是主要的温室气体,以
是主要的温室气体,以 和
和 为原料制造更高价值的化学产品是用来缓解温室效应的研究方向。请回答下列问题:
为原料制造更高价值的化学产品是用来缓解温室效应的研究方向。请回答下列问题:
(1)工业上常用 和
和 为原料合成甲醇(
为原料合成甲醇( ),过程中发生如下两个反应:
),过程中发生如下两个反应:
反应Ⅰ:

反应Ⅱ:

①已知:键能指断开1 mol 气态键所吸收的能量或形成1 mol 气态键所释放的能量。
几种化学键的键能如下表所示:
则x=_______  (写出计算表达式);
(写出计算表达式);
②若反应Ⅱ逆反应活化能 (逆)为
(逆)为 ,则该反应的
,则该反应的 (正)活化能为
(正)活化能为_______  。
。
(2)向2 L容器中充入1 mol 和2 mol
和2 mol ,若只发生反应Ⅰ,测得反应在不同压强、不同温度下,平衡混合物中
,若只发生反应Ⅰ,测得反应在不同压强、不同温度下,平衡混合物中 体积分数如图Ⅰ所示,测得反应时逆反应速率与容器中
体积分数如图Ⅰ所示,测得反应时逆反应速率与容器中 关系如图Ⅱ所示:
关系如图Ⅱ所示:
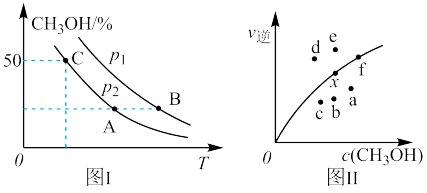
①图Ⅰ中A、B、C三点对应的平衡常数 、
、 、
、 由大到小的顺序排列为
由大到小的顺序排列为_______ ,图Ⅰ中C点 的转化率为
的转化率为_______ 。
②图Ⅱ中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是_______ 。
(3)若反应Ⅲ: 的正、逆反应速率分别可表示为
的正、逆反应速率分别可表示为 、
、 ,
, 、
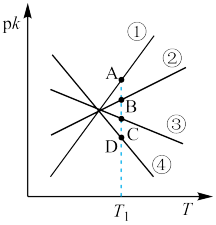
、 分别为正、逆反应速率常数,c为物质的量浓度。则下图(
分别为正、逆反应速率常数,c为物质的量浓度。则下图( ;T表示温度)所示①、②、③、④四条斜线中,能表示以
;T表示温度)所示①、②、③、④四条斜线中,能表示以 随T变化关系的是斜线
随T变化关系的是斜线_______ ,图中A、B、C、D点的纵坐标分别为a+3、a+1、a-1、a-3,则温度 时化学平衡常数
时化学平衡常数
_______ 。
CO2和CH4是两种主要的温室气体,以CO2和CH4为原料制造更高价值的化学产品是用来缓解温室效应的研究方向。回答下列问题:
(1)工业上CO2-CH4催化重整是目前大规模制取合成气(CO和H2混合气)的重要方法,其原理为:
反应I:CH4(g)+H2O(g) CO(g)+3H2(g) ∆H1=+206.4 kJ·mol-1
CO(g)+3H2(g) ∆H1=+206.4 kJ·mol-1
反应II:CO(g)+H2O(g) CO2(g)+H2(g) ∆H2=-41 kJ·mol-1
CO2(g)+H2(g) ∆H2=-41 kJ·mol-1
几种化学键的键能如表所示:
①a=_______ kJ·mol-1。
②反应II中,若逆反应活化能Ea(逆)为124 kJ·mol-1,则Ea(正)为_______ kJ·mol-1。
(2)将等物质的量的CH4(g)和H2O(g)充入恒温恒容的密闭容器中,发生反应I和反应II,容器内气体的压强随时间的变化如表所示。
①若用单位时间内气体分压(气体分压=气体总压×体积分数)的变化来表示反应速率,则反应I前120min内的平均反应速率v(CH4)=_______ kPa·min-1(结果保留2位小数)。
②300 min时,测得氢气分压为100 kPa,则反应II在该温度下的平衡常数Kp=_______ (Kp为用气体分压表示的平衡常数,结果保留2位小数)。
(3)向2 L容器中充入1 mol CH4和1 mol H2O,若只发生反应I,测得反应在不同压强、不同温度下,平衡混合物中CH4体积分数如图I所示,某温度下逆反应速率与容器中c(CH4)关系如图II所示:
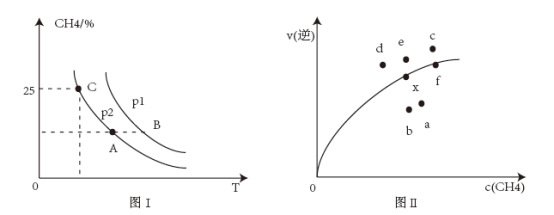
①图I中A、B、C三点对应的平衡常数K(A)、K(B)、K(C)由大到小的顺序为_______ ,p1_______ p2(填“>”“<”或“=”)。
②图II中当x点平衡体系升高至某温度时,反应可重新达平衡状态,新平衡点可能是_______ (填标号)。
(1)工业上CO2-CH4催化重整是目前大规模制取合成气(CO和H2混合气)的重要方法,其原理为:
反应I:CH4(g)+H2O(g)
反应II:CO(g)+H2O(g)
几种化学键的键能如表所示:
| 化学键 | C-H | H-O | H-H | C |
| 键能/kJ | 413 | 467 | 436 | a |
①a=
②反应II中,若逆反应活化能Ea(逆)为124 kJ·mol-1,则Ea(正)为
(2)将等物质的量的CH4(g)和H2O(g)充入恒温恒容的密闭容器中,发生反应I和反应II,容器内气体的压强随时间的变化如表所示。
| 时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
| 压强/kPa | 100 | 118 | 132 | 144 | 154 | 162 | 162 |
①若用单位时间内气体分压(气体分压=气体总压×体积分数)的变化来表示反应速率,则反应I前120min内的平均反应速率v(CH4)=
②300 min时,测得氢气分压为100 kPa,则反应II在该温度下的平衡常数Kp=
(3)向2 L容器中充入1 mol CH4和1 mol H2O,若只发生反应I,测得反应在不同压强、不同温度下,平衡混合物中CH4体积分数如图I所示,某温度下逆反应速率与容器中c(CH4)关系如图II所示:

①图I中A、B、C三点对应的平衡常数K(A)、K(B)、K(C)由大到小的顺序为
②图II中当x点平衡体系升高至某温度时,反应可重新达平衡状态,新平衡点可能是
(1)工业上常用
反应Ⅰ:
反应Ⅱ:
①已知:键能指断开1 mol 气态键所吸收的能量或形成1 mol 气态键所释放的能量。
几种化学键的键能如下表所示:
| 化学键 | ||||||
| 键能 | a | b | c | d | e | x |
则x=
②若反应Ⅱ逆反应活化能
(2)向2 L容器中充入1 mol

①图Ⅰ中A、B、C三点对应的平衡常数
②图Ⅱ中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是
(3)若反应Ⅲ:

CO2是主要的温室气体,以CO2和H2为原料制造更高价值的化学产品是用来缓解温室效应的研究方向,回答下列问题:
(1)工业上常用CO2和H2为原料合成甲醇(CH3OH),过程中发生如下两个反应:
反应I:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=—51kJ·mol-1
CH3OH(g)+H2O(g) △H1=—51kJ·mol-1
反应II:CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.17kJ·mol-1
CO(g)+H2O(g) △H2=+41.17kJ·mol-1
①已知:键能指断开1mol气态键所吸收的能量或形成1mol气态键所释放的能量。几种化学键的键能如下表所示:
则a=___________ kJ·mol-1;
②若反应II逆反应活化能Ea(逆)为124kJ·mol-1,则该反应的Ea(正)活化能为___________ kJ· mol-1。
(2)向2L容器中充入1molCO2和2molH2,若只发生反应I,测得反应在不同压强、不同温度下,平衡混合物中CH3OH体积分数如图1所示,测得反应时逆反应速率与容器中c(CH3OH)关系如图II所示:
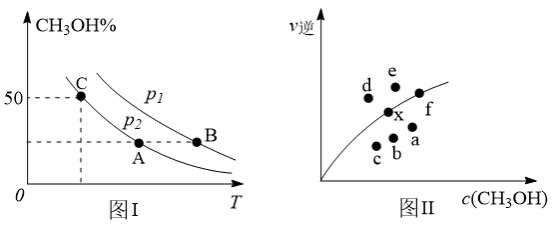
①图I中A、B、C三点对应的平衡常数K(A)、K(B)、K(C)由大到小的顺序排列为___________ ,图I中C点CO2的转化率为___________ 。
②图II中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是___________ 。
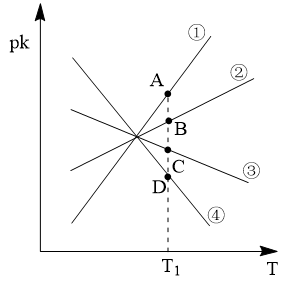
(3)若反应IIICO(g)+H2O(g) CO2(g)+H2(g)的正、逆反应速率分别可表示为v正=k正c(CO)·c(H2O)、v逆=k逆c(CO2)·c(H2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。则下图(pk=-lgk:T表示温度)所示①、②、③、④四条斜线中,能表示以pk正随T变化关系的是斜线
CO2(g)+H2(g)的正、逆反应速率分别可表示为v正=k正c(CO)·c(H2O)、v逆=k逆c(CO2)·c(H2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。则下图(pk=-lgk:T表示温度)所示①、②、③、④四条斜线中,能表示以pk正随T变化关系的是斜线___________ ,能表示pk逆随T变化关系的是斜线___________ ,图中A、B、C、D点的纵坐标分别为a+3、a+1、a-1、a-3,则温度T1时化学平衡常数K=___________ mol-1·L。
(1)工业上常用CO2和H2为原料合成甲醇(CH3OH),过程中发生如下两个反应:
反应I:CO2(g)+3H2(g)
反应II:CO2(g)+H2(g)
①已知:键能指断开1mol气态键所吸收的能量或形成1mol气态键所释放的能量。几种化学键的键能如下表所示:
| 化学键 | C-H | C-O | H-O(H2O中) | H-O(CH3OH中) | H-H | C=O |
| 键能/kJ· mol-1 | 406 | 351 | 462.5 | 465 | 436 | a |
②若反应II逆反应活化能Ea(逆)为124kJ·mol-1,则该反应的Ea(正)活化能为
(2)向2L容器中充入1molCO2和2molH2,若只发生反应I,测得反应在不同压强、不同温度下,平衡混合物中CH3OH体积分数如图1所示,测得反应时逆反应速率与容器中c(CH3OH)关系如图II所示:

①图I中A、B、C三点对应的平衡常数K(A)、K(B)、K(C)由大到小的顺序排列为
②图II中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是
(3)若反应IIICO(g)+H2O(g)

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


