解答题-原理综合题 较难0.4 引用2 组卷311
Ⅰ.已知断裂几种化学键要吸收的能量如下:
(1)1molHI(g)分解得 、
、 时,
时,_______ (填“吸收”或“放出”)约_______ kJ热量。
Ⅱ.某密闭恒压容器中,某气相化学反应 在4种不同条件下进行,
在4种不同条件下进行, 、
、 起始浓度为0,反应物HI的浓度(mol/L)随反应时间(min)的变化情况如下表:
起始浓度为0,反应物HI的浓度(mol/L)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列填空:
(2)在实验1,反应在10至40分钟时间内, 的平均反应速率为
的平均反应速率为_______ 。
(3)设实验1的反应速率为v1,实验2的反应速率为v2,则v2_______ v1 (“>”“=”“<”),并推测实验2隐含的条件可能是_______ ,并计算实验2,反应在0至20分钟内,反应物HI转化率为_______ 。
(4)结合上述4种不同条件的数据,最终颜色最深的实验是:_______ (填实验序号)。
(5)下列叙述能说明上述反应一定达到化学平衡状态的是_______ 。
A.混合气体的总物质的量不随时间的变化而变化
B.混合气体颜色不随时间的变化而变化
C.单位时间内每消耗1mol ,同时生成1mol
,同时生成1mol
D.混合气体的密度不随时间的变化而变化
E.混合气体的平均摩尔质量不随时间的变化而变化
F.
Ⅲ.燃料电池是一种高效、环境友好的供电装置,如图为 燃料电池的工作原理示意图,a、b均为惰性电极。
燃料电池的工作原理示意图,a、b均为惰性电极。
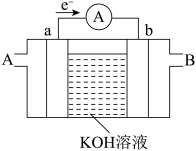
(6)该电池放电时a极的电极反应为:_______ 。
| 化学键 | H-H | H-I | I-I |
| 断裂1mol键吸收的能量/kJ | 436.0 | 298.7 | 152.7 |
Ⅱ.某密闭恒压容器中,某气相化学反应
| 实验序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | 1.2 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(2)在实验1,反应在10至40分钟时间内,
(3)设实验1的反应速率为v1,实验2的反应速率为v2,则v2
(4)结合上述4种不同条件的数据,最终颜色最深的实验是:
(5)下列叙述能说明上述反应一定达到化学平衡状态的是
A.混合气体的总物质的量不随时间的变化而变化
B.混合气体颜色不随时间的变化而变化
C.单位时间内每消耗1mol
D.混合气体的密度不随时间的变化而变化
E.混合气体的平均摩尔质量不随时间的变化而变化
F.
Ⅲ.燃料电池是一种高效、环境友好的供电装置,如图为

(6)该电池放电时a极的电极反应为:
21-22高一下·四川广安·期末
类题推荐
Ⅰ、某温度时,在一个 10L 的恒容容器中,X、Y、Z 均为气体,三种物质的物 质的量随时间的变化曲线如图所示.根据图中数据填空:
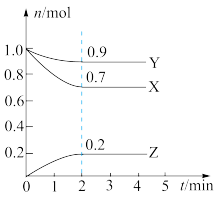
(1)该反应的化学方程式为______ ;
(2)反应开始至 2min,以气体 Z 表示的平均反应速率为______ ;
(3)平衡时容器内混合气体密度比起始时______ (填“变大”,“变小”或“不变” 下同),混合气体的平均相对分子质量比起始时__________ ;
(4)将 a mol X 与 b mol Y 的混合气体发生上述反应,反应到某时刻各物质的量恰好满足: n(X)=n(Y)=2n(Z),则原混合气体中 a:b=______ 。
Ⅱ、在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强,②混合 气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜 色,⑥各反应物或生成物的反应速率之比等于化学计量数之比
(1)一定能证明 2SO2(g)+O2(g) 2SO3(g)达到平衡状态的是
2SO3(g)达到平衡状态的是_____ (填序号,下同)。
(2)一定能证明 I2(g)+H2(g) 2HI(g)达到平衡状态的是
2HI(g)达到平衡状态的是 ______ 。
(3)一定能证明 A(s)+2B(g) C(g)+D(g)达到平衡状态的是
C(g)+D(g)达到平衡状态的是______ 。(B C D 均无色)
III 、某化学反应 2A B+D 在四种条件下进行,B、D 起始浓度为 0,反应物 A 的浓度(mol/L)随反应时间(min)的变化情况如表:
B+D 在四种条件下进行,B、D 起始浓度为 0,反应物 A 的浓度(mol/L)随反应时间(min)的变化情况如表:
比较实验 4 和实验 1 可推测该正反应是_____ 反应(填“吸热”或“放热”)。 理由_________

(1)该反应的化学方程式为
(2)反应开始至 2min,以气体 Z 表示的平均反应速率为
(3)平衡时容器内混合气体密度比起始时
(4)将 a mol X 与 b mol Y 的混合气体发生上述反应,反应到某时刻各物质的量恰好满足: n(X)=n(Y)=2n(Z),则原混合气体中 a:b=
Ⅱ、在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强,②混合 气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜 色,⑥各反应物或生成物的反应速率之比等于化学计量数之比
(1)一定能证明 2SO2(g)+O2(g)
(2)一定能证明 I2(g)+H2(g)
(3)一定能证明 A(s)+2B(g)
III 、某化学反应 2A
| 实验序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800 | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
某化学反应2A⇌B+D在四种不同条件下进行,B、D起始浓度为0.反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20min时间内平均速率为___________ mol·(L·min)-1。
(2)在实验2中A的初始浓度C2=___________ mol·L-1,反应经20min就达到平衡,可推测实验2中还隐含的条件是___________ 。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3___________ v1(填“>”“=”或“<”=,且C3___________ 1.0mol·L-1(填“>”“=”或“<”=)。
(4)比较实验4和实验1,可推测该反应是___________ 反应(选填“吸热”或“放热”),理由是___________ 。
| 实验 序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)在实验1,反应在10至20min时间内平均速率为
(2)在实验2中A的初始浓度C2=
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3
(4)比较实验4和实验1,可推测该反应是
某化学反应2A  B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为___________ mol/(L·min)。
(2)在实验2,A的初始浓度c2=___________ mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是___________ 。
(3)设实验3的反应速率为v3, 实验1的反应速率为v1,则v3___________ v1(填>、<、=)。
(4)比较实验4和实验1,可推测该反应是___________ 反应(选填吸热、放热)。理由是___________ 。
| 实验序号 |  | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为
(2)在实验2,A的初始浓度c2=
(3)设实验3的反应速率为v3, 实验1的反应速率为v1,则v3
(4)比较实验4和实验1,可推测该反应是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


