填空题 适中0.65 引用5 组卷579
甲、乙两位同学探究外界条件对化学反应速率的影响。
【实验原理】反应:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,反应过程中溶液出现乳白色浑浊和有刺激性气味的气体。
【实验用品】0.1mol/LNa2S2O3溶液、0.1mol/LH2SO4溶液、蒸馏水。
试管、烧杯、量筒、胶头滴管等。
实验一:甲同学利用如图装置测定化学反应速率。_______ 。除如图所示的实验用品外,还需要的实验仪器是_______ 。
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出在2min内的反应速率v(H+)=0.02mol/(L·min),而该速率值比实际值偏小,其原因是_______ 。
实验二:乙同学得到各组实验数据如下表。
(3)实验Ⅰ、Ⅱ探究_______ 对化学反应速率的影响。
①a=_______ 。
②V=_______ ,加入VmL水的目的是_______ 。
(4)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象是_______ 。
【实验原理】反应:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,反应过程中溶液出现乳白色浑浊和有刺激性气味的气体。
【实验用品】0.1mol/LNa2S2O3溶液、0.1mol/LH2SO4溶液、蒸馏水。
试管、烧杯、量筒、胶头滴管等。
实验一:甲同学利用如图装置测定化学反应速率。
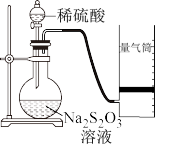
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出在2min内的反应速率v(H+)=0.02mol/(L·min),而该速率值比实际值偏小,其原因是
实验二:乙同学得到各组实验数据如下表。
| 实验编号 | Na2S2O3溶液 | H2SO4溶液 | 蒸馏水 | ||||
| 浓度/ (mol/L) | 体积/mL | 浓度/ (mol/L) | 体积/mL | 体积/mL | 温度/℃ | ||
| Ⅰ | 0.1 | 1.5 | 0.1 | 1.5 | V | 20 | |
| Ⅱ | 0.1 | 2.5 | 0.1 | 1.5 | 8 | a | |
| Ⅲ | 0.1 | 2.5 | 0.1 | 1.5 | 8 | 30 | |
①a=
②V=
(4)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象是
21-22高一下·北京东城·期末
类题推荐
回答下列问题。
Ⅰ.某实验小组用 100mL0.50mol·L-1NaOH 溶液与 60mL0.50mol·L-1 硫酸溶液进行中和热的测定,装置如图1所示。回答下列问题:
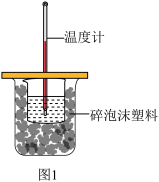
(1)图中装置缺少的仪器是___________ 。
(2)硫酸稍过量的原因是___________ 。
(3)某小组同学实验数据记录如下表,若近似认为 0.50mol•L-1NaOH 溶液与 0.50mol•L-1硫酸溶液的密度都是1g•cm-3,中和后生成溶液的比热容 c=4.18J•g-1•℃-1,则上述实验测得的中和热△H =___________ (结果保留至小数点后一位)。
(4)上述实验测得中和热的数值小于 57.3kJ·mol-1,产生偏差的原因可能是___________(填字母)。
Ⅱ.甲、乙两位同学探究外界条件对化学反应速率的影响。
【实验原理】反应:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,反应过程中溶液出现乳白色浑浊和有刺激性气味的 气体。
【实验用品】0.1mol/LNa2S2O3溶液、0.1mol/LH2SO4溶液、蒸馏水、试管、烧杯、量筒、胶头滴管等。
实验一:甲同学利用如图装置测定化学反应速率。
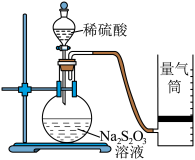
(5)为保证实验的准确性和可靠性,利用该装置进行实验前应先进行的操作是___________ 。除如图所示的实验用品外,还需要的实验仪器 是___________ 。
(6)若在 2min 时收集到 224mL(已折算成标准状况)气体,可计算出在 2min 内的反应速率v(H+)=0.02mol/(L·min),而该速率值比实际值偏小,其原因是_____________________ 。
实验二:乙同学得到各组实验数据如下表。
(7)实验Ⅰ、Ⅱ探究___________ 对化学反应速率的影响,a=___________ ,V=___________ 。
(8)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象是___________ 。
Ⅰ.某实验小组用 100mL0.50mol·L-1NaOH 溶液与 60mL0.50mol·L-1 硫酸溶液进行中和热的测定,装置如图1所示。回答下列问题:

(1)图中装置缺少的仪器是
(2)硫酸稍过量的原因是
(3)某小组同学实验数据记录如下表,若近似认为 0.50mol•L-1NaOH 溶液与 0.50mol•L-1硫酸溶液的密度都是1g•cm-3,中和后生成溶液的比热容 c=4.18J•g-1•℃-1,则上述实验测得的中和热△H =
| 实验序号 | 起始温度t1/℃ | 终止温度T2/℃ | 平均温度差(t2-t1)/℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | _____ |
| 2 | 27.0 | 27.2 | 27.1 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
| A.量取 NaOH 溶液时仰视读数 |
| B.为了使反应充分,向酸溶液中分次加入碱溶液 |
| C.实验装置保温隔热效果差 |
| D.用铜丝代替玻璃搅拌器搅拌 |
Ⅱ.甲、乙两位同学探究外界条件对化学反应速率的影响。
【实验原理】反应:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,反应过程中溶液出现乳白色浑浊和有刺激性气味的 气体。
【实验用品】0.1mol/LNa2S2O3溶液、0.1mol/LH2SO4溶液、蒸馏水、试管、烧杯、量筒、胶头滴管等。
实验一:甲同学利用如图装置测定化学反应速率。

(5)为保证实验的准确性和可靠性,利用该装置进行实验前应先进行的操作是
(6)若在 2min 时收集到 224mL(已折算成标准状况)气体,可计算出在 2min 内的反应速率v(H+)=0.02mol/(L·min),而该速率值比实际值偏小,其原因是
实验二:乙同学得到各组实验数据如下表。
| 实验编号 | Na2S2O3溶液 | H2SO4溶液 | 蒸馏水 | |||
| 浓度/(mol/L) | 体积/mL | 浓度/(mol/L) | 体积/mL | 体积/mL | 温度/℃ | |
| I | 0.1 | 3.0 | 0.1 | 3.0 | V | 20 |
| Ⅱ | 0.1 | 5.0 | 0.1 | 3.0 | 0 | a |
| Ⅲ | 0.1 | 5.0 | 0.1 | 3.0 | 0 | 30 |
(8)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象是
化学反应速率是描述化学反应进行快慢程度的物理量。下面是某同学测定化学反应速率并探究其影响因素的实验。
Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率。(已知:S2O32-+2H+===H2O+S↓+SO2↑)
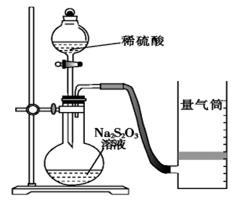
(1)为保证实验准确性、可靠性,利用该装置进行实验前应先进行的步骤是_____________________ ;除如图装置所示的实验用品、仪器外,还需要的一件实验仪器是______________ 。
(2)若在2 min时收集到224 mL(已折算成标准状况)气体,可计算出该2 min内H+的反应速率,而该测定值比实际值偏小,其原因是________________________ 。
(3)试简述测定该反应的化学反应速率的其他方法:__________________ (写一种)。
Ⅱ.为探讨化学反应速率的影响因素,设计的实验方案如下表。
(已知 I2+2S2O32-===S4O62-+2I-,其中Na2S2O3溶液均足量)
(4)该实验进行的目的是_____________ 淀粉溶液的作用是____________ 。表中Vx==_______ mL,比较t1、t2、t3大小,试推测该实验结论:___________________________
Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率。(已知:S2O32-+2H+===H2O+S↓+SO2↑)

(1)为保证实验准确性、可靠性,利用该装置进行实验前应先进行的步骤是
(2)若在2 min时收集到224 mL(已折算成标准状况)气体,可计算出该2 min内H+的反应速率,而该测定值比实际值偏小,其原因是
(3)试简述测定该反应的化学反应速率的其他方法:
Ⅱ.为探讨化学反应速率的影响因素,设计的实验方案如下表。
(已知 I2+2S2O32-===S4O62-+2I-,其中Na2S2O3溶液均足量)
| 实验序号 | 体积V/mL | 时间/s | |||
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
化学反应速率是描述化学反应进行快慢程度的物理量。下面是某同学测定化学反应速率并探究其影响因素的实验。
I.测定化学反应速率:该同学利用如图装置测定化学反应速率。(已知: +2H+ = H2O+S↓+SO2↑)
+2H+ = H2O+S↓+SO2↑)
(1)为保证实验准确性、可靠性,利用该装置进行实验前应先检验装置的气密性;除如图所示的实验用品、仪器外,还需要的一件实验仪器是___________ 。
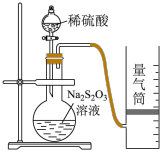
(2)若在2 min时收集到224 mL(已折算成标准状况)的气体,可计算出该2 min内H+的反应速率,而该测定值比实际值偏小,其原因是___________ 。
(3)试简述测定该反应的化学反应速率的其他方法:___________ (写一种)。
II.为探讨化学反应速率的影响因素,设计的实验方案如下表:
(已知 I2+2 =
=  +2I-,其中Na2S2O3溶液均足量)
+2I-,其中Na2S2O3溶液均足量)
(4)该实验进行的目的是___________ ,淀粉溶液的作用是___________ ,表中Vx=___________ mL,比较t1、t2、t3大小,试推测该实验结论:___________ 。
I.测定化学反应速率:该同学利用如图装置测定化学反应速率。(已知:
(1)为保证实验准确性、可靠性,利用该装置进行实验前应先检验装置的气密性;除如图所示的实验用品、仪器外,还需要的一件实验仪器是

(2)若在2 min时收集到224 mL(已折算成标准状况)的气体,可计算出该2 min内H+的反应速率,而该测定值比实际值偏小,其原因是
(3)试简述测定该反应的化学反应速率的其他方法:
II.为探讨化学反应速率的影响因素,设计的实验方案如下表:
(已知 I2+2
实验序号 | 体积V/mL | 时间/s | |||
Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


