解答题-结构与性质 适中0.65 引用1 组卷103
元素周期表中第四周期元素形成的化合物性质丰富,回答下列问题:
(1)复兴号高铁车体材质用到 、
、 等元素。
等元素。 的一种配合物化学式为
的一种配合物化学式为 ,下列说法正确的是___________(填字母标号)。
,下列说法正确的是___________(填字母标号)。
(2) 能形成化合物
能形成化合物 ,在该化合物中不含
,在该化合物中不含___________ (填字母标号)。
A. 键 B.
键 B. 键 C.配位键 D.离子键 E.极性键 F.非极性键
键 C.配位键 D.离子键 E.极性键 F.非极性键
(3) 中
中 的键角比
的键角比 的键角
的键角___________ (填“大”或“小”)原因是___________ 。
(4)在 催化作用下,呋喃(
催化作用下,呋喃( )可与氨反应,转化为吡咯(
)可与氨反应,转化为吡咯( )。二者熔、沸点关系为:呋喃
)。二者熔、沸点关系为:呋喃___________ 吡咯(填“高于”或“低于”),原因是___________ 。
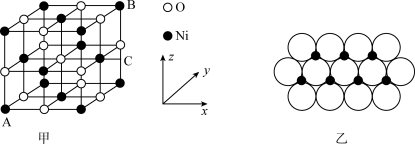
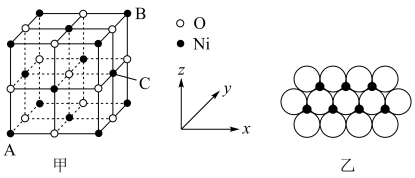
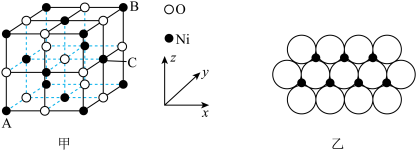
(5) 的晶胞结构如图甲所示,其中离子坐标参数A为
的晶胞结构如图甲所示,其中离子坐标参数A为 ,B为
,B为 ,则C的离子坐标参数为
,则C的离子坐标参数为___________ 。一定温度下, 晶体可以自发地分散并形成“单分子层”,可以认为
晶体可以自发地分散并形成“单分子层”,可以认为 作密置单层排列,
作密置单层排列, 填充其中(如图乙),已知
填充其中(如图乙),已知 的半径为
的半径为 ,设阿伏加德罗常数值为
,设阿伏加德罗常数值为 ,每平方米面积上具有该晶体的质量为
,每平方米面积上具有该晶体的质量为___________ g(用含a、 的代数式表示)。
的代数式表示)。
(1)复兴号高铁车体材质用到
| A. |
| B. |
| C. |
| D. |
A.
(3)
(4)在
 )可与氨反应,转化为吡咯(
)可与氨反应,转化为吡咯( )。二者熔、沸点关系为:呋喃
)。二者熔、沸点关系为:呋喃(5)

21-22高二下·内蒙古赤峰·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 )可与氨反应,转化为吡咯(
)可与氨反应,转化为吡咯(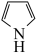 )。二者熔、沸点关系为:呋喃
)。二者熔、沸点关系为:呋喃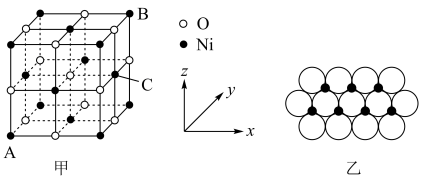
 B.
B. C.
C. D.
D.