填空题 适中0.65 引用1 组卷255
H与O可以形成 和
和 两种化合物。请回答:
两种化合物。请回答:
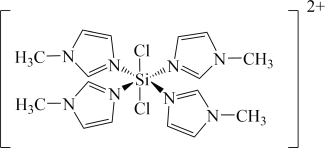
(1) 可与
可与 形成
形成 ,
, 的空间构型名称为
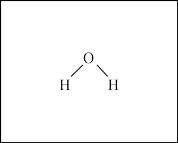
的空间构型名称为___________ 。根据 的成键特点,画出与下图中
的成键特点,画出与下图中 分子直接相连的所有氢键
分子直接相连的所有氢键_____ (用O—H…O表示)。
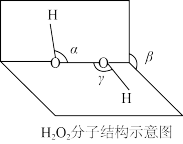
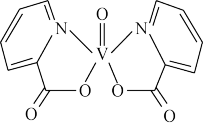
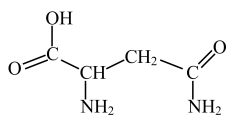
(2) 分子结构如图所示,
分子结构如图所示, 、
、 、
、 中相等的角是
中相等的角是___________ , 是
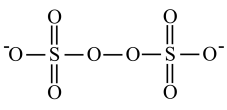
是___________ 分子(填“极性”或“非极性”)。 晶体中有4种作用力:①
晶体中有4种作用力:① 键、②
键、② 键、③范德华力、④氢键,这4种作用力由强到弱依次为:
键、③范德华力、④氢键,这4种作用力由强到弱依次为:___________ 。
(3)哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。根据以上原理,下列金属离子不能催化双氧水分解的是___________
A. B.
B. C.
C. D.
D. E.
E.
(4)实验测得,25℃时 的
的 小于
小于 的
的 ,原因是
,原因是___________ (运用物质结构原理解释)。
(1)

(2)

(3)哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。根据以上原理,下列金属离子不能催化双氧水分解的是
A.
(4)实验测得,25℃时
21-22高二下·浙江台州·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 )反应可以得到
)反应可以得到