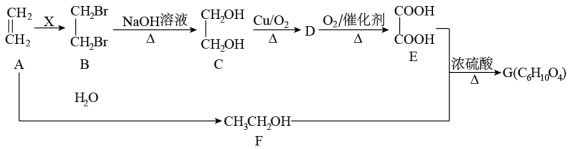
填空题 适中0.65 引用1 组卷231
二甲醚(CH3OCH3)气体是一种可再生绿色新能源,被誉为“21 世纪的清洁燃料”。
(1)写出二甲醚一种同分异构体的结构简式:___________ 。
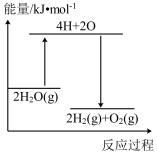
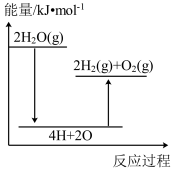
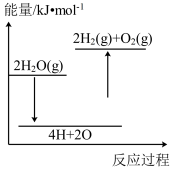
(2)已知:4.6g二甲醚气体完全燃烧生成液态水放出 145.5kJ 热量,写出其燃烧的热化学反应方程式___________ 。
(3)工业上可用水煤气合成二甲醚:2CO(g) + 4H2(g)⇌CH3OCH3(g) + H2O(g)
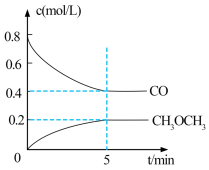
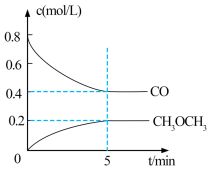
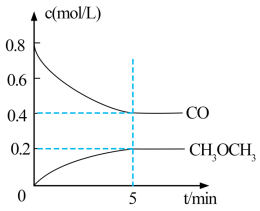
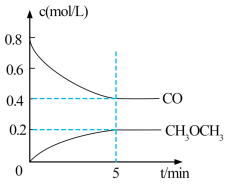
①测得 CO 和 CH3OCH3(g)的浓度随时间变化如图所示,则反应开始至平衡时的 H2平均反应速率v(H2)=___________ mol/(L·min )。
②该反应在恒容密闭容器中进行,下列叙述中能表示该反应达到平衡状态的是___________ 。
A.单位时间内生成CO和H2的物质的量之比为1﹕2
B.CH3OCH3的浓度不再变化
C.容器内压强不再变化
D.CH3OCH3与H2O的物质的量相等
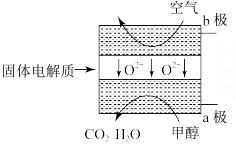
(4)二甲醚燃料电池工作原理如图所示
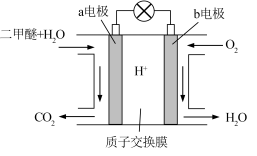
①该电池的负极是___________ (填“a 电极”或“b 电极”)
②H+通过质子交换膜时的移动方向是___________ 。(填选项字母)
A.从左向右 B.从右向左
③通入O2的电极反应式是___________ 。
(5)标况下每转移6mol电子需要氧气多少L______ ?(写出解题过程)
(1)写出二甲醚一种同分异构体的结构简式:
(2)已知:4.6g二甲醚气体完全燃烧生成液态水放出 145.5kJ 热量,写出其燃烧的热化学反应方程式
(3)工业上可用水煤气合成二甲醚:2CO(g) + 4H2(g)⇌CH3OCH3(g) + H2O(g)
①测得 CO 和 CH3OCH3(g)的浓度随时间变化如图所示,则反应开始至平衡时的 H2平均反应速率v(H2)=

②该反应在恒容密闭容器中进行,下列叙述中能表示该反应达到平衡状态的是
A.单位时间内生成CO和H2的物质的量之比为1﹕2
B.CH3OCH3的浓度不再变化
C.容器内压强不再变化
D.CH3OCH3与H2O的物质的量相等
(4)二甲醚燃料电池工作原理如图所示

①该电池的负极是
②H+通过质子交换膜时的移动方向是
A.从左向右 B.从右向左
③通入O2的电极反应式是
(5)标况下每转移6mol电子需要氧气多少L
21-22高一下·江苏盐城·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 D.
D.