单选题 适中0.65 引用2 组卷543
下列说法不正确的是
| A.某价层电子排布为3d24s2的基态原子,该元素位于周期表中第四周期第IVB族 |
| B.在元素周期表中,s区、d区和ds区的元素都是金属元素 |
C.当碳原子的核外电子排布由 转变为 转变为 时,释放能量,由激发态转化成基态 时,释放能量,由激发态转化成基态 |
| D.非金属元素形成的共价化合物中,原子的最外层电子数不一定是2或8 |
21-22高二下·黑龙江双鸭山·阶段练习
类题推荐
下列各项叙述中,正确的是( )
| A.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
| B.价电子排布为3d104s1的元素位于第四周期ⅠA族,是s区元素 |
| C.硅有14种不同运动状态的电子 |
| D.p轨道电子能量一定高于s轨道电子能量 |
下列各项叙述中,正确的是
| A.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
| B.价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |
C.由图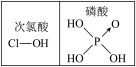 知酸性:H3PO4>HClO,因为H3PO4中非羟基氧原子数大于次氯酸中非羟基氧原子数 知酸性:H3PO4>HClO,因为H3PO4中非羟基氧原子数大于次氯酸中非羟基氧原子数 |
| D.元素周期表中s区、d区和ds区的元素都是金属元素 |
下列各项叙述中,正确的是
| A.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
| B.24Cr原子的电子排布式是1s22s22p63s23p63d44s2 |
| C.所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同 |
| D.价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


