单选题 适中0.65 引用3 组卷207
工业上可用PbO2来制备KClO4。在酸性条件下,PbO2与NaClO3反应生成NaClO4。过滤,向滤液中加入KNO3,常温下结晶可得KClO4晶体。下列说法错误的是
| A.NaClO3与PbO2反应中,PbO2作氧化剂 |
| B.常温下KClO4的溶解度比NaClO4小 |
| C.21.3gNaClO3完全反应,转移电子0.2mol |
| D.由上述反应得知氧化性:PbO2>NaClO4 |
21-22高一下·重庆·阶段练习
类题推荐
工业用强氧化剂 PbO2来制备 KClO4的工业流程如图:
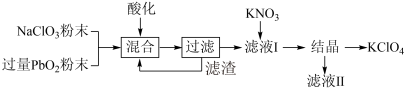
下列判断不正确的是

下列判断不正确的是
| A.“滤渣”的主要成分是 PbO2,可循环使用 |
| B.“酸化”的试剂可用浓盐酸 |
| C.NaClO3与 PbO2反应的物质的量之比为1:1 |
| D.在滤液1中加入 KNO3制得 KClO4利用的是体系中各物质溶解度不同 |
高氯酸钾是一种强氧化剂和分析试剂,易溶于水。以氯化钠为原料制备高氯酸钾的一种流程如图所示。下列说法错误的是
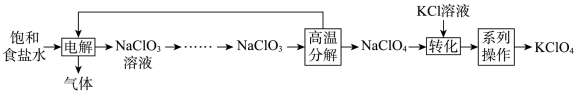

| A.“电解”过程中阴极生成气体的主要成分为H2 |
| B.“高温分解”反应中氧化剂和还原剂的物质的量之比为3:1 |
| C.本实验条件下,KClO4在水中的溶解度比NaClO4小 |
| D.“转化”过程所得副产物也可在上述流程中循环利用 |
工业用强氧化剂PbO2来制备KClO4的工业流程如下:
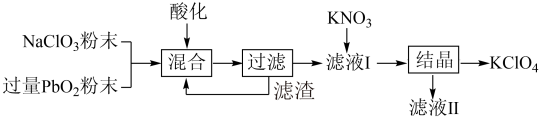
根据流程推测,下列判断不正确的是

根据流程推测,下列判断不正确的是
| A.“酸化”的试剂是稀硝酸或浓盐酸 |
| B.“滤渣”主要成分是PbO2粉末,可循环使用 |
| C.NaClO3与PbO2反应的离子方程式为 |
| D.在KNO3、KClO4、NaClO4、NaNO3中,常温下溶解度小的是KClO4 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


