解答题-原理综合题 适中0.65 引用1 组卷60
按要求回答以下内容。
(1)已知H2的燃烧热285.8kJ/mol,写出液态水电解生成H2和O2的热化学方程式_______ ;
(2)已知2SO2(g)+O2(g) 2SO3(g) ΔH=-197 kJ/mol,相同温度和压强下,4molSO2和2molO2充入容器中反应至平衡时放出的能量为Q kJ,则Q
2SO3(g) ΔH=-197 kJ/mol,相同温度和压强下,4molSO2和2molO2充入容器中反应至平衡时放出的能量为Q kJ,则Q_______ 394kJ(填“>”“<”或“=”)
甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇:
反应I:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
反应II:CO(g)+2H2(g) CH3OH(g) ΔH2
CH3OH(g) ΔH2
下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K)
(3)由表中数据判断ΔH2 _______ 0(填“>”、“<”或“=”)。
(4)若容器容积不变,下列措施可增加甲醇产率的是_______ 。
A.升高温度
B.将CH3OH(g)从体系中分离
C.使用合适的催化剂
D.恒温恒容充入He,使体系总压强增大
E.按原比例再充入CO和H2
(5)某温度下,将2 mol CO和6 mol H2充入2L的恒容密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol·L-1,则CO的转化率为_______ ,此时的温度为_______ (从上表中选择);
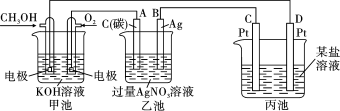
按如图所示装置进行实验,并回答下列问题:

(6)甲池,通入CH3OH(甲醇)的电极反应式为_______ 。
(7)乙池中的总反应化学方程式为_______ 。
(8)当甲池中消耗O2为0.56L(标准状况下)时,理论上乙池中B极的质量增加_______ g;此时丙装置中_______ (填“C”或“D”)电极析出3.20g金属,则按丙装置中的的某盐溶液可能是_______ (填序号)。
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
(1)已知H2的燃烧热285.8kJ/mol,写出液态水电解生成H2和O2的热化学方程式
(2)已知2SO2(g)+O2(g)
甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇:
反应I:CO2(g)+3H2(g)
反应II:CO(g)+2H2(g)
下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
(4)若容器容积不变,下列措施可增加甲醇产率的是
A.升高温度
B.将CH3OH(g)从体系中分离
C.使用合适的催化剂
D.恒温恒容充入He,使体系总压强增大
E.按原比例再充入CO和H2
(5)某温度下,将2 mol CO和6 mol H2充入2L的恒容密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol·L-1,则CO的转化率为
按如图所示装置进行实验,并回答下列问题:

(6)甲池,通入CH3OH(甲醇)的电极反应式为
(7)乙池中的总反应化学方程式为
(8)当甲池中消耗O2为0.56L(标准状况下)时,理论上乙池中B极的质量增加
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
21-22高二下·四川成都·阶段练习
类题推荐
碳及其化合物应用广泛。
I.工业上利用CO和水蒸气反应制氢气,存在以下平衡:
CO(g)+H2O(g) CO2(g)+H2(g)△H>0
CO2(g)+H2(g)△H>0
(1)向1L恒容密闭容器中注入CO(g)和H2O(g),830℃时测得部分数据如下表。则该温度下反应的平衡常数K=______________ 。
(2)相同条件下,向1L恒容密闭容器中,同时注入2mol CO、2mol H2O(g),1molCO2和1molH2,此时v(正 ) __________ v(逆)(填“>”“=”或“<”)
(3)上述反应达到平衡时,要提高CO的转化率,可采取的措施是_______ (填字母代号)。
A.升高温度
B.加入催化剂
C.增大压强
D.增加CO的浓度
E.及时分离出CO2
II.已知CO(g)+1/2 O2(g)=CO2(g) △H=-141 kJ·mol-1
2H2(g)+ O2(g)=2H2O(g) △H=-484 kJ·mol-1
CH3OH(1)+3/2O2(g)=CO2(g)+2H2O(g) △H=-726 kJ·mol-1
(4)用CO(g)、H2(g)化合制得液态甲醇的热化学方程式为___________________________ 。
III.某同学设计了一个甲醇燃料电池,并用该电池电解100mL一定浓度NaCl与CuSO4混合溶液,其装置如图:
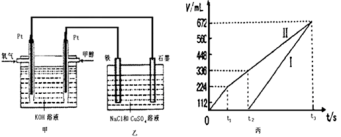
(5)写出甲中通入甲醇这一极的电极反应式__________________________________ 。
(6)理论上乙中两极所得气体的体积随时间变化的关系如丙图所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式____________ ,原混合溶液中CuSO4的物质的量浓度____________ mol/L。(假设溶液体积不变)
(7)将在t2时所得的溶液稀释至200mL,该溶液的pH约为___________ 。
I.工业上利用CO和水蒸气反应制氢气,存在以下平衡:
CO(g)+H2O(g)
(1)向1L恒容密闭容器中注入CO(g)和H2O(g),830℃时测得部分数据如下表。则该温度下反应的平衡常数K=
| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n( CO)/mol | 0.200 | 0.160 | 0.125 | 0.099 | 0.080 | 0.080 |
| n( H2O)/mol | 0.300 | 0.260 | 0.225 | 0.199 | 0.180 | 0.180 |
(3)上述反应达到平衡时,要提高CO的转化率,可采取的措施是
A.升高温度
B.加入催化剂
C.增大压强
D.增加CO的浓度
E.及时分离出CO2
II.已知CO(g)+1/2 O2(g)=CO2(g) △H=-141 kJ·mol-1
2H2(g)+ O2(g)=2H2O(g) △H=-484 kJ·mol-1
CH3OH(1)+3/2O2(g)=CO2(g)+2H2O(g) △H=-726 kJ·mol-1
(4)用CO(g)、H2(g)化合制得液态甲醇的热化学方程式为
III.某同学设计了一个甲醇燃料电池,并用该电池电解100mL一定浓度NaCl与CuSO4混合溶液,其装置如图:

(5)写出甲中通入甲醇这一极的电极反应式
(6)理论上乙中两极所得气体的体积随时间变化的关系如丙图所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式
(7)将在t2时所得的溶液稀释至200mL,该溶液的pH约为
Ⅰ.能源短缺是人类面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用如下反应合成甲醇:CO(g)+2H2(g) CH3OH(g)ΔH
CH3OH(g)ΔH
下表所列数据是该反应在不同温度下的化学平衡常数(K):
①由表中数据判断ΔH_____ (填“>”“<”或“=”)0。
②若容器容积不变,下列措施可增大甲醇产率的是_____ (填字母)。
A.升高温度B.将CH3OH(g)从体系中分离
C.使用合适的催化剂D.充入He,使体系总压强增大
E.按原比例再充入CO和H2
③某温度下,将2molCO和6molH2充入2L的恒容密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol·L-1,则CO的转化率为_____ 。
④恒温恒压下,1molCO和nmolH2在一个容积可变的密闭容器中反应达到平衡后,生成amolCH3OH。若起始时充入3molCO、3nmolH2,则达平衡时生成CH3OH的物质的量为_____ mol。
Ⅱ.25℃时,CH3COOH、H2CO3、HClO的电离平衡常数如下:
(2)下列四种离子结合H+的能力由强到弱的顺序是_____ (填字母,下同)。
A. B.ClO-C.CH3COO-D.
B.ClO-C.CH3COO-D.
(3)下列反应不能 发生的是_____ 。
A. +2CH3COOH
+2CH3COOH 2CH3COO-+CO2↑+H2OB.ClO-+CH3COOH
2CH3COO-+CO2↑+H2OB.ClO-+CH3COOH CH3COO-+HClO
CH3COO-+HClO
C. +2HClO
+2HClO CO2↑+H2O+2ClO-D.2ClO-+CO2+H2O
CO2↑+H2O+2ClO-D.2ClO-+CO2+H2O
 +2HClO
+2HClO
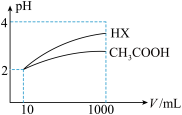
(4)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH的变化如图,则HX的电离平衡常数_____ 醋酸的电离平衡常数(填“大于”“等于”或“小于”),稀释后,HX溶液中水电离出来的c(H+)_____ 醋酸溶液中水电离出来的c(H+)(填“大于”“等于”或“小于”)。
(1)工业上一般采用如下反应合成甲醇:CO(g)+2H2(g)
 CH3OH(g)ΔH
CH3OH(g)ΔH下表所列数据是该反应在不同温度下的化学平衡常数(K):
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
①由表中数据判断ΔH
②若容器容积不变,下列措施可增大甲醇产率的是
A.升高温度B.将CH3OH(g)从体系中分离
C.使用合适的催化剂D.充入He,使体系总压强增大
E.按原比例再充入CO和H2
③某温度下,将2molCO和6molH2充入2L的恒容密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol·L-1,则CO的转化率为
④恒温恒压下,1molCO和nmolH2在一个容积可变的密闭容器中反应达到平衡后,生成amolCH3OH。若起始时充入3molCO、3nmolH2,则达平衡时生成CH3OH的物质的量为
Ⅱ.25℃时,CH3COOH、H2CO3、HClO的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(2)下列四种离子结合H+的能力由强到弱的顺序是
A.
(3)下列反应
A.
 2CH3COO-+CO2↑+H2OB.ClO-+CH3COOH
2CH3COO-+CO2↑+H2OB.ClO-+CH3COOH CH3COO-+HClO
CH3COO-+HClOC.
 CO2↑+H2O+2ClO-D.2ClO-+CO2+H2O
CO2↑+H2O+2ClO-D.2ClO-+CO2+H2O
(4)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH的变化如图,则HX的电离平衡常数

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网