解答题-原理综合题 较难0.4 引用1 组卷335
苯酚( )是一种广泛使用的化工产品,但若在水体中存在超标又会导致严重的污染。
)是一种广泛使用的化工产品,但若在水体中存在超标又会导致严重的污染。
I.现有一种在一定温度下用某分子筛催化 废气氧化苯制备苯酚的新方法,方程式为:
废气氧化苯制备苯酚的新方法,方程式为: 。
。
(1)已知: (s,石墨)
(s,石墨)



 (s,石墨)
(s,石墨)

则

_______ 。
(2)以固定 和苯酚比例、恒定流速、
和苯酚比例、恒定流速、 加入量为1%的条件下,考查单因素改变反应温度时对
加入量为1%的条件下,考查单因素改变反应温度时对 转化率和苯酚选择性的影响如图1和图2所示。
转化率和苯酚选择性的影响如图1和图2所示。
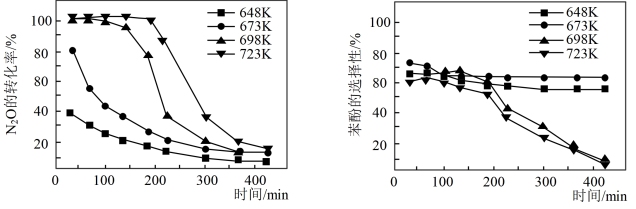
①由图1可见,在723K进行反应时, 的初始转化率很高,随着反应时间的延续,
的初始转化率很高,随着反应时间的延续, 转化率迅速降低,究其原因可能是
转化率迅速降低,究其原因可能是_______ 。
②由图2可见,在648K和673K反应时,苯酚的选择性基本保持恒定,而在698K和723K时,苯酚选择性随着反应进行迅速下降,高温时苯酚选择性下降的原因可能是:_______ 。
II.以苯酚为原料化合成某有机物的反应机理如图所示(图中个别反应物未列出,Ph为苯环):
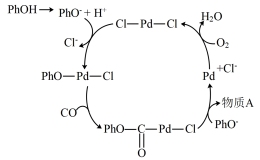
(3)过程中生成的物质A的结构简式为_______ 。
III.Fenton试剂氧化法是一种很好的除去废水中苯酚的方法。Fenton试剂是由亚铁盐和过氧化氢组成, 单独处理有机废水时,由于本身的氧化性能较差,很难达到理想的处理效果;而当
单独处理有机废水时,由于本身的氧化性能较差,很难达到理想的处理效果;而当 联合处理有机废水时,
联合处理有机废水时, 反应生成了氧化性能极强的
反应生成了氧化性能极强的 ,使废水中的苯酚得到降解。
,使废水中的苯酚得到降解。
(4)当总质量一定时, 与
与 的质量之比过小或过大,处理苯酚的效果均较差,请分析可能的原因:
的质量之比过小或过大,处理苯酚的效果均较差,请分析可能的原因:_______ 。
I.现有一种在一定温度下用某分子筛催化
(1)已知:
则
(2)以固定

①由图1可见,在723K进行反应时,
②由图2可见,在648K和673K反应时,苯酚的选择性基本保持恒定,而在698K和723K时,苯酚选择性随着反应进行迅速下降,高温时苯酚选择性下降的原因可能是:
II.以苯酚为原料化合成某有机物的反应机理如图所示(图中个别反应物未列出,Ph为苯环):

(3)过程中生成的物质A的结构简式为
III.Fenton试剂氧化法是一种很好的除去废水中苯酚的方法。Fenton试剂是由亚铁盐和过氧化氢组成,
(4)当总质量一定时,
21-22高三下·江苏南京·阶段练习
类题推荐
Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
【实验设计】
控制p-CP的初始浓度相同,恒定实验温度在298 K或313 K(其余实验条件见下表),设计如下对比实验:
(1)请完成以下实验设计表。
【数据处理】
实验测得p-CP的浓度随时间变化的关系如图所示。___________ mol·L-1·s-1。
【解释与结论】
(3)实验①、②表明温度升高,降解反应速率增大。但后续研究表明:温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:___________ 。
(4)实验③得出的结论是:pH等于10时,反应___________ (填“能”或“不能”)进行。
【思考与交流】
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:___________ 。
【实验设计】
控制p-CP的初始浓度相同,恒定实验温度在298 K或313 K(其余实验条件见下表),设计如下对比实验:
(1)请完成以下实验设计表。
| 实验编号 | 实验目的 | T/K | pH | c/10-3 mol·L-1 | |
| H2O2 | Fe2+ | ||||
| ① | 为以下实验作参照 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 | 3 | |||
| ③ | 298 | 10 | 6.0 | 0.30 | |
【数据处理】
实验测得p-CP的浓度随时间变化的关系如图所示。
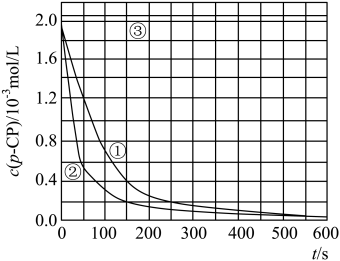
【解释与结论】
(3)实验①、②表明温度升高,降解反应速率增大。但后续研究表明:温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:
(4)实验③得出的结论是:pH等于10时,反应
【思考与交流】
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:
Fenton法常用于处理含难降解有机物的工业废水。通常是在H+和Fe2+浓度一定的废水中加入H2O2,利用反应产生的羟基自由基能氧化降解污染物,现运用该方法降解有机污染物p-CP,试探究有关因素对该降解反应速率的影响。实验中控制p-CP的初始浓度为2.0×10-3mol·L-1,恒定实验温度在298K或313K(其余实验条件见下表)设计如下对比实验。
(1)其中实验①、②的目的是___________ 。实验①、③的目的是___________ 。
(2)测得实验①、②、③中p-CP的浓度随时间变化的关系如下图所示。

请根据上图实验①曲线,计算降解反应在50-450s内的平均反应速率,v(P-CP)=___________ ,以及450s时p-CP的降解率___________ 。
(3)实验①②表明适当升高温度,降解反应速率___________ (填写“增大”“减小”或“不变”)。但温度过高反而导致降解反应速率出现反常,请从所用试剂H2O2的角度分析原因___________ 。
(4)实验③得出的结论是:当废水中的c(H+)=10-10moL·L-1时,___________ 。
| 实验编号 | T/K | 废水中的c(H+)/ moL·L-1 | c/10-3 moL·L-1 | |
| H2O2 | Fe2+ | |||
| ① | 298 | 10-3 | 6.0 | 0.30 |
| ② | 313 | 10-3 | 6.0 | 0.30 |
| ③ | 298 | 10-10 | 6.0 | 0.30 |
(2)测得实验①、②、③中p-CP的浓度随时间变化的关系如下图所示。

请根据上图实验①曲线,计算降解反应在50-450s内的平均反应速率,v(P-CP)=
(3)实验①②表明适当升高温度,降解反应速率
(4)实验③得出的结论是:当废水中的c(H+)=10-10moL·L-1时,
Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物pCP,探究有关因素对该降解反应速率的影响。
[实验设计]控制pCP的初始浓度相同,恒定实验温度在298 K或313 K(其余实验条件见下表),设计如下对比实验。
(1)请完成以下实验设计表(表中不要留空格)。
[数据处理]实验测得pCP的浓度随时间变化的关系如图:
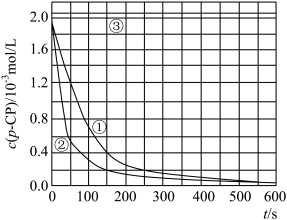
(2)请根据图中实验①曲线,列式并计算降解反应在50~150 s内的反应速率:________ 。
[解释与结论]
(3)实验①②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:____________ 。
(4)实验③得出的结论是:pH等于10时,_________________________ 。
[实验设计]控制pCP的初始浓度相同,恒定实验温度在298 K或313 K(其余实验条件见下表),设计如下对比实验。
(1)请完成以下实验设计表(表中不要留空格)。
| 编号 | 实验目的 | T/K | pH | c/10-3 mol/L | |
| H2O2 | Fe2+ | ||||
| ① | 为以下实验作参考 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 | ||||
| ③ | 298 | 10 | 6.0 | 0.30 | |

(2)请根据图中实验①曲线,列式并计算降解反应在50~150 s内的反应速率:
[解释与结论]
(3)实验①②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:
(4)实验③得出的结论是:pH等于10时,
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


