解答题-实验探究题 适中0.65 引用1 组卷88
三氧乙醛( )是生产农药、医药的重要中间体,实验室可用无水乙醇和氯气制备三氯乙醛:
)是生产农药、医药的重要中间体,实验室可用无水乙醇和氯气制备三氯乙醛: 。反应装置示意图(加热装置未画出)和有关数据如下:
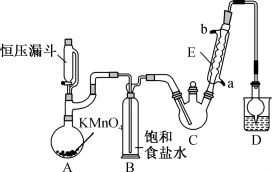
。反应装置示意图(加热装置未画出)和有关数据如下:
(1)恒压漏斗中所装的液体是_______ ,D中干燥管的作用是_______ 。
(2)E的具体名称是_______ ,冷凝水从_______ 口流入。(填“a”或“b”)
(3)反应时,装置C温度应保持在70℃左右,其原因是_______ 。(任答两点)
(4)已知 能被次氯酸氧化生成
能被次氯酸氧化生成 (三氯乙酸),所以该实验装置在设计流程中存在的一处明显缺陷是
(三氯乙酸),所以该实验装置在设计流程中存在的一处明显缺陷是_______ 。
(5)反应结束后,分离得到 的实验方法是应控制温度为
的实验方法是应控制温度为_______ 。
(6)某次实验用9.2g 进行实验,最终得到
进行实验,最终得到 20.0g,则产率为
20.0g,则产率为_______ %。(保留3位有效数字)
| 物质 | 物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ |
| 46 | -114.1 | 78.3 | 与水互溶 | |
| 147.5 | -57.5 | 97.8 | 可溶于水、乙醇 | |
| 163.5 | 58 | 198 | 可溶于水、乙醇、三氯乙醛 | |
| 64.5 | -138.7 | 12.3 | 微溶于水,可溶于乙醇 |
(2)E的具体名称是
(3)反应时,装置C温度应保持在70℃左右,其原因是
(4)已知
(5)反应结束后,分离得到
(6)某次实验用9.2g
21-22高二下·重庆渝中·阶段练习
类题推荐
三氯乙醛( )是生产农药、医药的重要中间体,实验室制备三氯乙醛的反应装置示意图(加热装置未画出)和有关数据如下:
)是生产农药、医药的重要中间体,实验室制备三氯乙醛的反应装置示意图(加热装置未画出)和有关数据如下:
①制备反应原理:
②反应过程中 和
和 可能会生成副产物
可能会生成副产物 ,同时
,同时 (三氯乙醛)也能被次氯酸继续氧化生成
(三氯乙醛)也能被次氯酸继续氧化生成 (三氯乙酸)
(三氯乙酸)
③相关物质的相对分子质量及部分物理性质:
回答下列问题:
(1)恒压漏斗中盛放的试剂的名称是_______ ,仪器A中发生反应的离子方程式为_______ 。
(2)仪器E的名称是_______ ,冷凝水的流向是_______ 。(用字母a、b回答)。
(3)该设计流程中存在一处缺陷是_______ ,导致的后果是_______ 。
(4)反应结束后,从C中的混合物中分离出 的方法是
的方法是_______ (填名称)。
(5)测定产品纯度:称取产品 配成待测溶液,加入
配成待测溶液,加入 碘标准溶液
碘标准溶液 ,再加入适量
,再加入适量 溶液,反应完全后,加盐酸调节溶液的
溶液,反应完全后,加盐酸调节溶液的 ,立即用
,立即用 溶液滴定至终点进行三次平行实验,测得平均消耗
溶液滴定至终点进行三次平行实验,测得平均消耗 溶液
溶液 。则产品的纯度为
。则产品的纯度为_______ %。滴定原理: 、
、 、
、 。
。

①制备反应原理:
②反应过程中
③相关物质的相对分子质量及部分物理性质:
| 物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 46 | 78.3 | 与水互溶 | ||
| 147.5 | 97.8 | 可溶于水、乙醇 | ||
| 163.5 | 58 | 198 | 可溶于水、乙醇、三氯乙醛 | |
| 64.5 | 12.3 | 微溶于水,可溶于乙醇 |
(1)恒压漏斗中盛放的试剂的名称是
(2)仪器E的名称是
(3)该设计流程中存在一处缺陷是
(4)反应结束后,从C中的混合物中分离出
(5)测定产品纯度:称取产品
三氯乙醛(CCl3CHO)是生产农药、医药的重要中间体,实验室制备三氯乙醛的反应装置示意图(加热装置未画出)和有关数据如图:
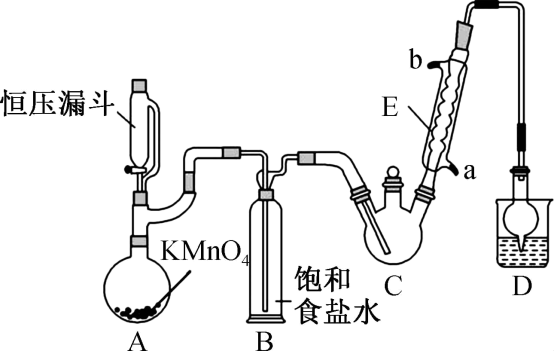
①制备反应原理:C2H5OH+4Cl2→CC13CHO+5HCl
②反应过程中C2H5OH和HCl可能会生成副产物C2H5Cl,同时CCl3CHO(三氯乙醛)也能被次氯酸继续氧化生成CC13COOH(三氯乙酸)
③相关物质的相对分子质量及部分物理性质:
回答下列问题:
(1)仪器A中发生反应的离子方程式为___ 。
(2)仪器E的名称是__ ,冷凝水的进水口是___ (用字母a、b回答)。
(3)该设计流程中存在处缺陷是___ ,导致的后果是___ 。
(4)反应结束后,从C中的混合物中分离出CC13CHO的方法是___ (填名称)。
(5)测定产品纯度:称取产品0.36g配成待测溶液,加入0.1000mol·L-1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000mol·L-1Na2S2O3溶液滴定至终点。进行三次平行实验,测得平均消耗Na2S2O3溶液20.00mL。则产品的纯度为___ %。(保留2位小数)
滴定原理:CC13CHO+OH-=CHCl3+HCOO-、HCOO-+I2=H++2I-+CO2、I2+2S2O =2I-+S4O
=2I-+S4O

①制备反应原理:C2H5OH+4Cl2→CC13CHO+5HCl
②反应过程中C2H5OH和HCl可能会生成副产物C2H5Cl,同时CCl3CHO(三氯乙醛)也能被次氯酸继续氧化生成CC13COOH(三氯乙酸)
③相关物质的相对分子质量及部分物理性质:
| 物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 |
| C2H5OH | 46 | -114.1 | 78.3 | 与水互溶 |
| CC13CHO | 147.5 | -57.5 | 97.8 | 可溶于水、乙醇 |
| CC13COOH | 163.5 | 58 | 198 | 可溶于水、乙醇、三氯乙醛 |
| C2H5Cl | 64.5 | 一138.7 | 12.3 | 微溶于水,可溶于乙醇 |
(1)仪器A中发生反应的离子方程式为
(2)仪器E的名称是
(3)该设计流程中存在处缺陷是
(4)反应结束后,从C中的混合物中分离出CC13CHO的方法是
(5)测定产品纯度:称取产品0.36g配成待测溶液,加入0.1000mol·L-1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000mol·L-1Na2S2O3溶液滴定至终点。进行三次平行实验,测得平均消耗Na2S2O3溶液20.00mL。则产品的纯度为
滴定原理:CC13CHO+OH-=CHCl3+HCOO-、HCOO-+I2=H++2I-+CO2、I2+2S2O
三氯乙醛是基本有机合成原料之一,是生产农药、医药的重要中间体。某化学兴趣小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验。
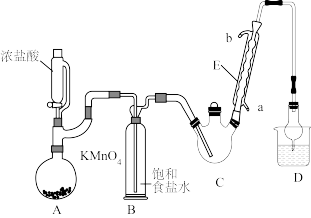
查阅资料,有关信息如下:
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O、CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的相对分子质量及部分物理性质:
(1)仪器E的名称是____________ ,冷凝水的流向是________ 进_______ 出(填“a”或“b”)。
(2)该设计流程中存在一处缺陷,该缺陷是__________ ,引起的后果是_________________ 。
(3)仪器A中发生反应的离子方程式为____________________ 。
(4)该装置C可采用_______________ ,加热的方法以控制反应温度在70℃左右。
(5)装置D干燥管的作用为_______________ ,装置D烧杯中的试剂是_______________ 。
(6)反应结束后,从C中的混合物中分离出Cl3CCOOH的方法是____________ (填名称)。
(7)已知:常温下Ka(CCl3COOH)=1.0×10-1mol·L-1,Ka(CH3COOH)=1.7×10-5mol·L-1,请设计实验证明三氯乙酸、乙酸的酸性强弱:____________________________ 。

查阅资料,有关信息如下:
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O、CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的相对分子质量及部分物理性质:
| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
(1)仪器E的名称是
(2)该设计流程中存在一处缺陷,该缺陷是
(3)仪器A中发生反应的离子方程式为
(4)该装置C可采用
(5)装置D干燥管的作用为
(6)反应结束后,从C中的混合物中分离出Cl3CCOOH的方法是
(7)已知:常温下Ka(CCl3COOH)=1.0×10-1mol·L-1,Ka(CH3COOH)=1.7×10-5mol·L-1,请设计实验证明三氯乙酸、乙酸的酸性强弱:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


