多选题 适中0.65 引用2 组卷331
直接排放含SO2的烟气会形成酸雨,用Na2SO3作为吸收液可吸收SO2,且吸收液可通过电解再生。室温条件下,吸收液吸收SO2的过程中,pH随n(SO ):n(HSO
):n(HSO )变化关系如表;当吸收液pH降至约为6时,需送至电解槽再生,再生示意图如图,下列说法不正确的是
)变化关系如表;当吸收液pH降至约为6时,需送至电解槽再生,再生示意图如图,下列说法不正确的是
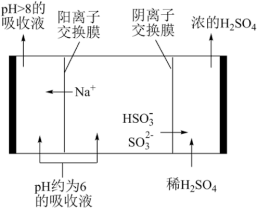
| n(SO | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
| A.由表中信息可推测,Na2SO3溶液显碱性,NaHSO3溶液显酸性 |
| B.吸收过程中离子浓度关系总有c(Na+)+c(H+)=2c(SO |
| C.电解槽右侧电极发生的反应主要是SO |
| D.电解槽左侧电极发生的反应有2HSO |
2022·山东东营·模拟预测
类题推荐
直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)用化学方程式表示SO2形成硫酸型酸雨的反应:______________ 。
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是________________________
(3)吸收液吸收SO2的过程中,pH随n(SO3²﹣):n(HSO3﹣)变化关系如下表:
①上表判断NaHSO3溶液显______ 性,用化学平衡原理解释:____________
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):____________
a.c(Na+)=2c(SO32-)+c(HSO3-),
b.c(Na+)> c(HSO3-)> c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)= c(SO32-)+ c(HSO3-)+c(OH-)
(4)当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下:
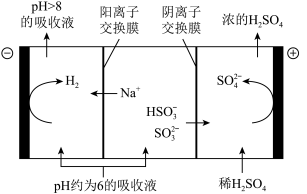
①HSO3-在阳极放电的电极反应式是_______________ 。
②当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理:__________
(1)用化学方程式表示SO2形成硫酸型酸雨的反应:
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是
(3)吸收液吸收SO2的过程中,pH随n(SO3²﹣):n(HSO3﹣)变化关系如下表:
| n(SO₃²﹣):n(HSO₃﹣) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):
a.c(Na+)=2c(SO32-)+c(HSO3-),
b.c(Na+)> c(HSO3-)> c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)= c(SO32-)+ c(HSO3-)+c(OH-)
(4)当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下:

①HSO3-在阳极放电的电极反应式是
②当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理:
直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)在钠碱循环法中,利用Na2SO3溶液作为吸收液,吸收液可由NaOH溶液吸收SO2制得,该反应的离子方程式是_______ 。
(2)吸收液吸收SO2的过程中,pH随n(SO ):n(HSO
):n(HSO )变化关系如表:
)变化关系如表:
①由上表判断NaHSO3溶液显_______ 性,用化学平衡原理解释:_______ 。
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):_______ 。
a.c(Na+)=2c(SO )+c(HSO
)+c(HSO )
)
b.c(Na+)>c(HSO )>c(SO
)>c(SO )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(SO )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)
(3)当吸收液的pH降至约为6时,送至电解槽再生。再生示意图如图:HSO 在阳极放电的电极反应式是
在阳极放电的电极反应式是_______ 。
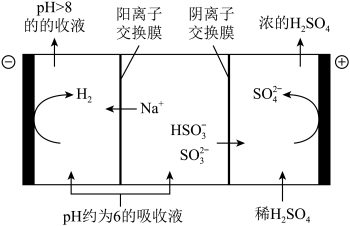
(1)在钠碱循环法中,利用Na2SO3溶液作为吸收液,吸收液可由NaOH溶液吸收SO2制得,该反应的离子方程式是
(2)吸收液吸收SO2的过程中,pH随n(SO
| n(SO | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
①由上表判断NaHSO3溶液显
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):
a.c(Na+)=2c(SO
b.c(Na+)>c(HSO
c.c(Na+)+c(H+)=c(SO
(3)当吸收液的pH降至约为6时,送至电解槽再生。再生示意图如图:HSO

硫及其化合物在生产生活中具有广泛应用。由自然界的硫磺和金属硫化物矿通过化学反应可得到SO2,SO2催化氧化生成SO3,其热化学方程式为2SO2(g)+O2(g) 2SO3(g) △H=-198kJ/mol。燃煤、金属冶炼和硫酸生产等产生的尾气中都含有SO2,用NaOH等碱性溶液吸收尾气中的SO2,可得到NaHSO3、Na2SO3等化工产品。直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法(Na2SO3溶液作为吸收液)可脱除烟气中的SO2。当吸收液的pH降至约为6时,送至电解槽再生。再生示意图如图所示:
2SO3(g) △H=-198kJ/mol。燃煤、金属冶炼和硫酸生产等产生的尾气中都含有SO2,用NaOH等碱性溶液吸收尾气中的SO2,可得到NaHSO3、Na2SO3等化工产品。直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法(Na2SO3溶液作为吸收液)可脱除烟气中的SO2。当吸收液的pH降至约为6时,送至电解槽再生。再生示意图如图所示:
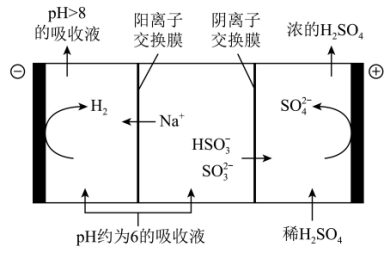
下列有关说法正确的是

下列有关说法正确的是
| A.该装置工作时,化学能转变为电能 |
| B.阴极反应式为:2H++2e-=H2↑ |
| C.阳极反应为:SO |
| D.根据中间室吸收液的成分,可推知:c(Na+)+c(H+)=c(SO |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


