解答题-实验探究题 适中0.65 引用4 组卷299
对氯苯氧乙酸是一种植物生长调节剂中间体,它的一种合成方法的原理如下:

副反应:ClCH2COOH + 2NaOH → HOCH2COONa+ NaCl+ H2O
已知:对氯苯氧乙酸在水中溶解度较小而在乙醇中溶解度较大。
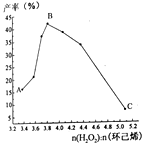
实验步骤:称取6.5g(0.05mol)对氯苯酚于仪器a(反应装置如图)中,加入10mL20%NaOH溶液,加入一定量KI溶液,在两恒压滴液漏斗中分别加入15 mL 20% NaOH溶液和5.3g氯乙酸水溶液。保持100~120° C加热,将两恒压滴液漏斗中的液体同时缓慢滴入仪器a中。反应完全后,停止加热,趁热将反应混合液倒入250 mL烧杯中,趁热边搅拌边滴加盐酸调pH至1,过滤得到对氯苯氧乙酸粗产品。
回答下列问题:
(1)仪器a的名称是____ ,保持反应温度在100~120 °C的加热方式为__ 。
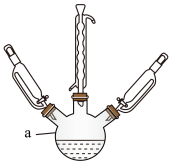
(2)经实验测定原料配比 对产率的影响如表所示。
对产率的影响如表所示。
工业上选撣的最佳原料配比为______ 。
(3)对氯苯氧乙酸钠在水中溶解度_____ (填“大”或“小”)。所得粗产品加入____ 溶解,再加入水,冷却结晶,过滤,冷水洗涤,真空干燥,得到对氯苯氧乙酸8.2 g,则产率为_____ %(保留两位有效数字)。

副反应:ClCH2COOH + 2NaOH → HOCH2COONa+ NaCl+ H2O
已知:对氯苯氧乙酸在水中溶解度较小而在乙醇中溶解度较大。
实验步骤:称取6.5g(0.05mol)对氯苯酚于仪器a(反应装置如图)中,加入10mL20%NaOH溶液,加入一定量KI溶液,在两恒压滴液漏斗中分别加入15 mL 20% NaOH溶液和5.3g氯乙酸水溶液。保持100~120° C加热,将两恒压滴液漏斗中的液体同时缓慢滴入仪器a中。反应完全后,停止加热,趁热将反应混合液倒入250 mL烧杯中,趁热边搅拌边滴加盐酸调pH至1,过滤得到对氯苯氧乙酸粗产品。

回答下列问题:
(1)仪器a的名称是
(2)经实验测定原料配比
| 产率(%) | |
| 1 : 1.00 1 : 1.05 1 : 1.10 1 : 1.20 | 76.1 81.5 90. 1 89.9 |
(3)对氯苯氧乙酸钠在水中溶解度
2022·辽宁锦州·模拟预测
类题推荐
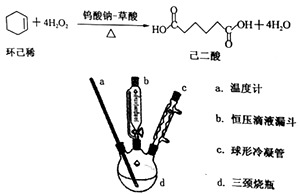
己二酸(HOOCCH2CH2CH2CH2COOH)是一种工业上有重要意义的二元酸,实验室利用环己醇(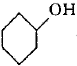 )合成己二酸的反应原理为:
)合成己二酸的反应原理为: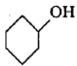 +8HNO3→HOOCCH2CH2CH2CH2COOH+8NO2↑+5H2O
+8HNO3→HOOCCH2CH2CH2CH2COOH+8NO2↑+5H2O
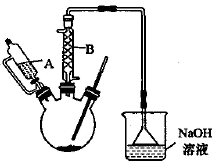
实验装置如下图:
可能用到的有关数据如下表所示:
实验步骤如下:
①在三口烧瓶中加入50mL50%硝酸(密度为 ),再加入1~2粒沸石,滴液漏斗中盛放5.4mL(5.2g)环己醇。
),再加入1~2粒沸石,滴液漏斗中盛放5.4mL(5.2g)环己醇。
②水浴加热三口烧瓶至50℃左右,移去水浴,逐滴加入5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩余的环己醇,维持反应温度在60~65℃之间。
③当环己醇全部加入后,将混合物用80~90℃水浴加热约10min(注意控制温度),直至_______为止。
④趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤得粗产品。
⑤粗产品经提纯后称重为5.2g。
回答下列问题:
(1)仪器B的名称为_______ 。
(2)步骤②环己醇要逐滴滴加的原因是_______ 。
(3)步骤③中,停止加热的判断依据是_______ 。
(4)烧杯中NaOH溶液的作用是_______ (用离子方程式表示)。
(5)步骤④中为了除去可能的杂质和减少产品损失,可分别用冰水和_______ 洗涤晶体。
(6)粗产品可用_______ 法(填实验操作名称)提纯。
(7)本实验所得己二酸产率为_______ 。(保留一位小数)
 )合成己二酸的反应原理为:
)合成己二酸的反应原理为: +8HNO3→HOOCCH2CH2CH2CH2COOH+8NO2↑+5H2O
+8HNO3→HOOCCH2CH2CH2CH2COOH+8NO2↑+5H2O实验装置如下图:

可能用到的有关数据如下表所示:
| 物质 | 熔点/℃ | 沸点/℃ | 溶解性 | 相对分子质量 |
| 环己醇 | 25.9 | 160.8 | 20℃时水中溶解度为3.6g,可溶于乙醇、苯 | 100 |
| 己二酸 | 152 | 337.5 | 在水中溶解度:15℃时为1.44g,25℃时为2.3g,易溶于乙醇,不溶于苯 | 146 |
①在三口烧瓶中加入50mL50%硝酸(密度为
②水浴加热三口烧瓶至50℃左右,移去水浴,逐滴加入5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩余的环己醇,维持反应温度在60~65℃之间。
③当环己醇全部加入后,将混合物用80~90℃水浴加热约10min(注意控制温度),直至_______为止。
④趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤得粗产品。
⑤粗产品经提纯后称重为5.2g。
回答下列问题:
(1)仪器B的名称为
(2)步骤②环己醇要逐滴滴加的原因是
(3)步骤③中,停止加热的判断依据是
(4)烧杯中NaOH溶液的作用是
(5)步骤④中为了除去可能的杂质和减少产品损失,可分别用冰水和
(6)粗产品可用
(7)本实验所得己二酸产率为
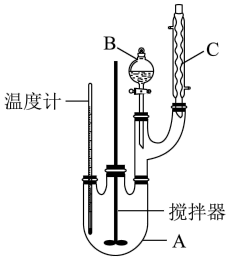
某科学小组制备硝基苯的实验装置如图,有关信息如下表:
实验步骤如下:
取100 mL烧杯,用20 mL浓硫酸与足量浓硝酸配制成混合酸,将混合酸小心地加入B中。把0.2mol(15.6 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,使溶液混合均匀。在50~60 °C下发生反应,直至反应结束。将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210 °C馏分,得到纯硝基苯18g。
回答下列问题:
(1)图中B仪器的名称为___________ ,图 中装置C的作用是___________ 。
(2)制备硝基苯的化学方程式为___________ 。
(3)为了使反应在50~60°C下进行,常用的加热方式是___________ 。反应结束并冷却至室温后A中液体就是粗硝基苯,粗硝基苯呈黄色的原因是___________ (用化学方程式说明),实验室常用氢氧化钠溶液除去该有色物质,涉及的离子方程式为___________ 。
(4)将粗产品置于分液漏斗中加水,振荡后静置,产物应在___________ (填“ 上”或“下”)层。
(5)本实验所得到的硝基苯的产率是___________ (结果保留 3位有效数字)。
| 物质 | 熔点/°C | 沸点/°C | 密度 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 不溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 浓硝酸 | — | 83 | 1.4 | 易溶于水 |
| 浓硫酸 | — | 338 | 1.84 | 易溶于水 |
取100 mL烧杯,用20 mL浓硫酸与足量浓硝酸配制成混合酸,将混合酸小心地加入B中。把0.2mol(15.6 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,使溶液混合均匀。在50~60 °C下发生反应,直至反应结束。将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210 °C馏分,得到纯硝基苯18g。

回答下列问题:
(1)图中B仪器的名称为
(2)制备硝基苯的化学方程式为
(3)为了使反应在50~60°C下进行,常用的加热方式是
(4)将粗产品置于分液漏斗中加水,振荡后静置,产物应在
(5)本实验所得到的硝基苯的产率是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网