解答题-工业流程题 适中0.65 引用3 组卷998
碳酸锶(SrCO3)难溶于水,主要用于电磁材料和金属冶炼。一种由工业碳酸锶(含少量Ba2+、Ca2+、 Mg2+、 Pb2+等 )制备高纯碳酸锶的工艺流程如下:
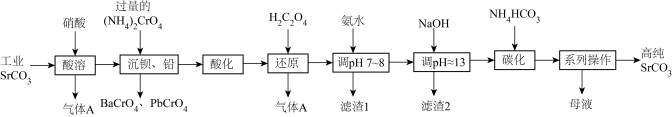
已知:I.Cr(OH)3为两性氢氧化物;
Ⅱ.常温下,各物质的溶度积常数如下表所示。
回答下列问题:
(1)气体A的电子式为_______ 。
(2)“除钡、铅”时,pH过低会导致(NH4)2CrO4的利用率降低,原因为_______ (结合化学用语解释);“还原”时发生反应的离子方程式为_______ 。
(3)“滤渣1”的主要成分为_______ (填化学式)。
(4)用氨水和NaOH分步调节pH,而不是直接调节溶液的pH≈13的原因为_______ 。
(5)“调pH≈13”后需对溶液进行煮沸并趁热过滤出滤渣2,煮沸并趁热过滤的原因为_______ 。
(6)已知:碳酸的电离常数Ka1=4.4×10-7、 Ka2= 4.7×10-11, 则“碳化”时,反应Sr2+(aq)+2 (aq)
(aq) SrCO3(s)+H2CO3(aq)的平衡常数 K =
SrCO3(s)+H2CO3(aq)的平衡常数 K =_______ (保留两位有效数字)。
(7)“系列操作”中,将结晶过滤后,不经洗涤,直接以200℃热风烘干,便可得高纯SrCO3,其原因是_______ 。

已知:I.Cr(OH)3为两性氢氧化物;
Ⅱ.常温下,各物质的溶度积常数如下表所示。
| 化合物 | Cr(OH)3 | Ca(OH)2 | Mg(OH)2 | SrCO3 |
| Ksp近似值 | 1×10-31 | 5.5×10-6 | 1.8×10-11 | 5.6×10-10 |
(1)气体A的电子式为
(2)“除钡、铅”时,pH过低会导致(NH4)2CrO4的利用率降低,原因为
(3)“滤渣1”的主要成分为
(4)用氨水和NaOH分步调节pH,而不是直接调节溶液的pH≈13的原因为
(5)“调pH≈13”后需对溶液进行煮沸并趁热过滤出滤渣2,煮沸并趁热过滤的原因为
(6)已知:碳酸的电离常数Ka1=4.4×10-7、 Ka2= 4.7×10-11, 则“碳化”时,反应Sr2+(aq)+2
(7)“系列操作”中,将结晶过滤后,不经洗涤,直接以200℃热风烘干,便可得高纯SrCO3,其原因是
2022·北京西城·三模
类题推荐
碳酸锶(SrCO3)难溶于水,主要用于电磁材料和金属冶炼。一种由工业碳酸锶(含少量Ba2+、Ca2+、Mg2+、Pb2+等)制备高纯碳酸锶的工艺流程如下:

已知:①Sr(OH)2为强碱,Cr(OH)3为两性氢氧化物;
②常温下,各物质的溶度积常数如表所示。
回答下列问题:
(1)气体A的电子式为_____________ 。
(2)“酸化”步骤发生如下反应: ,则“还原”时发生反应的离子方程式为
,则“还原”时发生反应的离子方程式为______________ 。
(3)滤渣1的主要成分为_____________ ,滤渣2的主要成分为_____________ (填化学式)。
(4)用氨水和NaOH分步调节pH,而不直接用NaOH调节溶液的pH≈13的原因是_____________ 。
(5)“碳化”时,反应 的化学平衡常数K的计算关系式为
的化学平衡常数K的计算关系式为_____________ 。(用相关平衡常数表达,已知碳酸的电离常数为Ka1、Ka2)
(6)上述流程合成的碳酸锶与TiO2在高温下反应,可以制得高温超导基片材料SrTiO3,SrTiO3的立方晶胞结构如图所示,其中Ti处在体心位置,Sr与Ti的最近距离为a nm,已知SrTiO3的相对分子质量为M,阿伏加德罗常数的值为NA,则SrTiO3晶体的密度为_____________ g/cm3(列出M、NA、a相关的算式即可)。


已知:①Sr(OH)2为强碱,Cr(OH)3为两性氢氧化物;
②常温下,各物质的溶度积常数如表所示。
| 化合物 | Cr(OH)3 | Ca(OH)2 | Mg(OH)2 | SrCO3 |
| Ksp近似值 |
(1)气体A的电子式为
(2)“酸化”步骤发生如下反应:
(3)滤渣1的主要成分为
(4)用氨水和NaOH分步调节pH,而不直接用NaOH调节溶液的pH≈13的原因是
(5)“碳化”时,反应
(6)上述流程合成的碳酸锶与TiO2在高温下反应,可以制得高温超导基片材料SrTiO3,SrTiO3的立方晶胞结构如图所示,其中Ti处在体心位置,Sr与Ti的最近距离为a nm,已知SrTiO3的相对分子质量为M,阿伏加德罗常数的值为NA,则SrTiO3晶体的密度为

高纯碳酸锶主要用于荧光玻璃、电子陶瓷、磁氧体和高科技领域。一种由工业级硝酸锶(含有Ba2+、Ca2+、Mg2+等杂质)制备高纯碳酸锶的工艺流程如下:
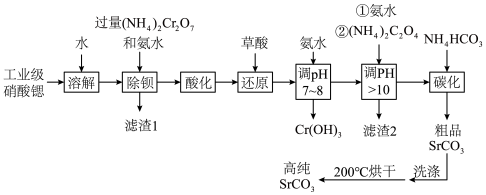
已知:①BaCrO4不溶于水,在水溶液中 与Ba2+不能结合。
与Ba2+不能结合。
② 在碱性条件下不能转化为Cr3+。
在碱性条件下不能转化为Cr3+。
③常温下,各物质的溶度积常数如下表所示:
回答下列问题:
(1)硝酸锶溶解前需要粉碎,其目的是___________ 。
(2)“除钡”时,pH偏低会导致 的利用率不高,原因是
的利用率不高,原因是___________ (用离子方程式解释);不同pH时 的利用率随时间变化曲线如图所示,分析“除钡”过程中需用氨水将溶液调至pH=
的利用率随时间变化曲线如图所示,分析“除钡”过程中需用氨水将溶液调至pH=___________ 。

(3)“还原”时发生反应的离子方程式为___________ 。
(4)“滤渣2”的成分主要是含镁物质和___________ (填化学式)。
(5)已知:碳酸的电离常数Ka1=4.5×10-7、Ka2=4.7×10-11,则“碳化”时,反应Sr2+(aq)+2 (aq)
(aq) SrCO3(s)+H2CO3(aq)的平衡常数K=
SrCO3(s)+H2CO3(aq)的平衡常数K=___________ (保留两位有效数字)。
(6)“洗涤”过程中能够除去SrCO3中的微量可溶性杂质,该杂质除NH4HCO3外还可能___________ (填化学式)。

已知:①BaCrO4不溶于水,在水溶液中
②
③常温下,各物质的溶度积常数如下表所示:
| 化合物 | Ca(OH)2 | CaC2O4 | Mg(OH)2 | MgC2O4 | SrCO3 |
| Ksp近似值 | 4.6×10-6 | 2.2×10-9 | 5.6×10-12 | 4.8×10-6 | 5.6×10-10 |
(1)硝酸锶溶解前需要粉碎,其目的是
(2)“除钡”时,pH偏低会导致

(3)“还原”时发生反应的离子方程式为
(4)“滤渣2”的成分主要是含镁物质和
(5)已知:碳酸的电离常数Ka1=4.5×10-7、Ka2=4.7×10-11,则“碳化”时,反应Sr2+(aq)+2
(6)“洗涤”过程中能够除去SrCO3中的微量可溶性杂质,该杂质除NH4HCO3外还可能
碳酸锶(SrCO3)难溶于水,主要用于电磁材料和金属冶炼。一种由工业碳酸锶(含少量Ba2+、Ca2+、Mg2+、Pb2+等)制备高纯碳酸锶的工艺流程如下:
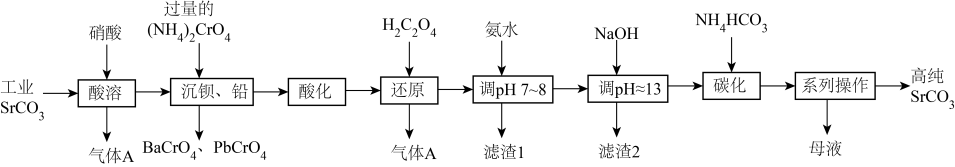
已知:①Sr(OH)2为强碱,Cr(OH)3为两性氢氧化物;
②常温下,各物质的溶度积常数如表所示。
回答下列问题:
(1)“酸溶”时能提高反应速率的措施有________________________ (答1条即可),基态Cr原子的价电子排布式是_____________ 。
(2)“酸化”步骤发生如下反应: ,则“还原”时发生反应的离子方程式为
,则“还原”时发生反应的离子方程式为____________________ 。
(3)滤渣1的主要成分为________ (填化学式)。
(4)用氨水和NaOH分步调节pH,而不直接用NaOH调节溶液的pH≈13的原因是________ 。
(5)“碳化”时,反应 的化学平衡常数K的计算关系式为
的化学平衡常数K的计算关系式为____________ 。(不用写出具体数值,用以下平衡常数表达:SrCO3的溶度积常数Ksp(SrCO3)、H2CO3的电离常数为Ka1、Ka2)
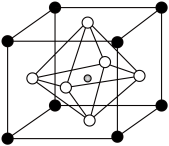
(6)上述流程合成的碳酸锶与TiO2在高温下反应,可以制得高温超导基片材料SrTiO3,SrTiO3的立方晶胞结构如图所示,其中Ti处在体心位置,晶胞边长为a nm,已知SrTiO3的相对分子质量为M,阿佛加德罗常数的值为NA,则SrTiO3晶体的密度为_____________ g/cm3(列出M、NA、a相关的算式即可)。

已知:①Sr(OH)2为强碱,Cr(OH)3为两性氢氧化物;
②常温下,各物质的溶度积常数如表所示。
| 化合物 | Cr(OH)3 | Ca(OH)2 | Mg(OH)2 | SrCO3 |
| Ksp近似值 |
回答下列问题:
(1)“酸溶”时能提高反应速率的措施有
(2)“酸化”步骤发生如下反应:
(3)滤渣1的主要成分为
(4)用氨水和NaOH分步调节pH,而不直接用NaOH调节溶液的pH≈13的原因是
(5)“碳化”时,反应
(6)上述流程合成的碳酸锶与TiO2在高温下反应,可以制得高温超导基片材料SrTiO3,SrTiO3的立方晶胞结构如图所示,其中Ti处在体心位置,晶胞边长为a nm,已知SrTiO3的相对分子质量为M,阿佛加德罗常数的值为NA,则SrTiO3晶体的密度为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


