解答题-工业流程题 适中0.65 引用1 组卷243
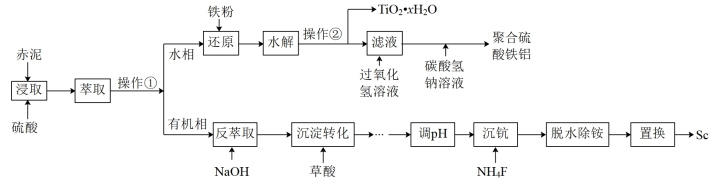
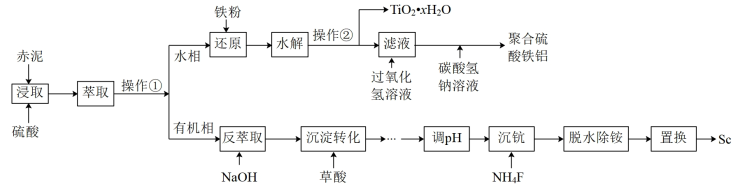
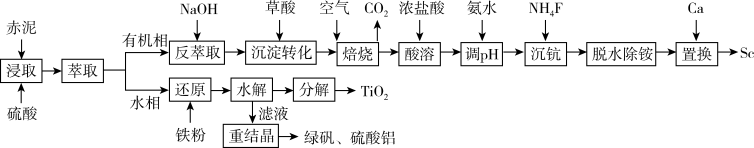
钪的价格昂贵,在地壳里的含量只有0.0005%。从铝土矿生产Al2O3的副产品“赤泥”(主要成分为Al2O3、Fe2O3、TiO2、Sc2O3)中回收钪,同时生产聚合硫酸铁铝[AlFe(OH)6-2n(SO4)n]具有极其重要的工业价值,一种工艺流程如图:
已知:钪离子可以在不同pH下生成[Sc(OH)n]3-n(n=1~6)。请回答以下问题:
(1)操作①和操作②中都使用的玻璃仪器是____ 。
(2)加入铁粉的作用:____ 。
(3)生成聚合硫酸铁铝[AlFe(OH)6-2n(SO4)n]沉淀,同时产生CO2,该反应的离子方程式为____ 。
(4)钪是一种重要的稀土金属,化学性质非常活泼,但发现较晚主要是因为____ 。
(5)“反萃取”时若加入的过量NaOH,则Sc(OH)3沉淀会溶解。写出Sc(OH)3与过量NaOH溶液反应生成n=6的含钪产物的化学方程式为____ 。
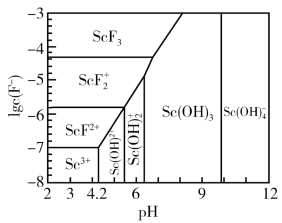
(6)常温下,三价Sc的部分存在形式与氟离子浓度的对数[1gc(F-)]、pH的关系如图所示。若溶液中c(F-)=5×10-6,“调pH”过程中控制pH=7,则调节pH后+3价Sc的存在形式为____ (填化学式)(lg5=0.7)。
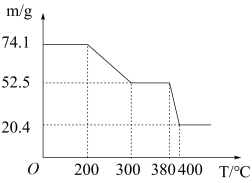
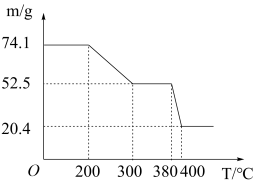
(7)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O分解得到ScF3,某固体样品质量与温度的关系如图所示。加热至380-400℃产生白烟,400℃以上质量不再改变。则a=____ (填数字)。

已知:钪离子可以在不同pH下生成[Sc(OH)n]3-n(n=1~6)。请回答以下问题:
(1)操作①和操作②中都使用的玻璃仪器是
(2)加入铁粉的作用:
(3)生成聚合硫酸铁铝[AlFe(OH)6-2n(SO4)n]沉淀,同时产生CO2,该反应的离子方程式为
(4)钪是一种重要的稀土金属,化学性质非常活泼,但发现较晚主要是因为
(5)“反萃取”时若加入的过量NaOH,则Sc(OH)3沉淀会溶解。写出Sc(OH)3与过量NaOH溶液反应生成n=6的含钪产物的化学方程式为
(6)常温下,三价Sc的部分存在形式与氟离子浓度的对数[1gc(F-)]、pH的关系如图所示。若溶液中c(F-)=5×10-6,“调pH”过程中控制pH=7,则调节pH后+3价Sc的存在形式为

(7)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O分解得到ScF3,某固体样品质量与温度的关系如图所示。加热至380-400℃产生白烟,400℃以上质量不再改变。则a=

2022·福建龙岩·模拟预测
类题推荐
从铝土矿废料“赤泥”(主要成分为Al2O3、Fe2O3、TiO2、Sc2O3)中提钪与TiO2的一种工艺流程如下:
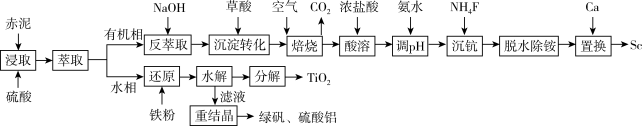
已知:该工艺条件下,溶液中相关离子开始沉淀和完全沉淀的pH值如下表:
(1)基态Sc原子的价电子排布式为___________ 。
(2)“沉淀转化”过程中,需加入过量的草酸,其原因是___________ 。
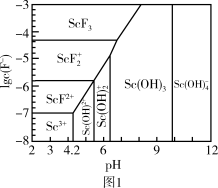
(3)“焙烧”过程中,生成Sc2O3的化学方程式为___________ 。
(4)常温下,三价Sc的几种存在形式与氟离子浓度的对数[1gc(F-)]、pH的关系如图1所示。已知c(F-)=5×10-4,“调pH”过程中控制pH=4.0,则调节pH值后三价Sc的存在形式为___________ (填化学式)。
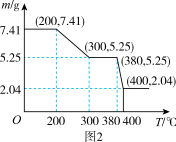
(5)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O分解得到ScF3,某固体样品质量与温度的关系如图2所示。加热至380-400℃产生白烟,400°C以上质量不再改变。则a___________ (填数字)。
(6)“水解”过程中,加水稀释后,TiOSO4水解为TiO2·xH2O的离子方程式为___________ ;应控制溶液的pH值为___________ 。

已知:该工艺条件下,溶液中相关离子开始沉淀和完全沉淀的pH值如下表:
| 离子 | Fe2+ | Fe3+ | Al3+ | TiO2+ |
| 开始沉淀pH | 7.0 | 1.9 | 3.0 | 0.3 |
| 完全沉淀pH | 9.0 | 3.2 | 4.7 | 2.0 |
(2)“沉淀转化”过程中,需加入过量的草酸,其原因是
(3)“焙烧”过程中,生成Sc2O3的化学方程式为
(4)常温下,三价Sc的几种存在形式与氟离子浓度的对数[1gc(F-)]、pH的关系如图1所示。已知c(F-)=5×10-4,“调pH”过程中控制pH=4.0,则调节pH值后三价Sc的存在形式为

(5)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O分解得到ScF3,某固体样品质量与温度的关系如图2所示。加热至380-400℃产生白烟,400°C以上质量不再改变。则a

(6)“水解”过程中,加水稀释后,TiOSO4水解为TiO2·xH2O的离子方程式为
从铝土矿废料“赤泥”(主要成分为Al2O3、Fe2O3、TiO2、Sc2O3)中提钪与TiO2的一种工艺如下:
已知:该工艺条件下,溶液中相关离子开始沉淀和完全沉淀的pH值如下表:
(1)钪为21号元素,该元素在元素周期表中的位置是_______ 。
(2)“沉淀转化”过程中,需加入过量的草酸,其原因是_______ 。
(3)“焙烧”过程中,生成Sc2O3的化学方程式为_______ 。
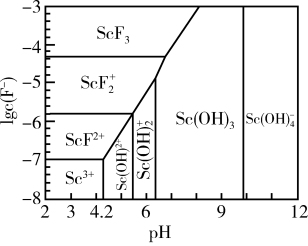
(4)常温下,三价Sc的几种存在形式与氟离子浓度的对数[lgc(F-)、pH的关系如图所示。已知c(F-)=1×10-5,“调pH”过程中控制pH=4.0,则调节pH值后三价Sc的存在形式为_______ (填化学式)。
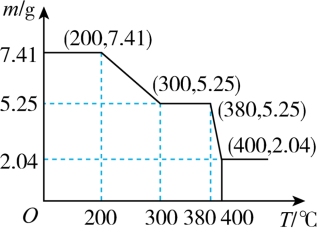
(5)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O分解得到ScF3,某固体样品质量与温度的关系如图所示。加热至380-400℃产生白烟,400℃以上质量不再改变。则a=_______ (填数字)。
(6)“水解”过程中,加水稀释后,TiOSO4水解为TiO2·xH2O的离子方程式为_______ ;应控制溶液的pH值为_______ 。

已知:该工艺条件下,溶液中相关离子开始沉淀和完全沉淀的pH值如下表:
| 离子 | Fe2+ | Fe3+ | Al3+ | TiO2+ |
| 开始沉淀pH | 7.0 | 1.9 | 3.0 | 0.3 |
| 完全沉淀pH | 9.0 | 3.2 | 4.7 | 2.0 |
(1)钪为21号元素,该元素在元素周期表中的位置是
(2)“沉淀转化”过程中,需加入过量的草酸,其原因是
(3)“焙烧”过程中,生成Sc2O3的化学方程式为
(4)常温下,三价Sc的几种存在形式与氟离子浓度的对数[lgc(F-)、pH的关系如图所示。已知c(F-)=1×10-5,“调pH”过程中控制pH=4.0,则调节pH值后三价Sc的存在形式为

(5)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O分解得到ScF3,某固体样品质量与温度的关系如图所示。加热至380-400℃产生白烟,400℃以上质量不再改变。则a=

(6)“水解”过程中,加水稀释后,TiOSO4水解为TiO2·xH2O的离子方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网