解答题-工业流程题 较难0.4 引用1 组卷1293
碳酸锶是重要的无机化工产品。利用锶渣(主要成分SrSO4,含少量CaCO3、Fe2O3、Al2O3、MgCO3杂质)制备超细碳酸锶的工艺如图:
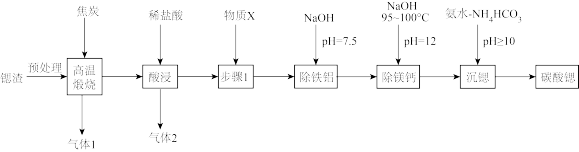
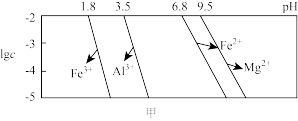
已知:25℃时溶液中金属离子物质的量浓度c与pH的关系如图甲所示:
回答下列问题:
(1)原料预处理的目的是加快煅烧反应速率,提高原料利用率。预处理方式可以是____ 。
(2)“高温煅烧”得到的主要产物为锶的硫化物和一种可燃性气体。则“高温煅烧”的主要反应化学方程式为____ 。
(3)气体2为____ 。步骤1的目的为____ ,不设置步骤1带来的后果是____ 。
(4)“除铁铝”过程维持温度在75℃的好处是____ 。“除铁铝”后溶液温度降至室温(25℃),溶液中c(Fe3+)为____ mol/L。(100.9=7.9)
(5)①写出“沉锶”的离子反应方程式:____ 。
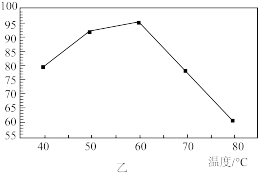
②反应温度对锶转化率的影响如图乙,温度高于60℃时,锶转化率降低的原因为____ 。

已知:25℃时溶液中金属离子物质的量浓度c与pH的关系如图甲所示:

回答下列问题:
(1)原料预处理的目的是加快煅烧反应速率,提高原料利用率。预处理方式可以是
(2)“高温煅烧”得到的主要产物为锶的硫化物和一种可燃性气体。则“高温煅烧”的主要反应化学方程式为
(3)气体2为
(4)“除铁铝”过程维持温度在75℃的好处是
(5)①写出“沉锶”的离子反应方程式:
②反应温度对锶转化率的影响如图乙,温度高于60℃时,锶转化率降低的原因为

2022·四川成都·一模
类题推荐
碳酸锶 主要用于制造磁性材料、电子元件等。利用锶渣(主要成分
主要用于制造磁性材料、电子元件等。利用锶渣(主要成分 ,含少量
,含少量 杂质),工业上制备超细碳酸锶的工艺如图1所示:
杂质),工业上制备超细碳酸锶的工艺如图1所示:
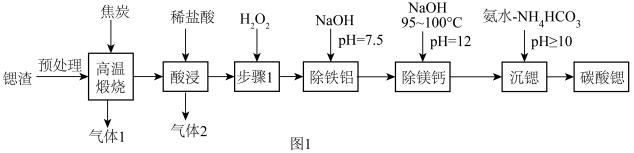
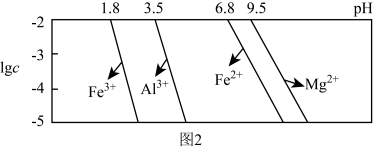
已知:①室温下,溶液中金属离子物质的量浓度 与溶液pH的关系如图2所示:
与溶液pH的关系如图2所示:
② 在不同温度下的溶解度如下表:
在不同温度下的溶解度如下表:
回答下列问题:
(1)“高温煅烧”得到的主要产物为锶的硫化物和一种可燃性气体。则“高温煅烧”的主要反应化学方程式为____________ 。
(2)“步骤1”的目的是____________ 。
(3)“除铁铝”后溶液温度降至室温,溶液中 为
为______  。
。
(4)“除镁钙”过程温度控制在95~100℃的目的是_____________________________________________ 。
(5)“沉锶”的离子反应方程式为_________________________ 。
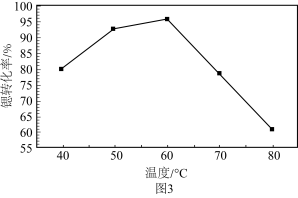
(6)“沉锶”过程中反应温度对锶转化率的影响如图3所示,温度高于60℃时,锶转化率降低的原因为_____________________________________
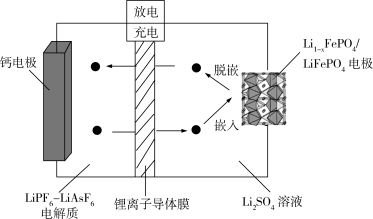
(7)如图为 可充放电电池的工作原理示意图,锂离子导体膜只允许
可充放电电池的工作原理示意图,锂离子导体膜只允许 通过,充电时,钙电极为
通过,充电时,钙电极为______ (“阳极”或“阴极”),放电时,正极上发生 的嵌入的电极反应是
的嵌入的电极反应是______ 。

已知:①室温下,溶液中金属离子物质的量浓度

②
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 90 | 100 |
| 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | 0.07 | |
| 0.91 | 1.77 | 3.95 | 8.42 | 20.20 | 44.50 | 91.20 |
(1)“高温煅烧”得到的主要产物为锶的硫化物和一种可燃性气体。则“高温煅烧”的主要反应化学方程式为
(2)“步骤1”的目的是
(3)“除铁铝”后溶液温度降至室温,溶液中
(4)“除镁钙”过程温度控制在95~100℃的目的是
(5)“沉锶”的离子反应方程式为
(6)“沉锶”过程中反应温度对锶转化率的影响如图3所示,温度高于60℃时,锶转化率降低的原因为

(7)如图为

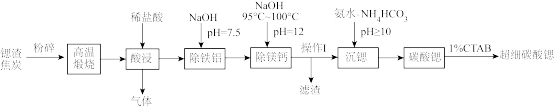
超细碳酸锶是重要的无机化工产品。利用锶渣(主要成分SrSO4,含少量CaCO3、Fe2O3、Al2O3、MgCO3等杂质)制备超细碳酸锶的工艺如下:
已知:①“高温煅烧”过程中发生的主要反应为:SrSO4+4C SrS+4CO↑
SrS+4CO↑
②Sr(OH)2、Ca(OH)2在不同温度下的溶解度表(g/100mLH2O)
回答下列问题:
(1)“粉碎”的目的是_______
(2)“酸浸”过程中主要反应的化学方程式为_______
(3)“除铁铝”过程中温度控制在75℃左右,适宜的加热方式为_______
(4)“操作I”为_______
(5)①写出“沉锶”的离子方程式_______
②反应温度对锶转化率的影响如图,温度高于60℃时,“锶转化率”降低的原因为_______ 。
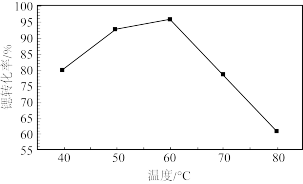
③从平衡移动的角度分析“沉锶”过程中控制pH≥10的原因_______ 。

已知:①“高温煅烧”过程中发生的主要反应为:SrSO4+4C
②Sr(OH)2、Ca(OH)2在不同温度下的溶解度表(g/100mLH2O)
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 90 | 100 |
| 氢氧化钙 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | 0.07 |
| 氢氧化锶 | 0.91 | 1.77 | 3.95 | 8.42 | 20.20 | 44.50 | 91.20 |
回答下列问题:
(1)“粉碎”的目的是
(2)“酸浸”过程中主要反应的化学方程式为
(3)“除铁铝”过程中温度控制在75℃左右,适宜的加热方式为
(4)“操作I”为
(5)①写出“沉锶”的离子方程式
②反应温度对锶转化率的影响如图,温度高于60℃时,“锶转化率”降低的原因为

③从平衡移动的角度分析“沉锶”过程中控制pH≥10的原因
碳酸锶纯品是重要的无机化工产品。一种利用含锶矿渣(主要成分为SrSO4,还含有少量CaCO3和FeO)生产高纯碳酸锶的流程如图:
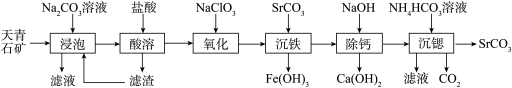
已知:①Ksp(SrSO4)=3.2×10-7,Ksp(SrCO3)=1.6×10-10
②Sr(OH)2、Ca(OH)2在不同温度下的溶解度表(g/100mLH2O)
③“除钙”时,控制溶液温度95℃~100℃,向滤液中加入NaOH溶液,调节pH≥12,趁热过滤得Ca(OH)2沉淀。
(1)浸泡后所得滤液中c(CO )=2.0×10-3mol•L-1,则c(SO
)=2.0×10-3mol•L-1,则c(SO )=
)=_____ 。
(2)“氧化”反应的离子反应方程式为_____ 。
(3)“沉铁”反应的离子反应方程式为_____ 。
(4)“沉锶”也可以使用Na2CO3溶液,但使用Na2CO3溶液可能会生成杂质。使用Na2CO3溶液可能会生成杂质及原因是_____ 。

已知:①Ksp(SrSO4)=3.2×10-7,Ksp(SrCO3)=1.6×10-10
②Sr(OH)2、Ca(OH)2在不同温度下的溶解度表(g/100mLH2O)
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 90 | 100 |
| Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | 0.07 |
| Sr(OH)2 | 0.91 | 1.77 | 3.95 | 8.42 | 20.20 | 44.50 | 91.20 |
(1)浸泡后所得滤液中c(CO
(2)“氧化”反应的离子反应方程式为
(3)“沉铁”反应的离子反应方程式为
(4)“沉锶”也可以使用Na2CO3溶液,但使用Na2CO3溶液可能会生成杂质。使用Na2CO3溶液可能会生成杂质及原因是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


