解答题-工业流程题 适中0.65 引用4 组卷159
甲烷在工业上有很多用途。回答下列问题:
Ⅰ.利用甲烷催化还原 消除氮氧化物的污染:
消除氮氧化物的污染:
ⅰ. ;
;
ⅱ. ;
;
ⅲ. 。
。
其中: 。
。
(1)
_______ (用含a、b的代数式表示)。
(2)在4L某恒容密闭容器中充入 和
和 ,只发生反应ⅲ,
,只发生反应ⅲ, 的平衡转化率
的平衡转化率 随温度的变化关系如图所示。
随温度的变化关系如图所示。
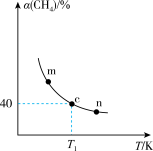
①曲线上m、n两点的正反应速率:
_______ (填“>”、“<”或“=”) 。
。
②T1时,若反应进行到 时达到平衡,此时测得混合气体的总压强为
时达到平衡,此时测得混合气体的总压强为 ,则
,则 内,
内,
_______  ,反应平衡常数
,反应平衡常数
_______  (用分压表示,分压=物质的量分数×总压)。
(用分压表示,分压=物质的量分数×总压)。
③下列说法正确的是_______ (填标号)。
A.当混合气体的密度不再随时间改变时,该反应达到平衡
B.该反应的反应物的键能总和小于生成物的键能总和
C.降低温度,有利于提高 的转化率,反应平衡常数也增大
的转化率,反应平衡常数也增大
D.加入合适的催化剂, 的值增大
的值增大
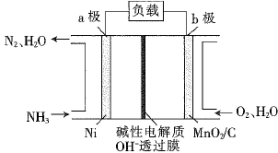
(3)甲烷-氧气燃料电池的工作原理如图所示(L、K均为惰性电极,气体已换算成标准状况)。
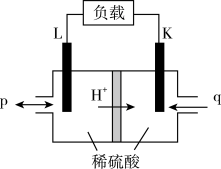
①电池工作时,K电极上发生_______ (填“还原反应”或“氧化反应”)。
②L电极上的电极反应式为_______ 。
③每消耗 ,电路中转移电子的物质的量为
,电路中转移电子的物质的量为_______ mol。
Ⅰ.利用甲烷催化还原
ⅰ.
ⅱ.
ⅲ.
其中:
(1)
(2)在4L某恒容密闭容器中充入

①曲线上m、n两点的正反应速率:
②T1时,若反应进行到
③下列说法正确的是
A.当混合气体的密度不再随时间改变时,该反应达到平衡
B.该反应的反应物的键能总和小于生成物的键能总和
C.降低温度,有利于提高
D.加入合适的催化剂,
(3)甲烷-氧气燃料电池的工作原理如图所示(L、K均为惰性电极,气体已换算成标准状况)。

①电池工作时,K电极上发生
②L电极上的电极反应式为
③每消耗
21-22高二下·河南·阶段练习
类题推荐
我国提出争取在2030年前实现碳达峰,2060年前实现碳中和,这对于改善环境、实现绿色发展至关重要。回答下列问题:
(1)若
 。已知有关物质的化学键键能数据如下表:
。已知有关物质的化学键键能数据如下表:
则 的键能
的键能
______  。
。
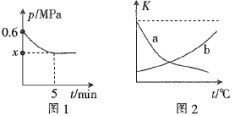
(2)利用 合成甲醇也是有效利用
合成甲醇也是有效利用 资源的重要途径。将原料气
资源的重要途径。将原料气 充入2L恒容密闭容器中,只发生
充入2L恒容密闭容器中,只发生
 ,在不同催化剂作用下,反应
,在不同催化剂作用下,反应 时
时 的转化率随温度的变化如图所示:
的转化率随温度的变化如图所示:

①若起始时CO2和H2的物质的量分别为1.5mol、4.5mol。2min末反应达到平衡,此时测得水和甲醇的物质的量之和为1.0mol,则此时容器内氢气的体积分数为______ 。
②图中e点,
______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③下列说法错误的是______ (填字母)。
A.当温度 时,选择催化剂Ⅰ
时,选择催化剂Ⅰ  的转化率更高
的转化率更高
B. 的平衡常数大于
的平衡常数大于 的平衡常数
的平衡常数
C.若容器内混合气体的密度不再变化时,该反应已达到平衡状态
D.c点转化率比a点低的原因一定是温度升高平衡逆向移动, 转化率降低
转化率降低
(3)工业上在Cu-ZnO催化下利用CO2发生如下反应Ⅰ生产甲醇,同时伴有反应Ⅱ发生。温度T时,在容积不变的密闭容器中充入 和
和 ,起始压强为
,起始压强为 ,10min达平衡时生成
,10min达平衡时生成 ,测得压强为
,测得压强为 。
。
Ⅰ.

Ⅱ.

①若反应速率用单位时间内分压变化表示,则10min内生成H2O的反应速率 为
为______  。
。
②计算出反应Ⅱ的平衡常数
______ ( 为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。
为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。
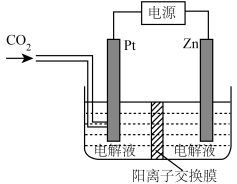
(4)将CH4与CO2利用电解装置进行耦合转化,其原理示意如图所示:
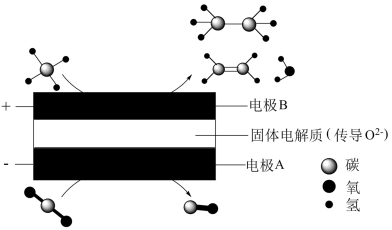
①电池工作时,电极A的电极反应式为____________ 。
②若两极恰好消耗标准状况下33.6LCH4和22.4LCO2,则生成乙烷的物质的量为______ mol。
(1)若
化学键 | |||||
键能/( | 436 | 343 | a | 413 | 465 |
(2)利用

①若起始时CO2和H2的物质的量分别为1.5mol、4.5mol。2min末反应达到平衡,此时测得水和甲醇的物质的量之和为1.0mol,则此时容器内氢气的体积分数为
②图中e点,
③下列说法错误的是
A.当温度
B.
C.若容器内混合气体的密度不再变化时,该反应已达到平衡状态
D.c点转化率比a点低的原因一定是温度升高平衡逆向移动,
(3)工业上在Cu-ZnO催化下利用CO2发生如下反应Ⅰ生产甲醇,同时伴有反应Ⅱ发生。温度T时,在容积不变的密闭容器中充入
Ⅰ.
Ⅱ.
①若反应速率用单位时间内分压变化表示,则10min内生成H2O的反应速率
②计算出反应Ⅱ的平衡常数
(4)将CH4与CO2利用电解装置进行耦合转化,其原理示意如图所示:

①电池工作时,电极A的电极反应式为
②若两极恰好消耗标准状况下33.6LCH4和22.4LCO2,则生成乙烷的物质的量为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网